Clear Sky Science · ru
Центральный и периферический аналгезия у облучённых крыс: модель боли, вызванной резерпином
Почему важно облегчать длительную боль
Многие люди живут с ежедневной болью, которую обычные обезболивающие лишь частично устраняют и которые часто сопровождаются нежелательными побочными эффектами. В этом исследовании рассмотрен нетривиальный помощник: очень низкие дозы гамма‑излучения — того же типа энергии, который применяют в гораздо больших дозах при лечении рака. На модели крыс, имитирующей некоторые черты хронической широко распространённой боли, учёные проверяли, может ли однократная низкая доза радиации безопасно уменьшить боль и что при этом происходит в организме и мозге.
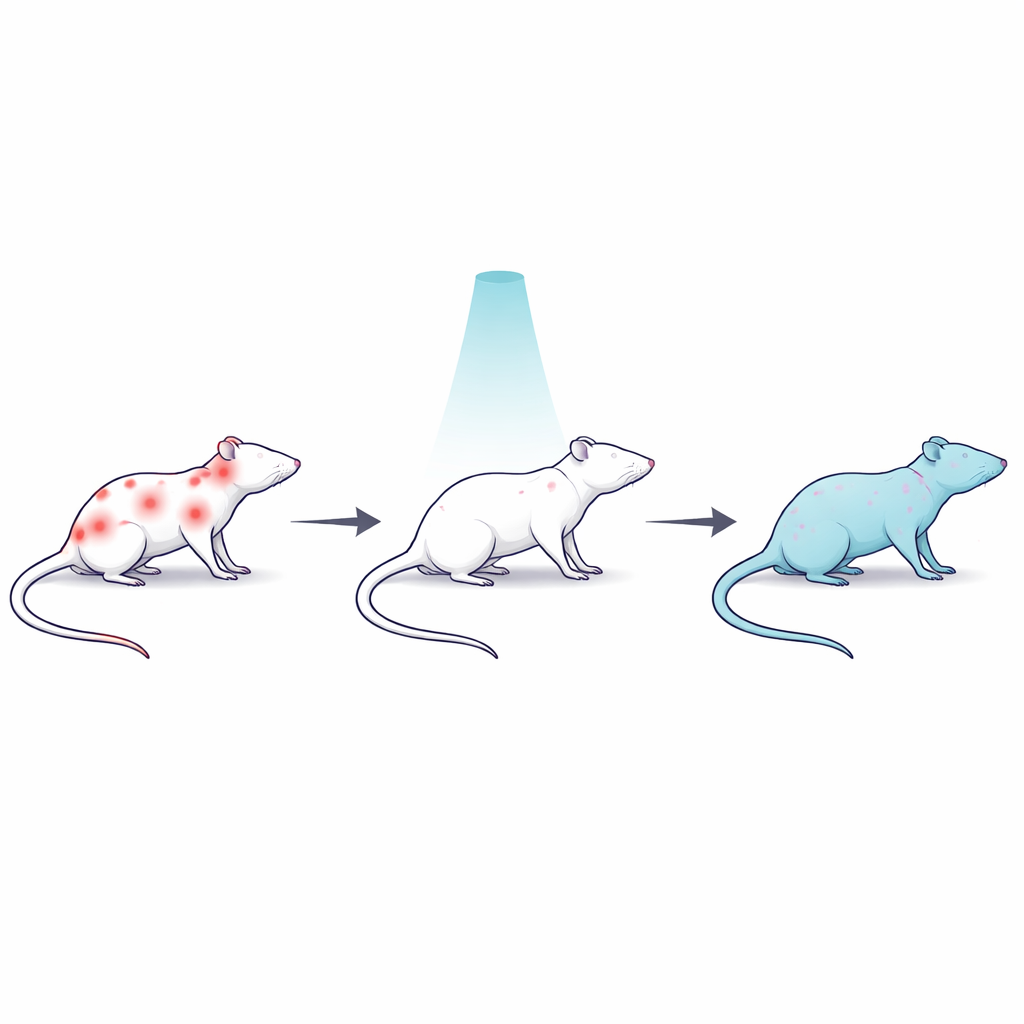
Модель упрямой, по всему телу распространяющейся боли у крыс
Чтобы изучить трудно поддающуюся лечению боль, учёные использовали препарат резерпин, который истощает ключевые мозговые вещества, участвующие в регуляции настроения и боли, и вызывает длительную мышечную и общую телесную боль у крыс. Тридцать самцов крыс разделили на несколько групп: здоровый контроль; группа резерпина с необработанной болью; группа резерпина, получившая однократную облучение всего тела низкой дозой гамма‑лучей; аналогичная облучённая группа, которая также получала налоксон — препарат, блокирующий опиоидные рецепторы в мозге; и группа резерпина, лечившаяся распространённым противовоспалительным обезболивающим диклофенаком. Такой дизайн позволил команде сравнить радиацию со стандартным препаратом и проверить, вносит ли вклад собственная опиоидоподобная система организма в возможное облегчение боли.
Тестирование боли и исследование мозга
Исследователи измеряли боль двумя способами. В тесте «хлыст‑рефлекс» (tail‑flick) хвост крысы помещают в тёплую воду, и время до того, как она отдернёт хвост, отражает чувствительность периферических нервов. В тесте Хаффнера с прищепкой (tail‑clip) небольшую прищепку мягко закрепляют близ основания хвоста, и время до реакции крысы — поворота, чтобы укусить прищепку — отражает обработку боли в спинном мозге и мозге. После этих тестов учёные собирали кровь и ткани мозга для измерения маркеров, связанных с болью и стрессом тканей: субстанции P и фактора некроза опухоли‑альфа в крови (оба связаны с болью и воспалением), а также оксида азота и малонового диальдегида (показатели окислительного, «ржавеющего», стресса) и дофамина (медиатор, участвующий в настроении и контроле боли) в мозге.
Неожиданный профиль обезболивания после облучения
Резерпин значительно повышал чувствительность к боли в обоих тестах и нарушал внутреннюю химию организма: показатели окислительного стресса и воспалительные сигналы росли, тогда как уровень дофамина в мозге падал. Однократная низкая доза гамма‑излучения обратила многие из этих изменений. Реакции на боль в обоих тестах замедлились, то есть крысы переносили больше дискомфорта до появления реакции. Для боли, передаваемой периферическими нервами хвоста, эффект радиации был схож с действием диклофенака. Для боли, затрагивающей спинной и головной мозг, радиация также снижала чувствительность, но это преимущество в основном исчезало при предварительном введении налоксона. Такая картина указывает на то, что низкодозное облучение запускает, по крайней мере частично, собственные опиоидоподобные системы организма, ослабляющие боль, помимо успокоения чрезмерно активных нервов.
Меньше химического «штормa», больше равновесия
На химическом уровне радиация очевидно смягчала внутренний «шторм», вызванный резерпином. Уровни оксида азота и малонового диальдегида в мозге снизились к норме, что указывает на уменьшение окислительного стресса. Содержание дофамина в мозге, подавленное резерпином, восстановилось после облучения. В крови повышенный уровень провоспалительного фактора некроза опухоли‑альфа и связанного с болью нейропептида субстанции P также снизился после низкой дозы. Блокирование опиоидных рецепторов налоксоном не отменяло этих антиоксидантных и противовоспалительных сдвигов, указывая на то, что химическое успокоение, вызванное радиацией, и её опиоид‑связанные сигнальные эффекты по крайней мере частично различны. Диклофенак тоже улучшал многие из этих показателей, но в отличие от стандартных препаратов низкодозная радиация делала это при однократном воздействии и без известных желудочно‑кишечных и сердечно‑сосудистых рисков длительного приёма противовоспалительных таблеток.
Что это может значить для будущей помощи при боли
Проясняя простыми словами, исследование показывает, что аккуратно контролируемая низкая доза гамма‑излучения может сделать болевые нервы менее возбудимыми, помочь восстановить защитные мозговые нейромедиаторы и утихомирить как окислительные, так и воспалительные сигналы, питающие хроническую боль. Работа выполнена на одной модели крыс с одной дозой радиации и в одной короткой временной точке, поэтому её пока нельзя напрямую переносить на пациентов. Тем не менее результаты поддерживают клинические наблюдения о том, что низкодозовая лучевая терапия может облегчать упрямую боль в суставах и сухожилиях, и указывают на конкретные биологические пути — антиоксидантную защиту, контроль воспаления и опиоид‑связанные нервные цепи — которые будущие целевые терапии, основанные на радиации или препаратах, могли бы безопасно использовать, чтобы помочь людям, живущим с хронической болью.
Цитирование: Saif-Elnasr, M. Central and peripheral analgesia in irradiated rats: reserpine-induced pain model. Sci Rep 16, 12193 (2026). https://doi.org/10.1038/s41598-026-44637-8
Ключевые слова: хроническая боль, низкодозная радиация, окислительный стресс, воспаление, опиоидные пути