Clear Sky Science · fr
Analgésie centrale et périphérique chez des rats irradiés : modèle de douleur induite par la réserpine
Pourquoi soulager la douleur persistante importe
Beaucoup de personnes vivent avec une douleur quotidienne que les analgésiques classiques soulagent seulement en partie et qui s’accompagne souvent d’effets indésirables préoccupants. Cette étude explore un auxiliaire inhabituel : des doses très faibles de rayonnement gamma, le même type d’énergie utilisé à des niveaux bien plus élevés pour traiter le cancer. À partir d’un modèle de rat qui reproduit certains aspects de la douleur chronique généralisée, les chercheurs ont demandé si une seule faible dose de radiation pouvait réduire la douleur en toute sécurité et ce qui pourrait se passer dans le corps et le cerveau lorsque cela arrive.
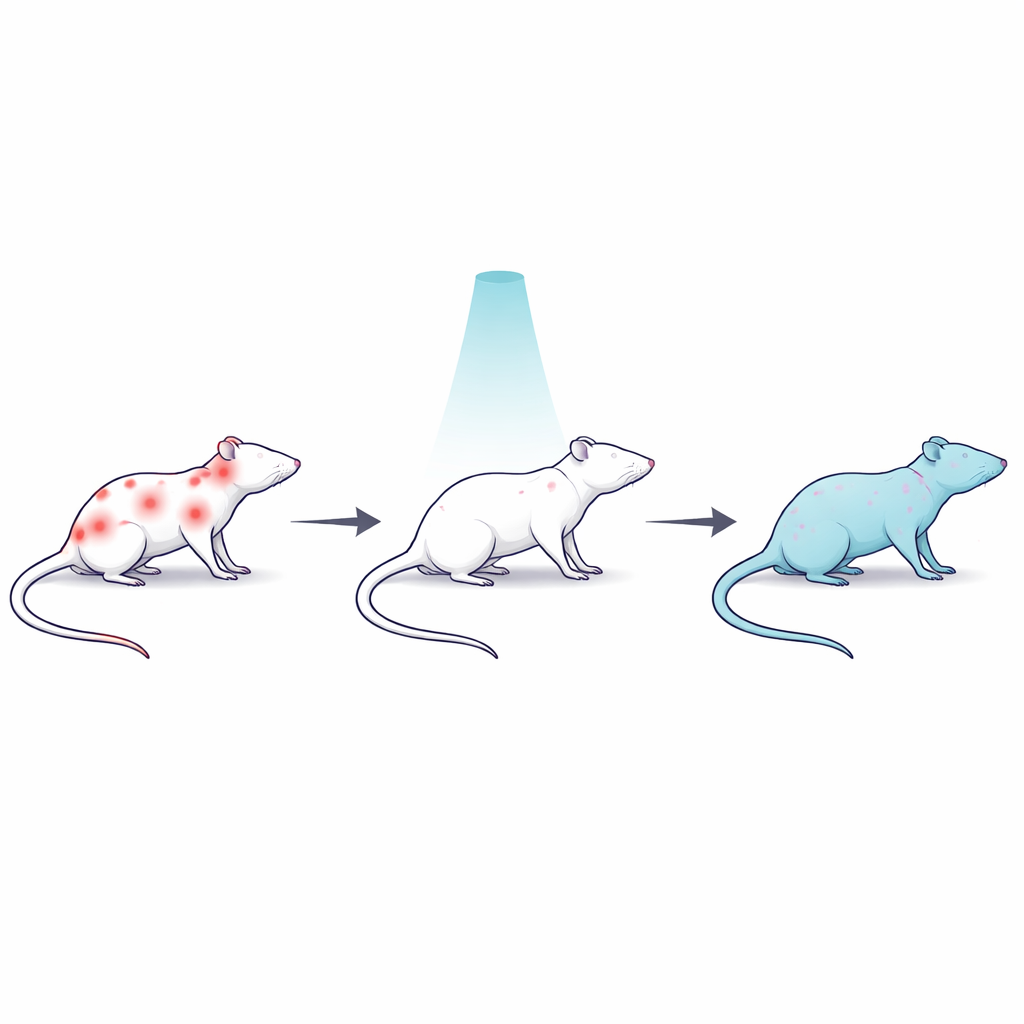
Un modèle de rat pour une douleur tenace et généralisée
Pour étudier une douleur difficile à traiter, les scientifiques ont utilisé la réserpine, un médicament qui vide des neurotransmetteurs clés impliqués dans l’humeur et le contrôle de la douleur et qui provoque chez le rat une douleur musculaire et corporelle durable. Trente rats mâles ont été répartis en plusieurs groupes : un groupe témoin sain ; un groupe réserpine sans traitement ; un groupe réserpine ayant reçu une seule irradiation gamma corps entier à faible dose ; un groupe irradié similaire ayant également reçu de la naloxone, un médicament qui bloque les récepteurs opioïdes du cerveau ; et un groupe réserpine traité avec le classique anti‑inflammatoire diclofénac. Cette conception a permis à l’équipe de comparer la radiation à un médicament standard et de tester si les systèmes opioïdes endogènes contribuaient à un éventuel soulagement de la douleur.
Mesurer la douleur et sonder le cerveau
Les chercheurs ont évalué la douleur de deux manières. Dans le test du battement de queue (tail‑flick), la queue du rat est placée dans de l’eau chaude et le temps avant qu’il la retire reflète la sensibilité de la douleur des nerfs périphériques. Dans le test de pince de Haffner (tail‑clip), une petite pince est appliquée près de la base de la queue, et le temps avant que le rat réagisse en se tournant pour mordre reflète le traitement de la douleur au niveau de la moelle épinière et du cerveau. Après ces tests, les scientifiques ont prélevé du sang et du tissu cérébral pour mesurer des marqueurs associés à la douleur et au stress tissulaire : la substance P et le facteur de nécrose tumorale alpha (tous deux liés à la douleur et à l’inflammation) dans le sang, et le monoxyde d’azote et le malondialdéhyde (signaux de stress oxydatif) ainsi que la dopamine (un messager impliqué dans l’humeur et le contrôle de la douleur) dans le cerveau.
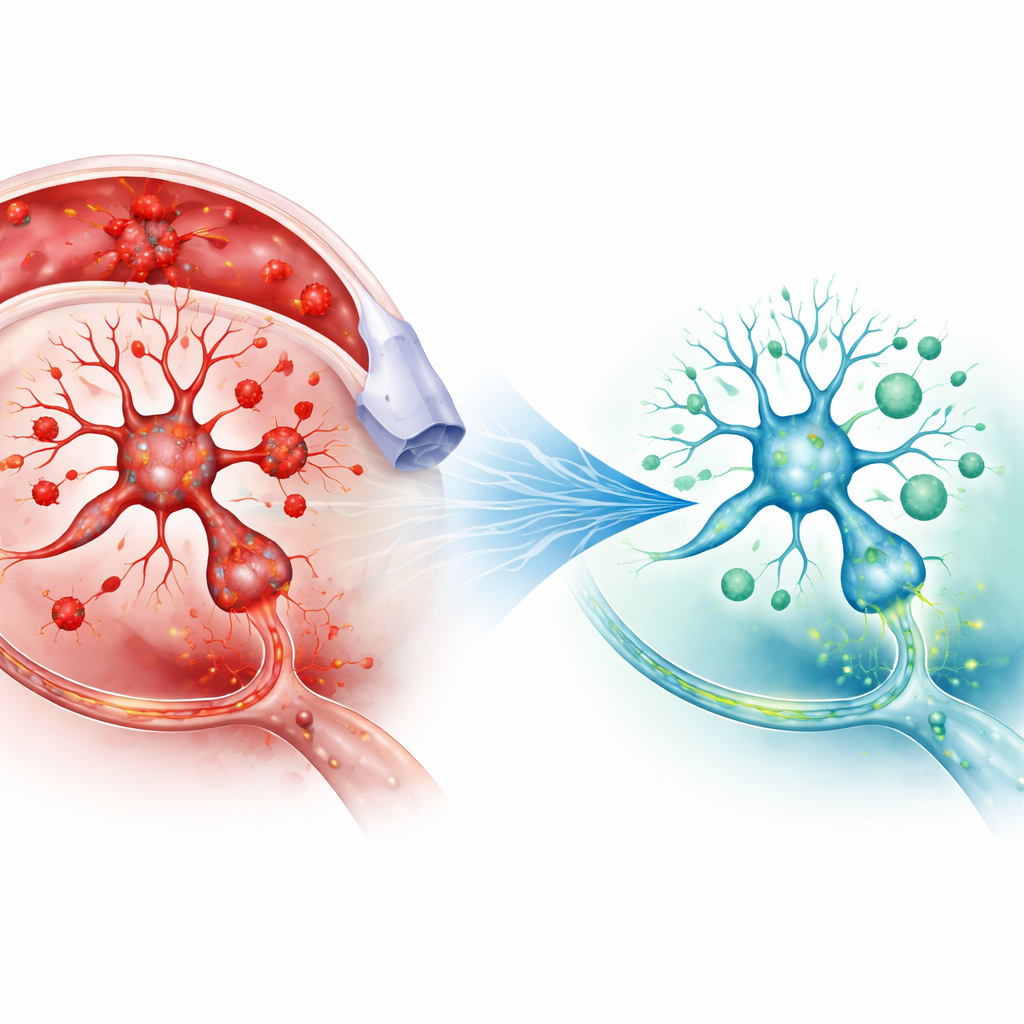
Un profil surprenant d’atténuation de la douleur par la radiation
La réserpine a rendu les rats beaucoup plus sensibles à la douleur dans les deux tests et a perturbé leur chimie interne : les marqueurs de stress oxydatif et les signaux inflammatoires ont augmenté, tandis que la dopamine cérébrale a diminué. Une seule faible dose de rayonnement gamma a inversé bon nombre de ces changements. Les réponses douloureuses dans les deux tests ont été retardées, ce qui signifie que les rats ont toléré davantage d’inconfort avant de réagir. Pour la douleur véhiculée par les nerfs de la queue, l’effet de la radiation était similaire à celui du diclofénac. Pour la douleur impliquant le cerveau et la moelle épinière, la radiation a à nouveau réduit la sensibilité, mais ce bénéfice a largement disparu lorsque la naloxone était administrée au préalable. Ce schéma suggère que la radiation à faible dose déclenche, au moins en partie, les systèmes analgésiques opioïdes endogènes en plus de calmer des nerfs hyperactifs.
Moins de « tempête » chimique, plus d’équilibre
Au niveau chimique, la radiation a nettement atténué la « tempête » interne provoquée par la réserpine. Les taux de monoxyde d’azote et de malondialdéhyde dans le cerveau sont retombés vers la normale, indiquant une réduction du stress oxydatif. La teneur en dopamine cérébrale, qui avait été abaissée par la réserpine, a rebondi après l’irradiation. Dans le sang, le messager inflammatoire élevé, le facteur de nécrose tumorale alpha, et le neuropeptide lié à la douleur, la substance P, ont tous deux diminué après la faible dose. Le blocage des récepteurs opioïdes par la naloxone n’a pas annulé ces modifications antioxydantes et anti‑inflammatoires, ce qui indique que l’effet calmant chimique de la radiation et ses effets liés aux voies opioïdes sont au moins en partie distincts. Le diclofénac a également amélioré bon nombre de ces paramètres, mais à la différence des médicaments conventionnels, la radiation à faible dose l’a fait avec une seule exposition et sans les risques digestifs et cardiovasculaires connus d’un usage prolongé d’anti‑inflammatoires.
Ce que cela pourrait signifier pour la prise en charge future de la douleur
En termes pratiques, l’étude suggère qu’une dose contrôlée et faible de rayonnement gamma peut rendre les nerfs sensibles à la douleur moins réactifs, contribuer à restaurer des messagers cérébraux protecteurs et calmer à la fois les signaux oxydatifs et inflammatoires qui entretiennent la douleur chronique. Les travaux ont été réalisés dans un seul modèle de rat avec une dose unique et un seul point temporel bref, ils ne peuvent donc pas encore être traduits directement aux patients. Néanmoins, ils corroborent des observations cliniques selon lesquelles la radiothérapie à faible dose peut soulager des douleurs articulaires et tendineuses rebelles, et ils mettent en évidence des voies biologiques concrètes — défenses antioxydantes, contrôle de l’inflammation et circuits nerveux liés aux opioïdes — que de futures thérapies ciblées, qu’elles reposent sur la radiation ou des médicaments, pourraient exploiter en toute sécurité pour aider les personnes vivant avec une douleur chronique.
Citation: Saif-Elnasr, M. Central and peripheral analgesia in irradiated rats: reserpine-induced pain model. Sci Rep 16, 12193 (2026). https://doi.org/10.1038/s41598-026-44637-8
Mots-clés: douleur chronique, radiation à faible dose, stress oxydatif, inflammation, voies opioïdes