Clear Sky Science · ar
التسكين المركزي والمحيطي في فئران مُشعَّة: نموذج الألم المحفَّز بالريزرپين
لماذا يهم تخفيف الألم طويل الأمد
يعيش كثير من الناس مع ألم يومي لا توفر المسكنات التقليدية سوى تخفيف جزئي له، وغالبًا ما يرافق هذه الأدوية آثار جانبية مزعجة. تستكشف هذه الدراسة مساعدًا غير مألوف: جرعات منخفضة جدًا من أشعة غاما، وهي نفس نوع الطاقة المستخدم بجرعات أعلى بكثير لعلاج السرطان. باستخدام نموذج فأر يحاكي بعض خصائص الألم المزمن المنتشر بالجسم، سأل الباحثون ما إذا كانت جرعة واحدة منخفضة من الإشعاع قد تقلل الألم بأمان، وما الذي قد يحدث داخل الجسم والدماغ حين يفعل ذلك.
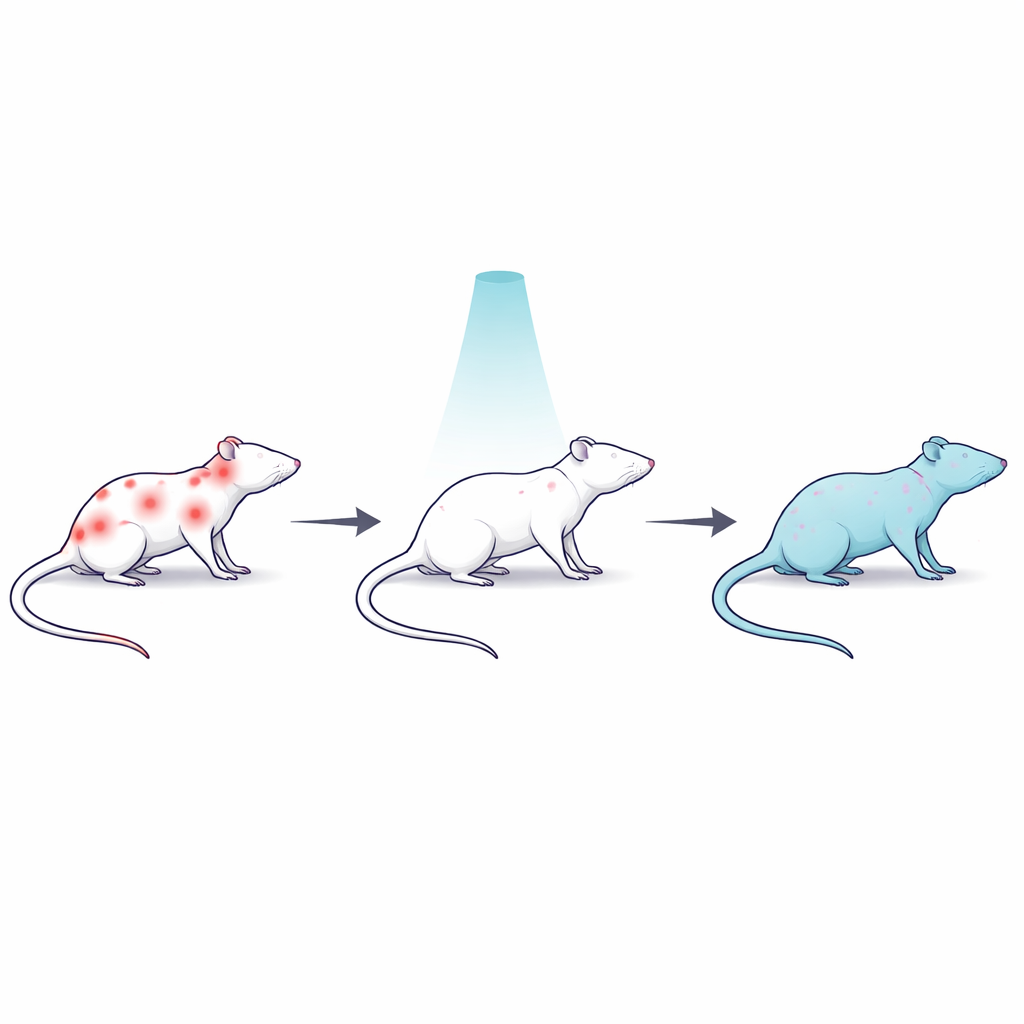
نموذج فأر لألم عنيد يشمل الجسم كله
لدراسة الألم الذي يصعب علاجه، استخدم العلماء الدواء ريزرپين، الذي يستنفد مواد كيميائية دماغية أساسية متعلقة بالمزاج والتحكم بالألم ويُحدث ألمًا عضليًا وجسديًا طويل الأمد في الفئران. قسّموا ثلاثين ذكرًا من الفئران إلى عدة مجموعات: مجموعة ضابطة سليمة؛ مجموعة ريزرپين مصابة بالألم دون علاج؛ مجموعة ريزرپين تلقت جرعة واحدة من إشعاع غاما منخفضة على كامل الجسم؛ مجموعة مشعة مماثلة تلقت أيضًا نالوكسون، وهو دواء يحجب مستقبلات المواد الأفيونية في الدماغ؛ ومجموعة ريزرپين عولجت بمسكن مضاد للالتهاب شائع هو ديكلوفيناك. سمح هذا التصميم للفريق بمقارنة الإشعاع مع دواء قياسي واختبار ما إذا كانت أنظمة الجسم الشبيهة بالأفيون تساهم في أي تخفيف للألم.
اختبار الألم وفحص الدماغ
قاس الباحثون الألم بطريقتين. في اختبار رفرفة الذيل، يُوضع ذيل الفأر في ماء دافئ ويعكس زمن الرفرفة حتى الانسحاب حساسية الألم في الأعصاب المحيطية خارج الدماغ والحبل الشوكي. في اختبار مشبك الذيل لهافنر، يُطبَّق مشبك صغير بلطف قرب قاعدة الذيل، والزمن قبل أن يتفاعل الفأر بالدوران والعض يعكس معالجة الألم في الحبل الشوكي والدماغ. بعد هذه الاختبارات جمع العلماء الدم وأنسجة الدماغ لقياس مؤشرات مرتبطة بالألم وإجهاد الأنسجة: السابستنس P والعامل النخر الورمي-ألفا (كلاهما مرتبط بالألم والالتهاب) في الدم، وأكسيد النيتريك والمالونديالدهيد (إشارات الإجهاد التأكسدي أو «الصدأي») بالإضافة إلى الدوبامين (ناقل عصبي يشارك في المزاج والتحكم بالألم) في الدماغ.
نمط مفاجئ لتأثير الإشعاع على الألم
أحدث الريزرپين حساسية أكبر للألم في كلا الاختبارين وخلّ في كيمياء الجسم الداخلية: ارتفعت مؤشرات الإجهاد التأكسدي والإشارات الالتهابية، بينما انخفض الدوبامين الدماغي. قلبت جرعة واحدة منخفضة من إشعاع غاما العديد من هذه التغيرات. تأخرت استجابات الألم في كلا الاختبارين، ما يعني أن الفئران تحملت مزيدًا من الانزعاج قبل التفاعل. بالنسبة للألم الناقل عبر أعصاب الذيل، كان تأثير الإشعاع مشابهًا لتأثير الديكلوفيناك. أما بالنسبة للألم الذي يشمل الدماغ والحبل الشوكي، فقد قللت الإشعاع الحساسية أيضًا، لكن هذه الفائدة اختفت إلى حد كبير عندما أُعطي نالوكسون أولًا. يشير هذا النمط إلى أن الإشعاع منخفض الجرعة يثير، على الأقل جزئيًا، أنظمة الجسم الشبيهة بالأفيون المهدئة للألم بالإضافة إلى تهدئته للأعصاب المفرطة النشاط.
عاصفة كيميائية أخف، وتوازن أكبر
على المستوى الكيميائي، خفف الإشعاع بوضوح «العاصفة» الداخلية التي أثارها الريزرپين. انخفضت مستويات أكسيد النيتريك والمالونديالدهيد في الدماغ باتجاه المعدلات الطبيعية، مما يشير إلى تقليل الإجهاد التأكسدي. تعافى محتوى الدوبامين في الدماغ، الذي كان قد انخفض بفعل الريزرپين، بعد التعرض للإشعاع. في مجرى الدم، هبطت المستويات المرتفعة للرسول الالتهابي العامل النخر الورمي-ألفا والپپتيد العصبي المرتبط بالألم السابستنس P بعد الجرعة المنخفضة. لم يلغِ حجب مستقبلات الأفيون بالنالوكسون هذه التحولات المضادة للأكسدة والمضادة للالتهاب، مما يدل على أن التهدئة الكيميائية للإشعاع وتأثيراته المتعلقة بإشارات الأفيون منفصلتان جزئيًا على الأقل. حسّن الديكلوفيناك أيضًا كثيرًا من هذه المقاييس، لكن خلافًا للأدوية القياسية، فعل الإشعاع منخفض الجرعة ذلك بتعرض واحد ودون المخاطر الهضمية والقلبية الوعائية المعروفة مع تناول مسكنات مضادة للالتهاب على المدى الطويل.
ماذا قد يعني هذا لرعاية الألم في المستقبل
بعبارات بسيطة، تقترح الدراسة أن جرعة خاضعة للضبط من أشعة غاما منخفضة قد تجعل أعصاب الإحساس بالألم أقل انفعالًا، وتساعد في استعادة المواد الكيميائية الوقائية في الدماغ، وتكبح إشارات الإجهاد التأكسدي والالتهابي التي تسهم في الألم المزمن. أُجريت التجربة في نموذج فأر واحد وبجرعة إشعاع واحدة ونقطة زمنية قصيرة واحدة فقط، لذا لا يمكن ترجمتها مباشرة إلى المرضى بعد. ومع ذلك، فهي تدعم ملاحظات سريرية تفيد أن العلاج الإشعاعي منخفض الجرعة يمكن أن يخفف آلام المفاصل والأوتار العنيدة، وتشير إلى مسارات بيولوجية ملموسة — دفاعات مضادة للأكسدة، ضبط الالتهاب، ودارات أعصاب مرتبطة بالأفيون — يمكن للعلاجات المستقبلية المستهدفة، سواء القائمة على الإشعاع أو الأدوية، أن تستغلها بأمان لمساعدة الأشخاص الذين يعيشون مع الألم المزمن.
الاستشهاد: Saif-Elnasr, M. Central and peripheral analgesia in irradiated rats: reserpine-induced pain model. Sci Rep 16, 12193 (2026). https://doi.org/10.1038/s41598-026-44637-8
الكلمات المفتاحية: ألم مزمن, إشعاع منخفض الجرعة, الإجهاد التأكسدي, الالتهاب, مسارات المواد الأفيونية