Clear Sky Science · es
Analgesia central y periférica en ratas irradiadas: modelo de dolor inducido por reserpina
Por qué aliviar el dolor persistente importa
Mucha gente vive con dolor diario que los analgésicos habituales solo alivian parcialmente y que a menudo vienen con efectos secundarios preocupantes. Este estudio explora un ayudante poco habitual: dosis muy bajas de radiación gamma, el mismo tipo de energía que se emplea a niveles mucho mayores para tratar el cáncer. Usando un modelo en ratas que imita algunos rasgos del dolor crónico generalizado, los investigadores preguntaron si una única dosis baja de radiación podría reducir el dolor de forma segura y qué podría estar ocurriendo dentro del cuerpo y el cerebro cuando lo hace.
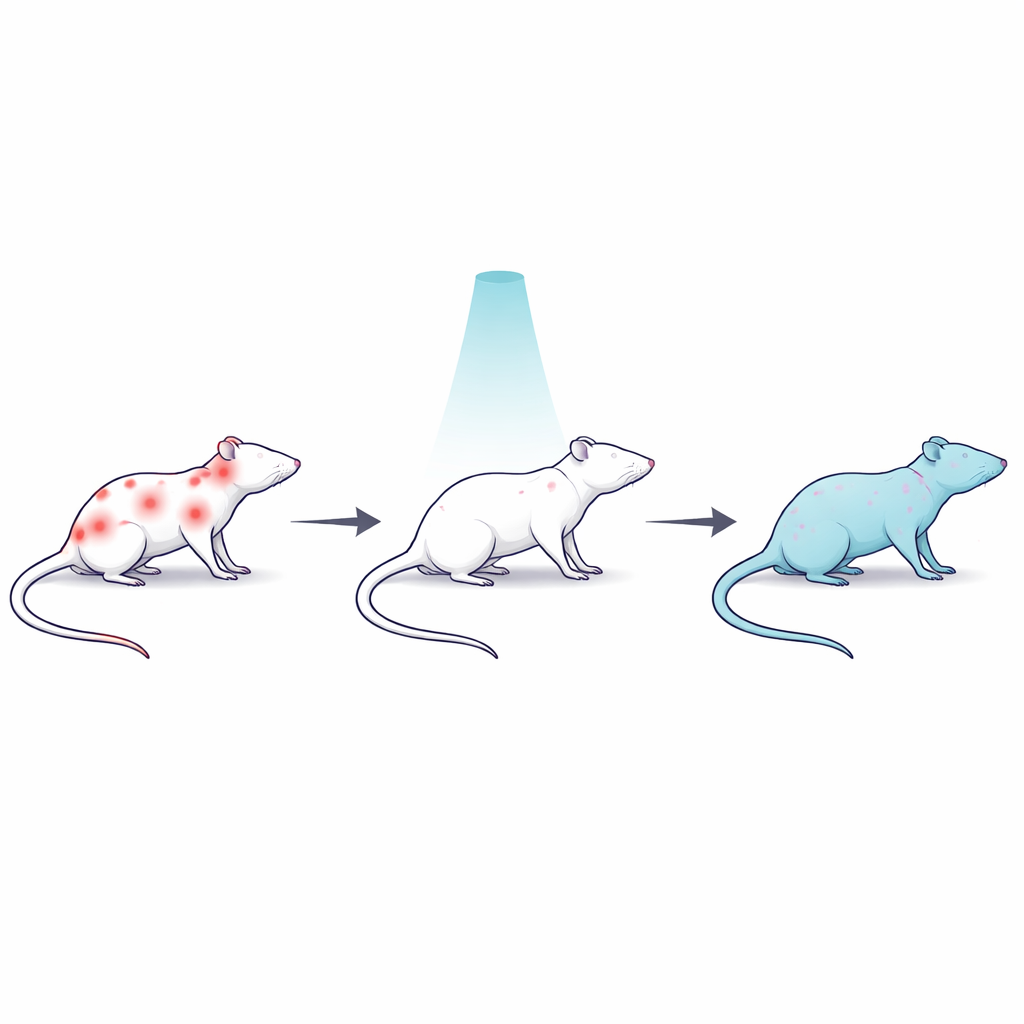
Un modelo de rata para el dolor corporal persistente
Para estudiar el dolor difícil de tratar, los científicos emplearon la reserpina, un fármaco que agota químicos cerebrales clave implicados en el estado de ánimo y el control del dolor y que produce dolor muscular y corporal de larga duración en ratas. Treinta ratas macho se dividieron en varios grupos: un grupo control sano; un grupo con reserpina y dolor sin tratar; un grupo con reserpina que recibió una única dosis corporal total de radiación gamma a baja dosis; un grupo irradiado similar que además recibió naloxona, un fármaco que bloquea los receptores opioides en el cerebro; y un grupo con reserpina tratado con el antiinflamatorio común diclofenaco. Este diseño permitió al equipo comparar la radiación con un fármaco estándar y comprobar si los sistemas propios similares a los opioides del organismo contribuían a cualquier alivio del dolor.
Evaluación del dolor y análisis del cerebro
Los investigadores midieron el dolor de dos maneras. En la prueba del latigazo de cola (tail‑flick), la cola de la rata se coloca en agua templada y el tiempo hasta que la mueve refleja la sensibilidad al dolor de los nervios periféricos fuera del cerebro y la médula espinal. En la prueba de clip de Haffner (tail‑clip), se aplica suavemente una pequeña pinza cerca de la base de la cola, y el tiempo antes de que la rata reaccione girando para morder refleja el procesamiento del dolor en la médula espinal y el cerebro. Tras estas pruebas, los científicos recolectaron sangre y tejido cerebral para medir marcadores relacionados con el dolor y el estrés tisular: sustancia P y factor de necrosis tumoral alfa (ambos asociados con dolor e inflamación) en la sangre, y óxido nítrico y malondialdehído (indicadores de estrés oxidativo, o “tipo óxido”) más dopamina (un mensajero implicado en el estado de ánimo y el control del dolor) en el cerebro.
El patrón sorprendente del alivio por radiación
La reserpina aumentó la sensibilidad al dolor de las ratas en ambas pruebas y alteró su química interna: subieron los marcadores de estrés oxidativo y las señales inflamatorias, mientras que la dopamina cerebral descendió. Una única dosis baja de radiación gamma revirtió muchos de estos cambios. Las respuestas al dolor en ambas pruebas se retrasaron, lo que significa que las ratas toleraron más incomodidad antes de reaccionar. Para el dolor transportado por nervios en la cola, el efecto de la radiación fue similar al del diclofenaco. Para el dolor que involucra el cerebro y la médula espinal, la radiación también redujo la sensibilidad, pero este beneficio desapareció en gran medida cuando se administró naloxona previamente. Ese patrón sugiere que la radiación a baja dosis activa, al menos en parte, los propios sistemas analgésicos de tipo opioide del organismo además de calmar nervios sobreactivos.
Menos “tormenta” química, más equilibrio
A nivel químico, la radiación atenuó claramente la “tormenta” interna provocada por la reserpina. Los niveles de óxido nítrico y malondialdehído en el cerebro bajaron hacia valores normales, lo que apunta a una reducción del estrés oxidativo. El contenido de dopamina cerebral, que la reserpina había deprimido, se recuperó tras la irradiación. En el torrente sanguíneo, tanto el mensajero inflamatorio factor de necrosis tumoral alfa como el neuropéptido relacionado con el dolor sustancia P disminuyeron después de la baja dosis. Bloquear los receptores opioides con naloxona no revirtió estos cambios antioxidantes y antiinflamatorios, lo que indica que la calma química inducida por la radiación y sus efectos sobre la señalización relacionada con opioides son al menos en parte independientes. El diclofenaco también mejoró muchas de estas medidas, pero a diferencia de los fármacos estándar, la radiación a baja dosis lo hizo con una sola exposición y sin los riesgos digestivos y cardiovasculares conocidos de los antiinflamatorios a largo plazo.
Qué podría significar esto para la atención del dolor en el futuro
En términos prácticos, el estudio sugiere que una dosis baja y controlada de radiación gamma puede hacer que los nervios sensores del dolor estén menos reactivos, ayudar a restaurar químicos protectores del cerebro y atenuar tanto las señales oxidativas como inflamatorias que contribuyen al dolor crónico. El trabajo se realizó en un solo modelo de rata con una única dosis de radiación y en un único punto temporal corto, por lo que todavía no puede traducirse directamente a pacientes. Aun así, respalda observaciones clínicas de que la radioterapia a baja dosis puede aliviar dolores resistentes en articulaciones y tendones, y apunta a vías biológicas concretas —defensas antioxidantes, control de la inflamación y circuitos neuronales relacionados con opioides— que futuras terapias dirigidas, ya sean basadas en radiación o en fármacos, podrían aprovechar de forma segura para ayudar a personas que viven con dolor crónico.
Cita: Saif-Elnasr, M. Central and peripheral analgesia in irradiated rats: reserpine-induced pain model. Sci Rep 16, 12193 (2026). https://doi.org/10.1038/s41598-026-44637-8
Palabras clave: dolor crónico, radiación a baja dosis, estrés oxidativo, inflamación, vías opioides