Clear Sky Science · zh
COPD 患者远端肺组织中软骨素/真皮素结构的变化
这对 COPD 患者有何意义
慢性阻塞性肺疾病(COPD)通常被描述为气道阻塞和肺泡受损的问题。但在这些熟悉的症状背后,存在一套由糖类和蛋白质构成的隐形支架,它帮助维持肺组织的结构并调控炎症。本研究对人类肺中的这套支架进行了精细分析,显示随着 COPD 进展,其糖链在化学上发生了重构。理解这些细微变化可能为减缓肺损伤(而不仅仅是治疗症状)开辟新的途径。
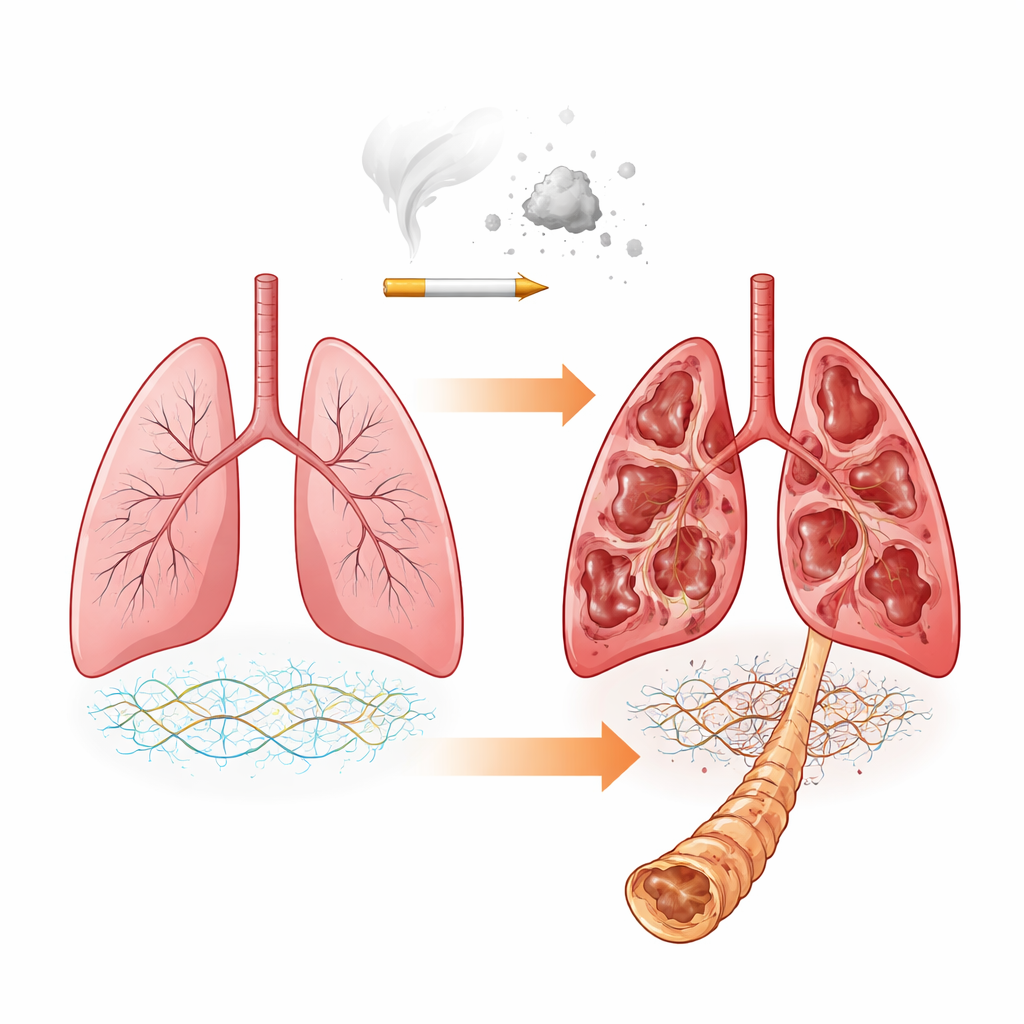
肺部的隐形支持网络
我们的肺由一套复杂的支持网络构建,称为细胞外基质。它由胶原等蛋白质和携带长糖链的蛋白多糖构成,这些长糖链被称为糖胺聚糖(GAGs)。这些 GAGs,包括软骨素硫酸、真皮素硫酸和肝素硫酸,决定了组织的硬度或弹性,并影响其与生长因子及分解基质的酶的相互作用。先前研究表明 COPD 时基质蛋白的整体组成会改变。本研究提出了一个更细致的问题:即使主要的蛋白骨架保持相似,附着的糖链在疾病恶化时是否会改变其成分和化学修饰?
比较健康者、吸烟者与 COPD 患者的肺
研究团队分析了来自非吸烟者、未患 COPD 的吸烟者以及中度和重度 COPD 患者的肺组织。通过敏感的化学方法,他们测量了发生气体交换的肺远端部位中 GAGs 的总量和精细结构,并重新审视了来自类似患者的已有蛋白质和基因活性数据集。尽管在小型蛋白质数据集中核心蛋白多糖本身未显示出大差异,COPD 患者的 GAGs 总量却更高,且在疾病更严重时尤为明显。最丰富的 GAGs 是软骨素硫酸和真皮素硫酸,并且这些在中度 COPD 患者中就已较健康对照升高。
病变肺中糖链的化学修饰
除了总量之外,科学家们还细察了 GAG 链中单个糖基如何被修饰。在重度 COPD 中,肝素硫酸在特定位置显示出更多的硫酸基添加,这种变化会改变其与信号分子的结合方式。更引人注目的是软骨素和真皮素硫酸的变化:携带特定位点(4位)硫酸基的糖残基在 COPD 各阶段更为常见,并且部分这些糖残基被转换为一种略有不同的形式(iduronic acid,艾杜糖醛酸),已知会影响基质与酶和生长因子的相互作用。这些结构特征与多种参与构建和修饰这些链的基因活性上升相吻合,尤其是 CHST11,它有助于在 4 位上加入硫酸基。
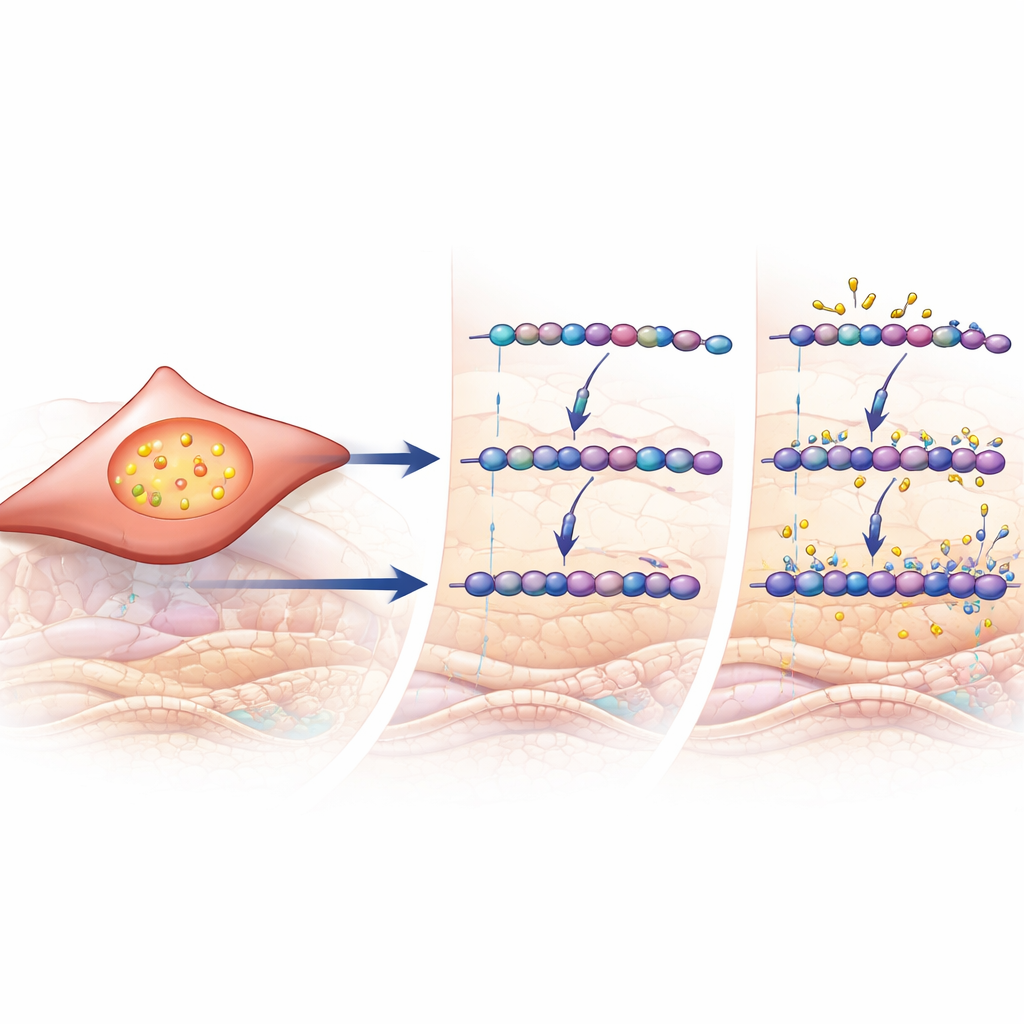
驱动重塑的信号开关
为弄清是什么可能激活这些糖链修饰酶,研究人员转向大规模基因数据和细胞实验。在患者肺样本中,上调基因富集于已知对信号分子 TGF-β 有反应的基因,这是一种在多种组织瘢痕形成和重塑中起关键作用的驱动因子。CHST11 及若干相关酶的表达与计算得出的 TGF-β 活性评分呈一致。在体外培养的人肺成纤维细胞中,直接暴露于 TGF-β 会增加软骨素/真皮素硫酸的产生、提升在患者肺中观察到的特定 4-硫酸化糖残基,并提高 CHST11 水平。这些发现将一个已知的重塑信号与 COPD 肺中观察到的 GAG 链精确化学重塑联系了起来。
这对未来治疗的意义
对于 COPD 患者而言,这些结果表明肺部的支架不仅仅是在瓦解;它正以疾病分期特异的方式被化学重编程。软骨素/真皮素和肝素硫酸链中新增的硫酸基和改变的糖型很可能会改变基质与酶、生长因子及炎性分子的结合方式,可能促成持续的组织损伤和瘢痕形成。由于这些变化与特定酶(如 CHST11)和 TGF-β 信号通路有关,它们指向了新的、更精确的药物靶点:未来疗法或许可以不再是广泛抑制炎症,而是温和地重新平衡肺糖链的合成与修饰,以稳定组织并减缓 COPD 的进展。
引用: Alsafadi, H.N., Nybom, A., Wagner, D. et al. Change in the chondroitin/dermatan structure in distal lung tissue from COPD patients. Sci Rep 16, 9721 (2026). https://doi.org/10.1038/s41598-026-44120-4
关键词: COPD, 肺基质, 糖胺聚糖, 细胞外基质重塑, TGF-beta 信号