Clear Sky Science · he
שינוי במבנה הדנדרואיטין/כונדרואיטין ברקמת הריאוּת המרוחקת ממטופלי COPD
מדוע זה חשוב עבור אנשים עם COPD
מחלת ריאה חסימתית כרונית (COPD) מתוארת בדרך כלל כבעיה של דרכי נשימה חסומות ונאדיות נפגעות. אבל מאחורי התסמינים המוכרים הללו קיימת מערכת תמיכה נסתרת של סוכרים וחלבונים שמחזיקה את רקמת הריאה ומווסתת דלקת. מחקר זה בוחן במפורט את המבנה התומך הזה בריאות אנושיות ומראה כי שרשראות הסוכר שבו עוברות שינויים כימיים ככל ש‑COPD מתקדם. הבנת השינויים העדינים האלה עשויה לפתוח דרכים חדשות להאטת הפגיעה בריאות במקום רק לטפל בתסמינים.
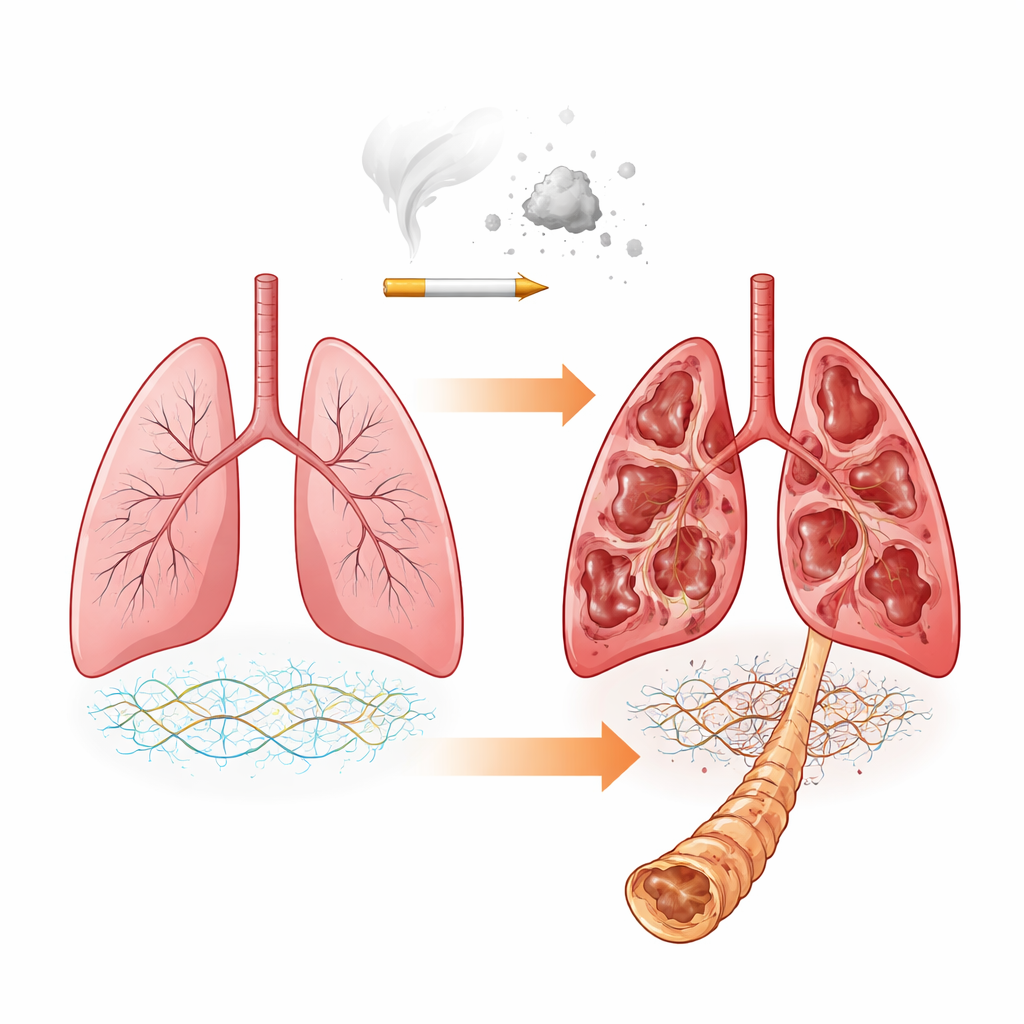
רשת התמיכה הנסתרת של הריאה
הריאות שלנו בנויות סביב רשת תמיכה מסועפת הנקראת מטריקס חוץ‑תאי. היא מורכבת מחלבונים, כמו קולגן, וממולקולות מיוחדות שנקראות פרוטאוגליקאנים הנושאים שרשראות סוכר ארוכות הידועות כגליקוזאמינוגליקנים (GAGs). GAGs אלה, כולל כונדרואיטין סולפט, דרמטאן סולפט והפאראן/הפאראן‑סולפט (Heparan sulfate), עוזרות לקבוע עד כמה הרקמה קשיחה או אלסטית וכיצד היא מתקשרת עם גורמי גדילה ועם אנזימים המפרקים את המטריקס. ב‑COPD מחקרים קודמים הראו שהתמהיל הכללי של חלבוני המטריקס משתנה. כאן החוקרים שאלו שאלה מפורטת יותר: גם אם שלד החלבונים הראשי נשאר דומה, האם שרשראות הסוכר המותקנות עליהן משנות את הרכבן וקישוטיהן הכימיים ככל שהמחלה מחמירה?
השוואה בין ריאות בריאות, מעשנים וחולי COPD
הצוות ניתח רקמות ריאה שנלקחו מאנשים שלא עישנו, מעשנים ללא COPD, ומטופלים עם COPD בדרגה מתונה וחמורה. באמצעות שיטות כימיות רגישות מדדו את הכמות הכוללת והמבנה העדין של ה‑GAGs בחלקים המרוחקים של הריאות, שם מתבצע חילוף הגזים. הם גם בחנו מחדש מאגרי נתונים של חלבונים וביטוי גנים מאותו סוג של מטופלים. בעוד שחלבוני הפרוטאוגליקאן הליבה עצמם לא הראו הבדלים גדולים בנתוני החלבון המצומצמים, הכמות הכוללת של GAGs הייתה גבוהה יותר ב‑COPD, ובעיקר במחלות מתקדמות יותר. ה‑GAGs השכיחים ביותר היו כונדרואיטין ודרמטאן סולפט, והם כבר היו מוגברים בחולים עם COPD מתון בהשוואה לבקרות בריאות.
התאמות כימיות לשרשראות הסוכר בריאות חולות
מעבר לרמות הכוללות, המדענים בחנו כיצד יחידות הסוכר הבודדות בתוך שרשראות ה‑GAG עברו שינויים. ב‑COPD חמור הראו פאראן/הפאראן‑סולפט (heparan sulfate) הוספת קבוצות סולפט במיקומים ספציפיים, שינוי שיכול לשנות את הקשירה שלו למולקולות איתות. עוד יותר בולטות היו השינויים בכונדרואיטין ודרמטאן סולפט. מולקולות סוכר הנושאות סוג מסוים של קבוצה סולפטית במיקום 4 הפכו לשכיחות יותר בכל שלבי ה‑COPD, וחלק מהסוכרים הללו הומרו לצורה מעט שונה (חומצה איאדורונית) הידועה כהשפעה על האינטראקציה של המטריקס עם אנזימים וגורמי גדילה. טביעות האצבע המבניות האלה תאמו עלייה בפעילות של מספר גנים הבונים ומשנים שרשראות אלו, ובעיקר CHST11, המסייע למקם את קבוצת ה‑4‑סולפט.
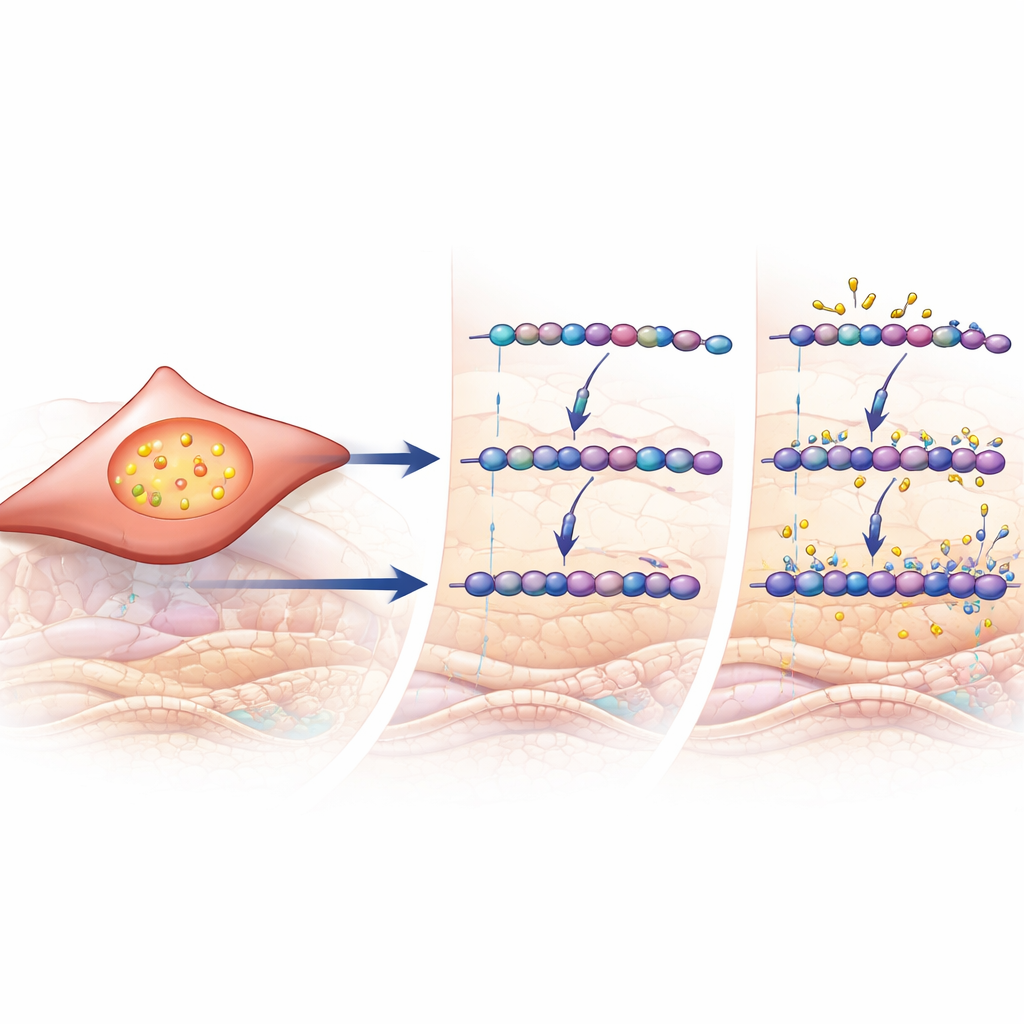
מתג איתות שמניע שחזור
כדי להבין מה עלול להפעיל את האנזימים המודיפיקטים של הסוכרים, פנו החוקרים לנתוני גנים בקנה מידה גדול ולניסויים על תאים. במדגמי ריאות של מטופלים, הגנים שעודדו בביטוי ב‑COPD היו מועשרים באלה הידועים כמשתתפים בתגובה לאות ה‑TGF‑β, מקדם מרכזי של צלקת ושחזור ברקמות רבות. הביטוי של CHST11 וכמה אנזימים קשורים עקב אחרי ניקוד פעילות מחושב של TGF‑β. בתאי פיברובלסט של ריאה אנושיים בתרבית, חשיפה ישירה ל‑TGF‑β הגבירה את ייצור כונדרואיטין/דרמטאן סולפט, הגבירה את הסוכרים המסולפטים ב‑4 הספציפיים שנראו בריאות המטופלים, והעלתה את רמות CHST11. יחד, הממצאים מקשרים אותיות איתות מוכרות לשינוי הכימי המדויק של שרשראות ה‑GAG הנצפה בריאות חולי COPD.
מה משמעות הדבר לטיפולים עתידיים
עבור אנשים החיים עם COPD, התוצאות האלה מצביעות על כך שהשלד של הריאה לא רק מתפרק; הוא עובר כוונון כימי המותאם לשלב המחלה. קבוצות הסולפט שהתוספו וצורות הסוכר המשתנות בשרשראות כונדרואיטין/דרמטאן והפאראן‑סולפט צפויות לשנות כיצד המטריקס נקשר לאנזימים, לגורמי גדילה ולמולקולות דלקת, ובכך עשויות להזין את הנזק המתמשך והצלקת. מכיוון ששינויים אלה מקושרים לאנזימים ספציפיים כגון CHST11 ולאותות TGF‑β, הם מצביעים על מטרות תרופתיות מדויקות יותר: במקום לחסום דלקת באופן רחב, טיפולים עתידיים עשויים לשאוף לאזן בעדינות את בניית ועריכת שרשראות הסוכר בריאה, במטרה לייצב את הרקמה ולהאט את התקדמות ה‑COPD.
ציטוט: Alsafadi, H.N., Nybom, A., Wagner, D. et al. Change in the chondroitin/dermatan structure in distal lung tissue from COPD patients. Sci Rep 16, 9721 (2026). https://doi.org/10.1038/s41598-026-44120-4
מילות מפתח: COPD, מטריקס ריאתי, גליקוזאמינוגליקנים, שחזור חוץ‑תאי, אותות TGF‑beta