Clear Sky Science · es
Cambio en la estructura de condroitina/dermatan en tejido pulmonar distal de pacientes con EPOC
Por qué importa a las personas con EPOC
La enfermedad pulmonar obstructiva crónica (EPOC) suele describirse como un problema de vías aéreas obstruidas y alvéolos dañados. Pero tras esos síntomas familiares existe un andamiaje oculto de azúcares y proteínas que ayuda a mantener la integridad del tejido pulmonar y a regular la inflamación. Este estudio examina ese armazón en pulmones humanos y muestra que sus cadenas de azúcares se reconfiguran químicamente a medida que la EPOC progresa. Comprender estos cambios sutiles podría abrir nuevas vías para frenar el daño en los pulmones en lugar de limitarse a tratar los síntomas.
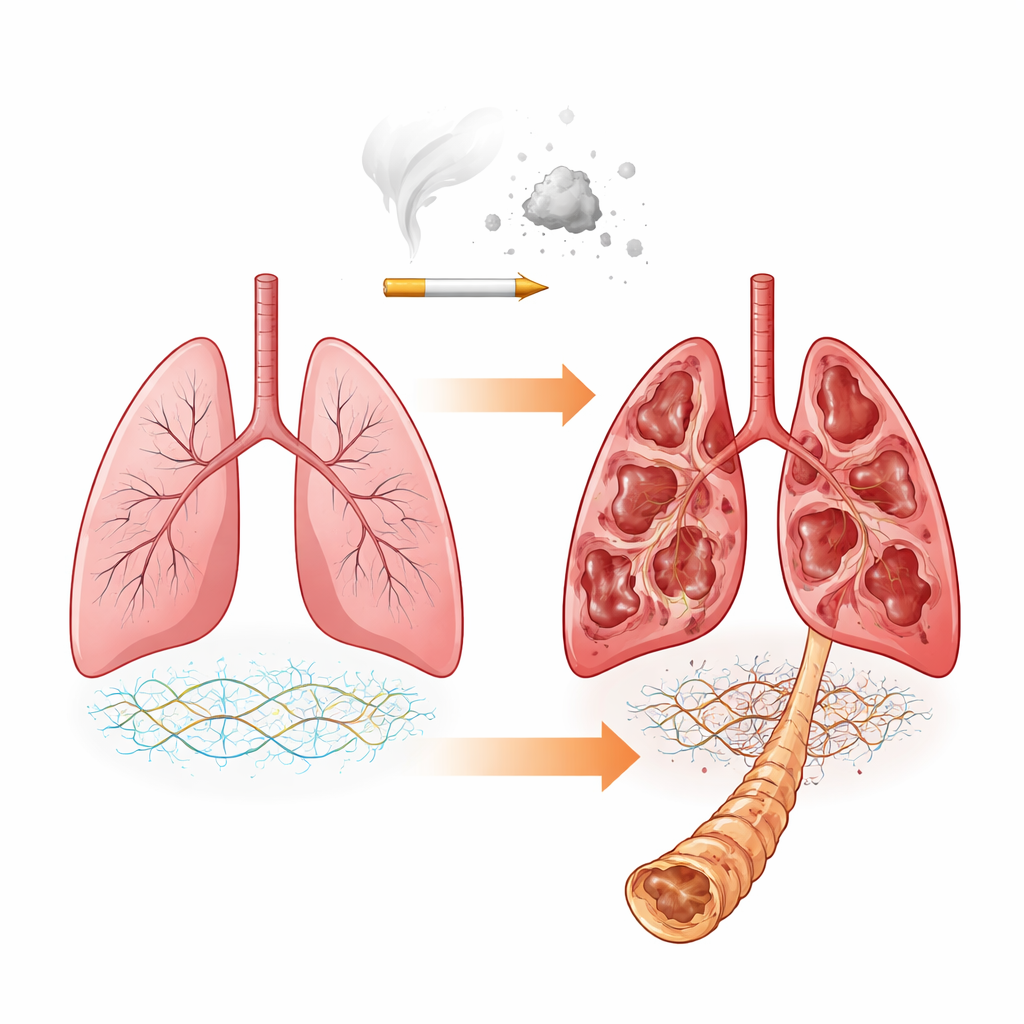
La red de soporte oculta del pulmón
Nuestros pulmones se organizan alrededor de una compleja red de soporte llamada matriz extracelular. Está formada por proteínas, como el colágeno, y por moléculas especiales llamadas proteoglicanos que portan largas cadenas de azúcares conocidas como glicosaminoglicanos (GAG). Estos GAG, entre ellos condroitín sulfato, dermatán sulfato y heparán sulfato, contribuyen a determinar cuán rígido o elástico es el tejido y cómo interactúa con factores de crecimiento y enzimas que degradan la matriz. En la EPOC, trabajos previos han mostrado que la mezcla global de proteínas de la matriz cambia. Aquí, los investigadores se plantearon una pregunta más detallada: aunque los esqueletos proteicos principales permanezcan similares, ¿cambian las cadenas de azúcares adjuntas en su composición y decoración química a medida que avanza la enfermedad?
Comparación de pulmones sanos, de fumadores y con EPOC
El equipo analizó tejido pulmonar tomado de no fumadores, fumadores sin EPOC y pacientes con EPOC moderada y severa. Usando métodos químicos sensibles, midieron la cantidad total y la estructura fina de los GAG en las zonas distales del pulmón, donde ocurre el intercambio gaseoso. También reexaminaron conjuntos de datos existentes de proteínas y actividad génica de pacientes similares. Si bien las proteínas núcleo de los proteoglicanos no mostraron grandes diferencias en el conjunto de datos proteico reducido, la cantidad total de GAG fue mayor en la EPOC, especialmente en fases más avanzadas de la enfermedad. Los GAG más abundantes fueron los condroitín y dermatán sulfatos, y estos ya estaban incrementados en pacientes con EPOC moderada en comparación con controles sanos.
Ajustes químicos en las cadenas de azúcares de pulmones enfermos
Más allá de los niveles totales, los científicos se centraron en cómo se modificaban las unidades individuales de azúcar dentro de las cadenas de GAG. En la EPOC severa, el heparán sulfato mostró más grupos sulfato añadidos en posiciones específicas, un cambio que puede alterar su unión a moléculas de señalización. Aún más llamativos fueron los cambios en condroitín y dermatán sulfato. Las unidades azucaradas que llevan un tipo particular de sulfato en la posición 4 se volvieron más frecuentes a lo largo de las etapas de la EPOC, y una fracción de estas azúcares se convirtió en una forma ligeramente distinta (ácido idurónico) conocida por influir en cómo la matriz interactúa con enzimas y factores de crecimiento. Estas huellas estructurales coincidieron con un aumento en la actividad de varios genes que construyen y modifican estas cadenas, de manera más notable CHST11, que participa en la colocación del grupo 4-sulfato.
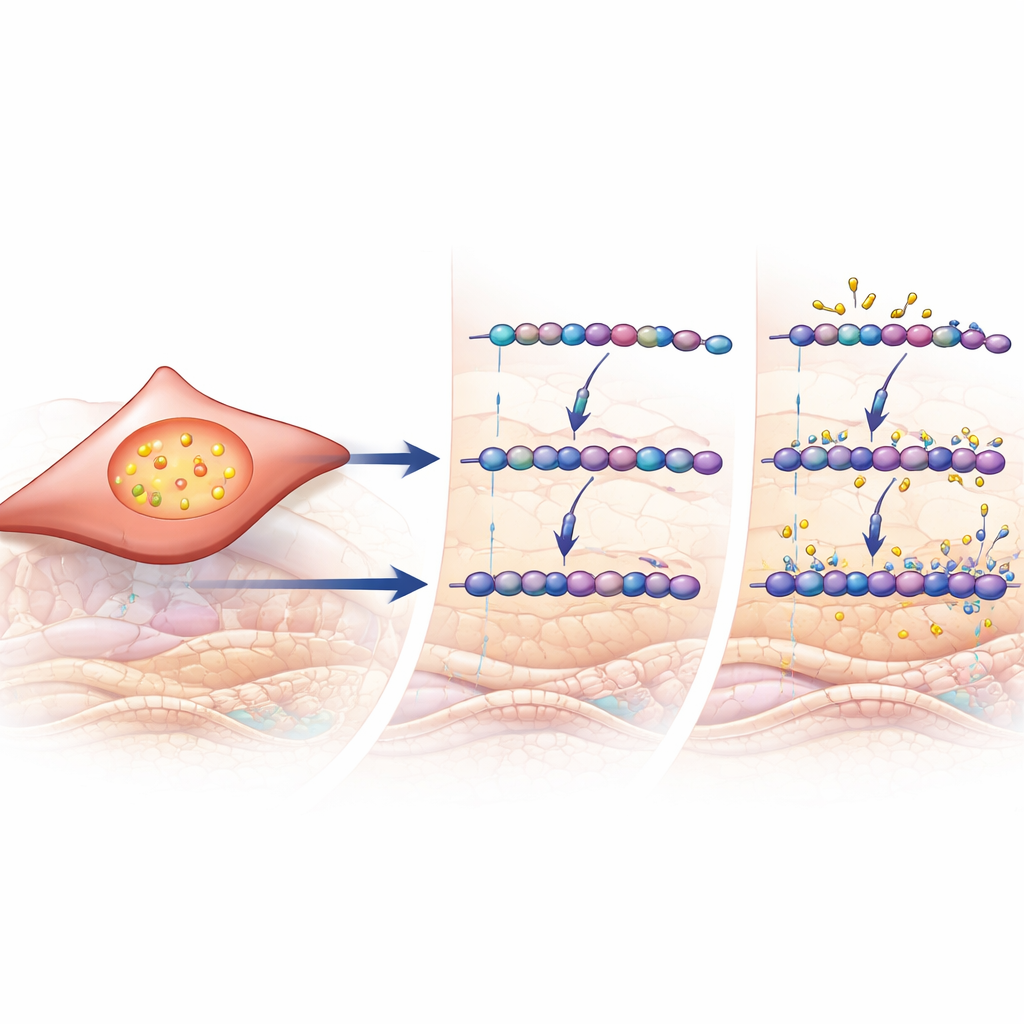
Un interruptor de señalización que impulsa el remodelado
Para averiguar qué podría activar estas enzimas modificadoras de azúcares, los investigadores recurrieron a datos génicos a gran escala y a experimentos celulares. En muestras pulmonares de pacientes, los genes elevados en EPOC estaban enriquecidos por aquellos que responden a la molécula de señalización TGF-β, un impulsor clave de la cicatrización y el remodelado en muchos tejidos. La expresión de CHST11 y de varias enzimas relacionadas se correlacionó con un puntaje computado de actividad de TGF-β. En fibroblastos pulmonares humanos cultivados, la exposición directa a TGF-β aumentó la producción de condroitín/dermatán sulfato, potenció las unidades 4-sulfatadas específicas observadas en pulmones de pacientes y elevó los niveles de CHST11. En conjunto, estos hallazgos conectan una señal de remodelado bien conocida con el reconfigurado químico preciso de las cadenas de GAG observado en pulmones con EPOC.
Qué significa esto para futuros tratamientos
Para las personas que viven con EPOC, estos resultados sugieren que el andamiaje pulmonar no solo se está deteriorando; se está reconfigurando químicamente de forma dependiente del estadio de la enfermedad. Los grupos sulfato añadidos y las formas azucaradas alteradas en las cadenas de condroitín/dermatán y heparán sulfato probablemente cambien cómo la matriz se une a enzimas, factores de crecimiento y moléculas inflamatorias, alimentando potencialmente el daño tisular y la formación de cicatriz continuos. Dado que estos cambios se vinculan a enzimas específicas como CHST11 y a la señalización por TGF-β, apuntan a dianas farmacológicas nuevas y más precisas: en lugar de bloquear la inflamación de forma amplia, las terapias futuras podrían procurar reequilibrar con delicadeza cómo se ensamblan y modifican las cadenas de azúcares pulmonares, con el objetivo de estabilizar el tejido y frenar la progresión de la EPOC.
Cita: Alsafadi, H.N., Nybom, A., Wagner, D. et al. Change in the chondroitin/dermatan structure in distal lung tissue from COPD patients. Sci Rep 16, 9721 (2026). https://doi.org/10.1038/s41598-026-44120-4
Palabras clave: EPOC, matriz pulmonar, glicosaminoglicanos, remodelado extracelular, señalización TGF-beta