Clear Sky Science · ar
تغير في تركيب الكوندرويتين/الدرماتان في أنسجة الرئة البعيدة لدى مرضى داء الانسداد الرئوي المزمن
لماذا يهم هذا الأشخاص المصابين بداء الانسداد الرئوي المزمن
عادة ما يُوصف داء الانسداد الرئوي المزمن بأنه مشكلة انسداد المجاري الهوائية وتلف الحويصلات الهوائية. لكن وراء تلك الأعراض المألوفة توجد بنية داعمة مخفية من السكريات والبروتينات تساعد في الحفاظ على نسيج الرئة والتحكم في الالتهاب. تدرس هذه الدراسة تلك البنية الداعمة في رئات البشر عن قرب وتظهر أن سلاسل السكّر فيها تُعاد تشكيلها كيميائياً مع تقدم المرض. قد يفتح فهم هذه التغيرات الطفيفة سبلًا جديدة لإبطاء تلف الرئتين بدل الاقتصار على علاج الأعراض.
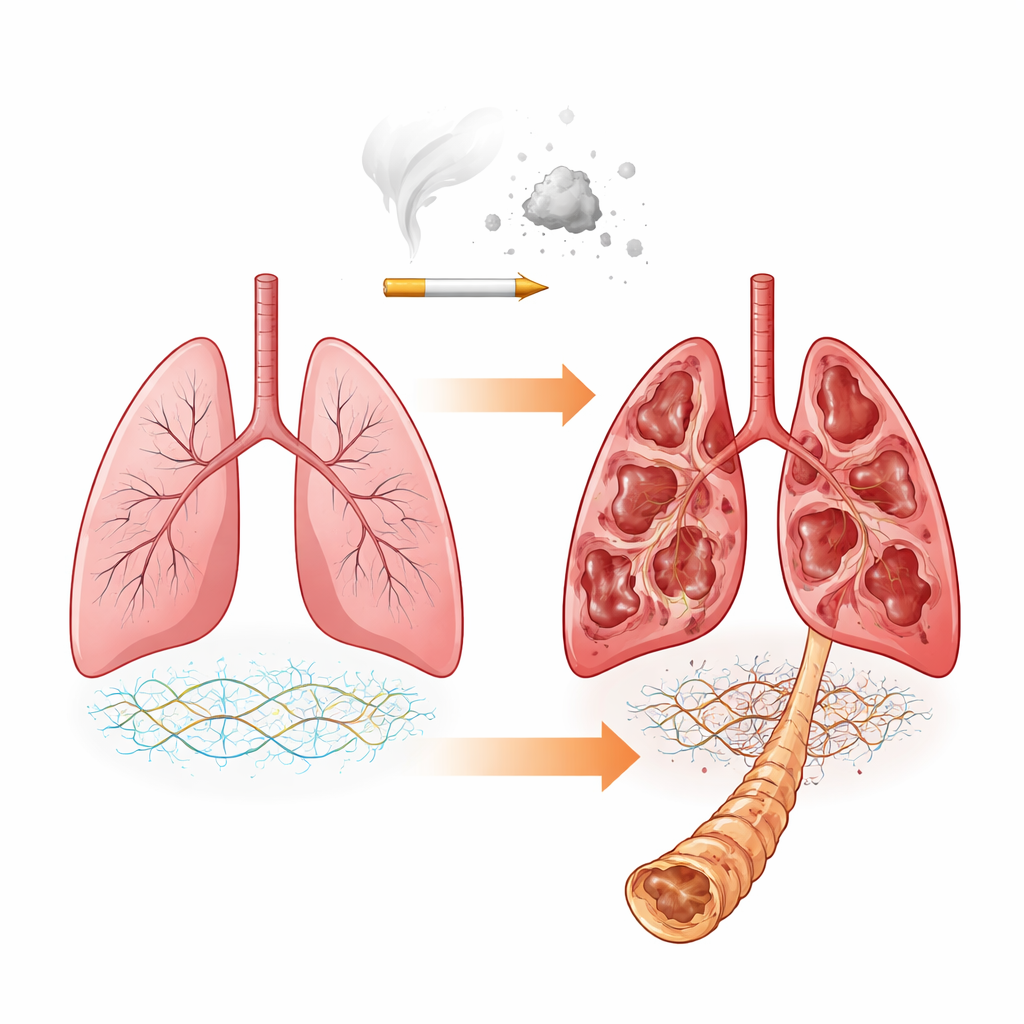
الشبكة الداعمة الخفية للرئة
تُبنى رئاتنا حول شبكة دعم معقّدة تسمى المصفوفة خارج الخلية. تتكوّن من بروتينات مثل الكولاجين وجزيئات خاصة تُدعى البروتيوغليكانات التي تحمل سلاسل سكّر طويلة معروفة بالغليكوزأمينوغليكانات (GAGs). تساعد هذه الغليكوزأمينوغليكانات، بما في ذلك كوندرويتين سلفات، درماتان سلفات، وهباران سلفات، على تحديد صلابة أو مرونة النسيج وكيفية تفاعله مع عوامل النمو والإنزيمات التي تهدم المصفوفة. أظهرت أعمال سابقة أن التكوين العام لبروتينات المصفوفة يتغير في داء الانسداد الرئوي المزمن. هنا، طرح الباحثون سؤالاً أكثر تفصيلاً: حتى لو بقيت الهياكل البروتينية الأساسية مماثلة، هل تتغيّر سلاسل السكّر المرتبطة بها في التركيب والزخرفة الكيميائية مع تفاقم المرض؟
مقارنة بين رئات الأصحاء والمدخنين ومرضى داء الانسداد الرئوي المزمن
حلّل الفريق أنسجة رئوية مأخوذة من غير المدخنين، ومدخنين بدون داء الانسداد الرئوي المزمن، ومرضى يعانون داء الانسداد الرئوي المتوسط والشديد. باستخدام طرق كيميائية حسّاسة، قاسوا الكمية الكلية والبنية الدقيقة للغليكوزأمينوغليكانات في أجزاء الرئة البعيدة حيث يحدث تبادل الغازات. أعادوا أيضاً فحص مجموعات بيانات بروتينية وجينية سابقة من مرضى مماثلين. بينما لم تُظهر بروتينات البروتيوغليكان الأساسية فروقاً كبيرة في مجموعة البروتينات الصغيرة، كانت الكمية الكلية من الغليكوزأمينوغليكانات أعلى في داء الانسداد الرئوي المزمن، خصوصاً في المراحل المتقدمة من المرض. أكثر الغليكوزأمينوغليكانات وفرة كانت كوندرويتين ودرماتان سلفات، وكانت مرتفعة بالفعل لدى مرضى داء الانسداد الرئوي المتوسط مقارنة بالمجموعة الضابطة السليمة.
تعديلات كيميائية على سلاسل السكّر في الرئات المريضة
بعيداً عن المستويات الكلية، ركز العلماء على كيفية تعديل وحدات السكّر الفردية داخل سلاسل الغليكوزأمينوغليكانات. في داء الانسداد الرئوي الشديد، أظهر الهباران سلفات إضافة مجموعات سلفات عند مواقع محددة، وهو تغيير يمكن أن يغيّر كيفية ارتباطه بجزيئات الإشارة. كانت التغيرات الأكثر بروزاً في كوندرويتين ودرماتان سلفات. ازدادت شيوع وحدات السكر التي تحمل نوعاً محدداً من مجموعة السلفات في الموقع 4 عبر مراحل داء الانسداد الرئوي، وتحولت نسبة من هذه الوحدات إلى شكل مختلف قليلاً (حمض الإيدورونيك) المعروف بتأثيره على تفاعل المصفوفة مع الإنزيمات وعوامل النمو. طابعت هذه البصمات التركيبية بارتفاع نشاط عدة جينات تبني وتعدّل هذه السلاسل، لا سيما CHST11 الذي يساعد في وضع مجموعة السلفات في الموقع 4.
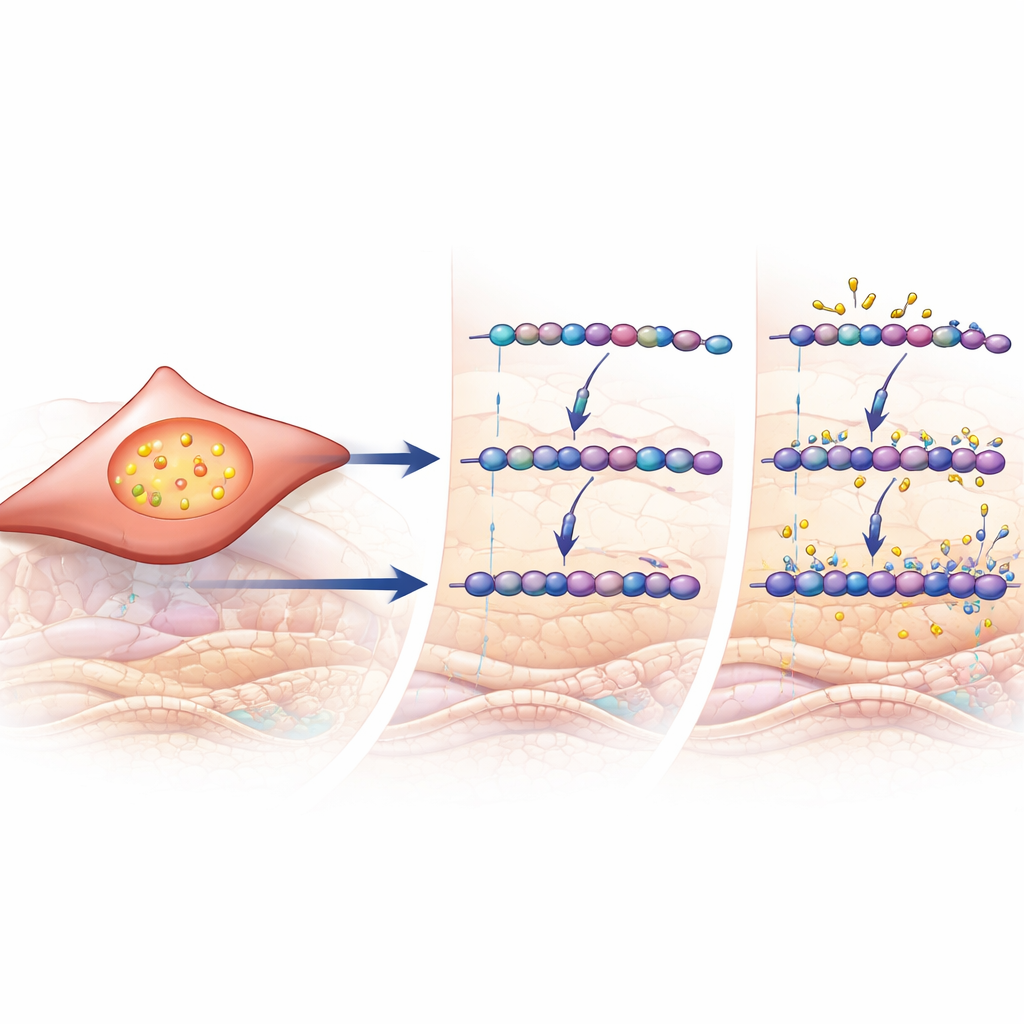
مفتاح إشاري يدفع عملية إعادة التشكيل
لاكتشاف ما قد يُفعّل هذه الإنزيمات المعدِّلة للسكّر، لجأ الباحثون إلى بيانات جينية واسعة ونماذج خلوية. في عينات رئوية من المرضى، كانت الجينات المرتفعة في داء الانسداد الرئوي غنية بتلك المعروفة بالاستجابة لجزيء الإشارة TGF-β، وهو محرك رئيسي للتندّب وإعادة التشكيل في العديد من الأنسجة. تبع تعبير CHST11 وعدة إنزيمات ذات صلة درجة نشاط محسوبة لـTGF-β. في خلايا الأرومة الليفية الرئوية البشرية المزروعة، زاد التعرض المباشر لـTGF-β إنتاج كوندرويتين/درماتان سلفات، وعزّز الوحدات السكرية 4-المكبَّرة المتواجدة في رئات المرضى، ورفَع مستويات CHST11. تربط هذه النتائج معاً إشارة إعادة التشكيل المعروفة بإعادة التشكيل الكيميائي الدقيق لسلاسل الغليكوزأمينوغليكانات التي لوحظت في رئات داء الانسداد الرئوي المزمن.
ماذا يعني هذا للعلاجات المستقبلية
بالنسبة للأشخاص الذين يعيشون مع داء الانسداد الرئوي المزمن، تشير هذه النتائج إلى أن بنية رئة الدعم ليست مجرد تفكك؛ بل تُعاد توصيلها كيميائياً بطريقة تعتمد على مرحلة المرض. من المرجح أن المجموعات السلفات المضافة والأشكال السكرية المعدَّلة في سلاسل كوندرويتين/درماتان وهباران سلفات تغيّر كيفية ارتباط المصفوفة بالإنزيمات وعوامل النمو والجزيئات الالتهابية، مما قد يساهم في استمرار تلف النسيج والتندّب. وبما أن هذه التغيرات مرتبطة بإنزيمات محددة مثل CHST11 وبإشارة TGF-β، فإنها تشير إلى أهداف دوائية جديدة وأكثر دقة: بدلاً من حجب الالتهاب بشكل واسع، قد تهدف العلاجات المستقبلية إلى إعادة توازن بناء وتعديل سلاسل السكّر في الرئة بلطف، بهدف استقرار النسيج وإبطاء تقدم داء الانسداد الرئوي المزمن.
الاستشهاد: Alsafadi, H.N., Nybom, A., Wagner, D. et al. Change in the chondroitin/dermatan structure in distal lung tissue from COPD patients. Sci Rep 16, 9721 (2026). https://doi.org/10.1038/s41598-026-44120-4
الكلمات المفتاحية: داء الانسداد الرئوي المزمن, مصفوفة الرئة, غليكوزأمينوغليكانات, إعادة تشكيل خارج الخلية, إشارات TGF-beta