Clear Sky Science · pt
Alteração na estrutura de condroitina/dermatan no tecido pulmonar distal de pacientes com DPOC
Por que isso importa para pessoas com DPOC
A doença pulmonar obstrutiva crônica (DPOC) costuma ser descrita como um problema de vias aéreas bloqueadas e alvéolos danificados. Mas por trás desses sintomas familiares existe um andaime oculto de açúcares e proteínas que ajuda a manter o tecido pulmonar unido e a controlar a inflamação. Este estudo examina de perto esse andaime em pulmões humanos e mostra que suas cadeias de açúcares são quimicamente reconfiguradas à medida que a DPOC progride. Compreender essas mudanças sutis pode abrir novas maneiras de frear o dano pulmonar, em vez de apenas tratar os sintomas.
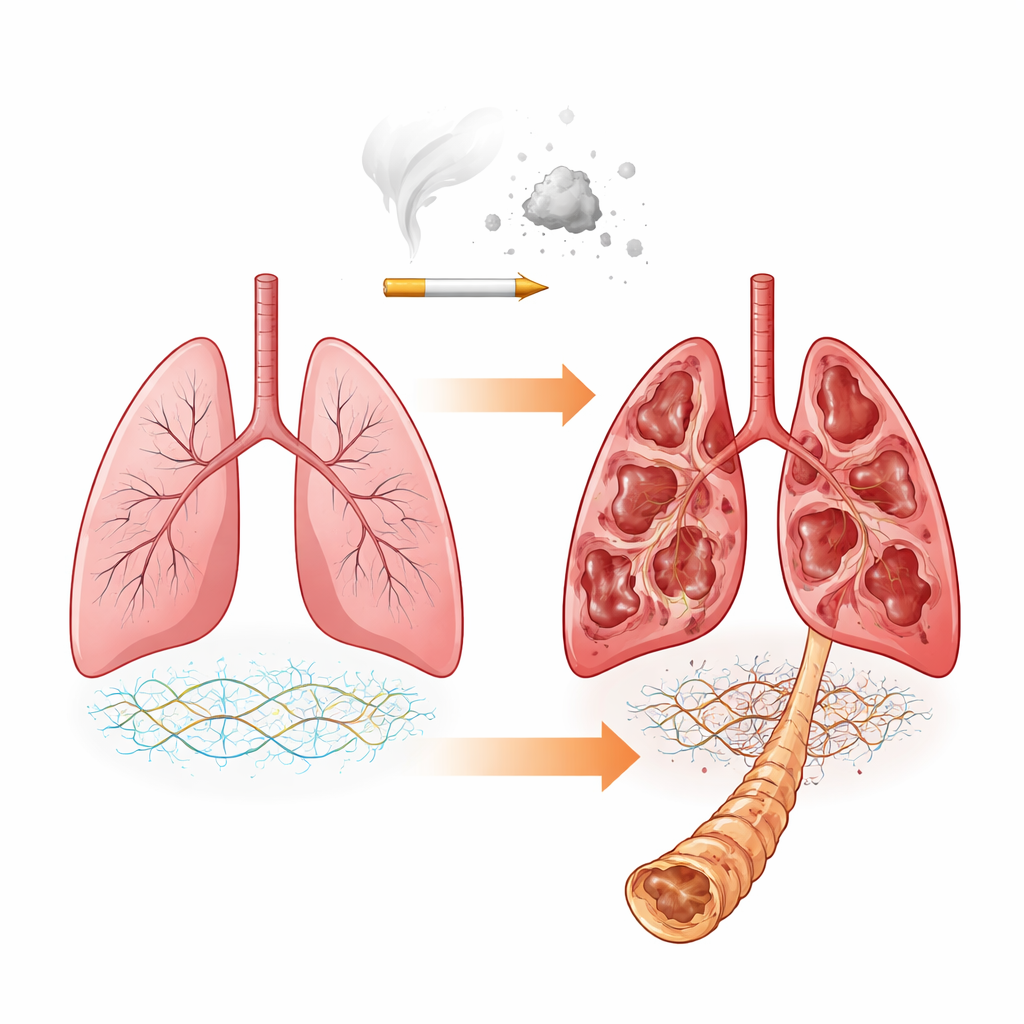
A rede de suporte oculta do pulmão
Nossos pulmões são construídos em torno de uma rede de suporte intrincada chamada matriz extracelular. Ela é composta por proteínas, como o colágeno, e por moléculas especiais chamadas proteoglicanos, que carregam longas cadeias de açúcares conhecidas como glicosaminoglicanos (GAGs). Esses GAGs, incluindo condroitina sulfato, dermatan sulfato e heparan sulfato, ajudam a determinar quão rígido ou elástico o tecido é e como ele interage com fatores de crescimento e enzimas que degradam a matriz. Na DPOC, trabalhos anteriores mostraram que a mistura geral de proteínas da matriz muda. Aqui, os pesquisadores fizeram uma pergunta mais detalhada: mesmo que os esqueletos proteicos principais permaneçam semelhantes, as cadeias de açúcares anexadas mudam sua composição e decorações químicas à medida que a doença piora?
Comparando pulmões saudáveis, de fumantes e com DPOC
A equipe analisou tecido pulmonar retirado de não fumantes, fumantes sem DPOC e pacientes com DPOC moderada e grave. Usando métodos químicos sensíveis, mediram a quantidade total e a estrutura fina dos GAGs nas partes distais dos pulmões, onde ocorre a troca gasosa. Eles também reanalisaram conjuntos de dados existentes de proteínas e atividade gênica de pacientes semelhantes. Embora as proteínas proteoglicanas centrais em si não tenham mostrado grandes diferenças no conjunto proteico reduzido, a quantidade total de GAGs foi maior na DPOC, especialmente nas formas mais avançadas da doença. Os GAGs mais abundantes foram condroitina e dermatan sulfatos, e estes já estavam elevados em pacientes com DPOC moderada em comparação com controles saudáveis.
Ajustes químicos nas cadeias de açúcar em pulmões doentes
Indo além dos níveis totais, os cientistas aprofundaram-se em como os blocos de construção individuais de açúcar dentro das cadeias de GAG foram modificados. Na DPOC grave, o heparan sulfato mostrou mais grupos sulfato adicionados em posições específicas, uma mudança que pode alterar como ele se liga a moléculas de sinalização. Ainda mais marcantes foram as alterações na condroitina e no dermatan sulfato. Açúcares carregando um tipo particular de grupo sulfato na posição 4 tornaram-se mais comuns nos estágios da DPOC, e uma fração desses açúcares foi convertida em uma forma ligeiramente diferente (ácido idurônico) conhecida por influenciar como a matriz interage com enzimas e fatores de crescimento. Essas impressões estruturais corresponderam a um aumento na atividade de vários genes que sintetizam e modificam essas cadeias, notadamente CHST11, que ajuda a colocar o grupo 4-sulfato.
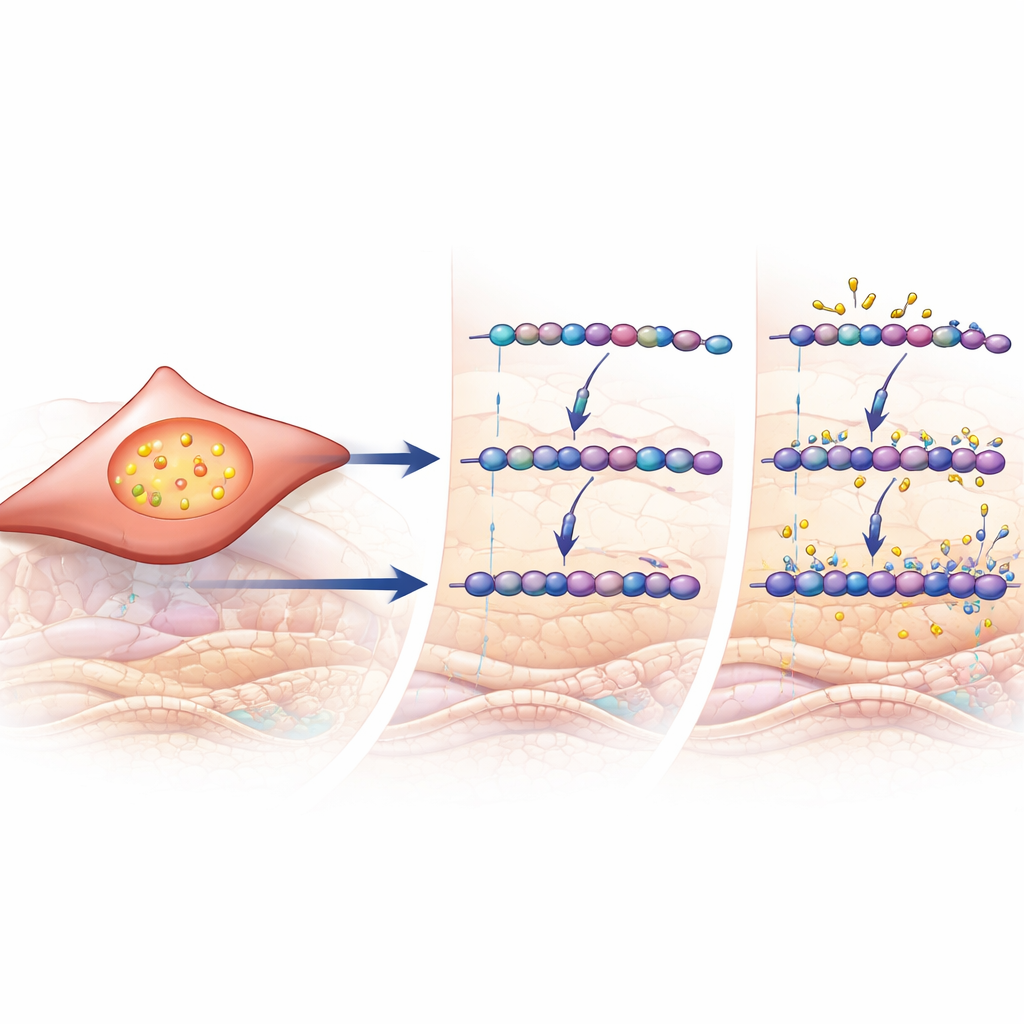
Um interruptor de sinalização que dirige o remodelamento
Para descobrir o que poderia estar ativando essas enzimas modificadoras de açúcares, os pesquisadores recorreram a grandes conjuntos de dados genômicos e a experimentos celulares. Nas amostras pulmonares dos pacientes, os genes sobressalentes na DPOC foram enriquecidos por aqueles conhecidos por responder à molécula de sinalização TGF-β, um motor-chave da cicatrização e do remodelamento em muitos tecidos. A expressão de CHST11 e de várias enzimas relacionadas acompanhou um escore computacional de atividade de TGF-β. Em fibroblastos pulmonares humanos cultivados, a exposição direta ao TGF-β aumentou a produção de condroitina/dermatan sulfato, elevou os açúcares 4-sulfatados específicos observados nos pulmões dos pacientes e aumentou os níveis de CHST11. Em conjunto, esses achados conectam um sinal de remodelamento bem conhecido ao remodelamento químico preciso das cadeias de GAG observado em pulmões com DPOC.
O que isso significa para tratamentos futuros
Para pessoas vivendo com DPOC, esses resultados sugerem que o andaime pulmonar não está apenas se degradando; ele está sendo quimicamente reprogramado de maneira dependente do estágio da doença. Os grupamentos sulfato adicionados e as formas de açúcar alteradas nas cadeias de condroitina/dermatan e heparan sulfato provavelmente mudam como a matriz se liga a enzimas, fatores de crescimento e moléculas inflamatórias, potencialmente alimentando o dano tecidual e a fibrose em curso. Como essas alterações estão ligadas a enzimas específicas, como CHST11, e à sinalização TGF-β, elas apontam para novos alvos farmacológicos mais precisos: em vez de bloquear amplamente a inflamação, terapias futuras poderiam visar reequilibrar de forma delicada como as cadeias de açúcar do pulmão são construídas e modificadas, com o objetivo de estabilizar o tecido e retardar a progressão da DPOC.
Citação: Alsafadi, H.N., Nybom, A., Wagner, D. et al. Change in the chondroitin/dermatan structure in distal lung tissue from COPD patients. Sci Rep 16, 9721 (2026). https://doi.org/10.1038/s41598-026-44120-4
Palavras-chave: DPOC, matriz pulmonar, glicosaminoglicanos, remodelamento extracellular, sinalização TGF-beta