Clear Sky Science · nl
Verandering in de chondroïtine/dermatan-structuur in distaal longweefsel van COPD-patiënten
Waarom dit belangrijk is voor mensen met COPD
Chronische obstructieve longziekte (COPD) wordt meestal beschreven als een probleem van geblokkeerde luchtwegen en beschadigde longblaasjes. Achter die bekende symptomen gaat echter een verborgen geraamte van suikers en eiwitten schuil dat longweefsel bij elkaar houdt en ontstekingsreacties reguleert. Deze studie bekijkt dat geraamte in menselijke longen nauwkeurig en toont aan dat de suikerketens chemisch worden herschikt naarmate COPD vordert. Inzicht in deze subtiele veranderingen kan nieuwe wegen openen om schade in de longen te vertragen in plaats van alleen de symptomen te behandelen.
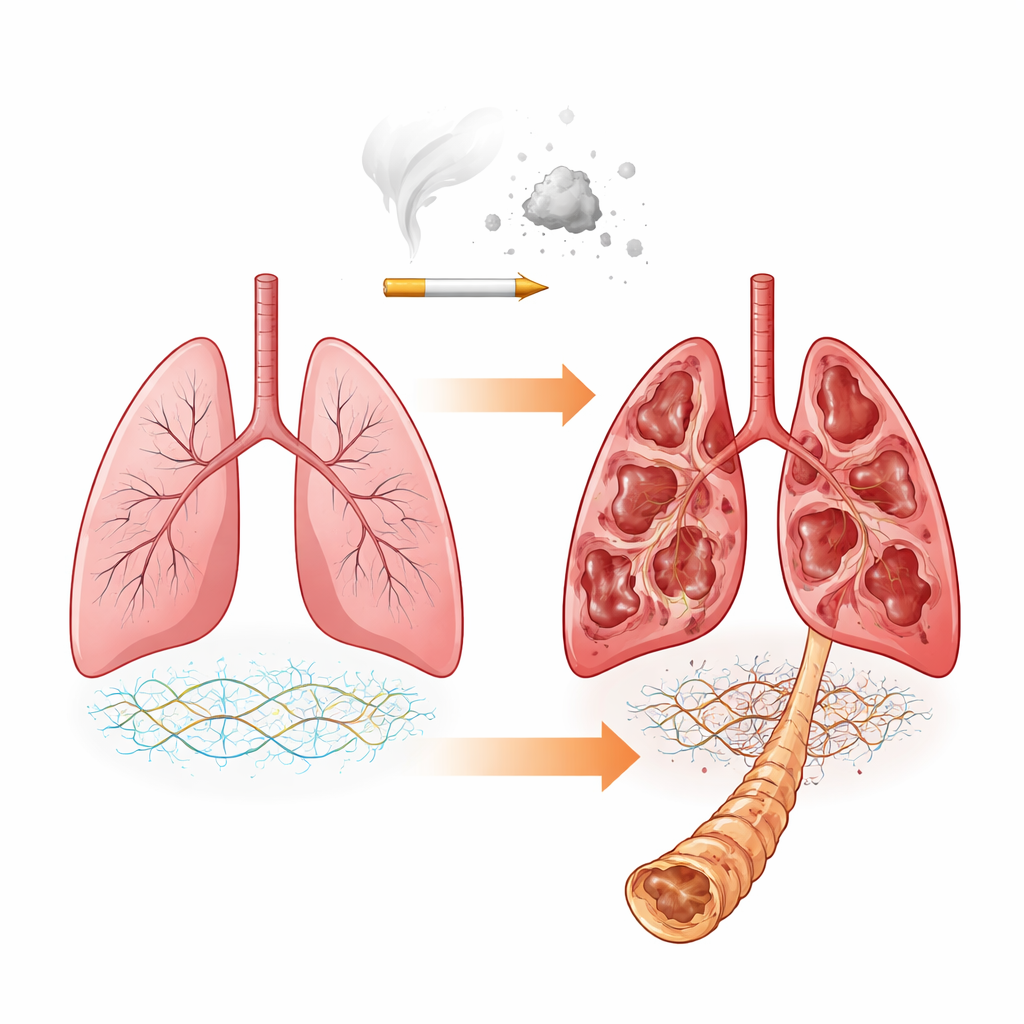
Het verborgen ondersteuningsnetwerk van de long
Onze longen zijn opgebouwd rond een ingewikkeld ondersteuningsnetwerk dat de extracellulaire matrix wordt genoemd. Het bestaat uit eiwitten, zoals collageen, en speciale moleculen die proteoglycanen heten en lange suikerketens dragen die bekendstaan als glycosaminoglycanen (GAGs). Deze GAGs, waaronder chondroïtinesulfaat, dermatansulfaat en heparansulfaat, bepalen mede hoe stijf of elastisch het weefsel is en hoe het omgaat met groeifactoren en enzymen die de matrix afbreken. Bij COPD heeft eerder werk laten zien dat de totale samenstelling van matrixeiwitten verandert. Hier stelden de onderzoekers een meer gedetailleerde vraag: zelfs als de belangrijkste proteïnebackbones vergelijkbaar blijven, veranderen de aangrijpende suikerketens dan in samenstelling en chemische versiering naarmate de ziekte verergert?
Vergelijking van gezonde, rokers- en COPD-longen
Het team analyseerde longweefsel afkomstig van niet-rokers, rokers zonder COPD en patiënten met matige en ernstige COPD. Met gevoelige chemische methoden maten ze de totale hoeveelheid en de fijne structuur van GAGs in de distale delen van de longen, waar gasuitwisseling plaatsvindt. Ze herkeken ook bestaande datasets over eiwitten en genactiviteit van vergelijkbare patiënten. Terwijl de kern-proteoglycaan-eiwitten zelf in de kleine proteïne-dataset geen grote verschillen lieten zien, was de totale hoeveelheid GAGs hoger bij COPD, vooral bij gevorderde ziekte. De meest overvloedige GAGs waren chondroïtine- en dermatansulfaten, en deze waren al verhoogd bij patiënten met matige COPD vergeleken met gezonde controles.
Chemische bijstellingen van suikerketens in zieke longen
Kijkend voorbij de totale hoeveelheden zoomden de wetenschappers in op hoe individuele suikerbouwstenen binnen GAG-ketens werden gemodificeerd. Bij ernstige COPD toonde heparansulfaat meer gesulfateerde groepen op specifieke posities, een verandering die kan beïnvloeden hoe het signaalmoleculen bindt. Nog opvallender waren de veranderingen in chondroïtine- en dermatansulfaat. Suikers met een bepaald type sulfaatgroep op de 4-positie werden vaker aangetroffen in alle COPD-stadia, en een deel van deze suikers werd omgezet in een iets andere vorm (iduronicumzuur) die bekendstaat om zijn invloed op hoe de matrix met enzymen en groeifactoren interageert. Deze structurele vingerafdrukken kwamen overeen met een toename in activiteit van meerdere genen die deze ketens opbouwen en modificeren, met name CHST11, dat helpt de 4-sulfaatgroep te plaatsen.
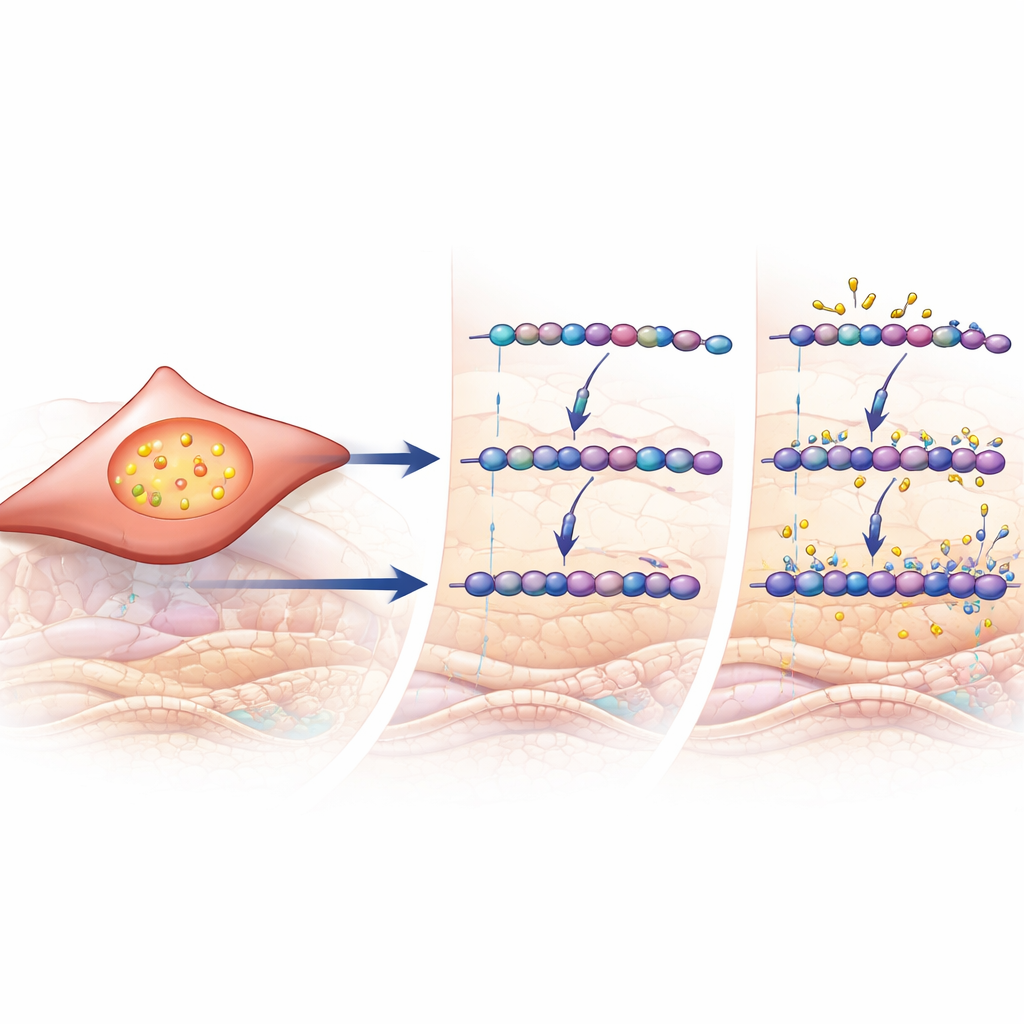
Een signaleringsschakelaar die remodellering aanstuurt
Om te achterhalen wat deze suiker-modificerende enzymen mogelijk activeert, richtten de onderzoekers zich op grootschalige genexpressiegegevens en celexperimenten. In longmonsters van patiënten werden genen die in COPD omhooggingen verrijkt gevonden voor genen die bekendstaan als responsief op het signaalmolecuul TGF-β, een belangrijke aanjager van littekenvorming en remodellering in vele weefsels. De expressie van CHST11 en meerdere verwante enzymen liep gelijk op met een berekende TGF-β-activiteitsscore. In gekweekte humane longfibroblasten verhoogde directe blootstelling aan TGF-β de productie van chondroïtine/dermatansulfaat, vergrootte de specifieke 4-gesulfateerde suikers die in patiëntlongen werden gezien, en verhoogde CHST11-niveaus. Gezamenlijk verbinden deze bevindingen een bekend remodelleringssignaal met de precieze chemische herschikking van GAG-ketens die in COPD-longen is waargenomen.
Wat dit betekent voor toekomstige behandelingen
Voor mensen die met COPD leven suggereren deze resultaten dat het longgeraamte niet alleen afbreekt; het wordt chemisch herbedraad op een manier die afhangt van het ziektestadium. De toegevoegde sulfaatgroepen en de gewijzigde suiker vormen in chondroïtine/dermatan- en heparansulfaatketens zullen waarschijnlijk veranderen hoe de matrix enzymen, groeifactoren en ontstekingsmoleculen bindt, wat mogelijk bijdraagt aan aanhoudende weefselschade en littekenvorming. Omdat deze veranderingen zijn gekoppeld aan specifieke enzymen zoals CHST11 en aan TGF-β-signaalroutes, wijzen ze op nieuwe, meer precieze medicinale doelwitten: in plaats van breedweg ontsteking te remmen, zouden toekomstige therapieën kunnen proberen de wijze waarop longsuikerketens worden opgebouwd en gemodificeerd voorzichtig te herevenwichtigen, met als doel het weefsel te stabiliseren en de progressie van COPD te vertragen.
Bronvermelding: Alsafadi, H.N., Nybom, A., Wagner, D. et al. Change in the chondroitin/dermatan structure in distal lung tissue from COPD patients. Sci Rep 16, 9721 (2026). https://doi.org/10.1038/s41598-026-44120-4
Trefwoorden: COPD, longmatrix, glycosaminoglycanen, extracellulair remodelleren, TGF-beta signalering