Clear Sky Science · fr
Modification de la structure chondroïtine/dermatane dans le tissu pulmonaire distal de patients atteints de BPCO
Pourquoi cela compte pour les personnes atteintes de BPCO
La bronchopneumopathie chronique obstructive (BPCO) est généralement décrite comme un problème d’obstruction des voies aériennes et de destruction des alvéoles. Mais derrière ces symptômes connus se cache une armature de sucres et de protéines qui maintient le tissu pulmonaire et régule l’inflammation. Cette étude examine de près cette armature dans des poumons humains et montre que les chaînes de sucres qui la composent sont chimiquement remaniées au fur et à mesure de la progression de la BPCO. Comprendre ces modifications subtiles pourrait ouvrir de nouvelles voies pour ralentir les dommages pulmonaires plutôt que de se limiter à traiter les symptômes.
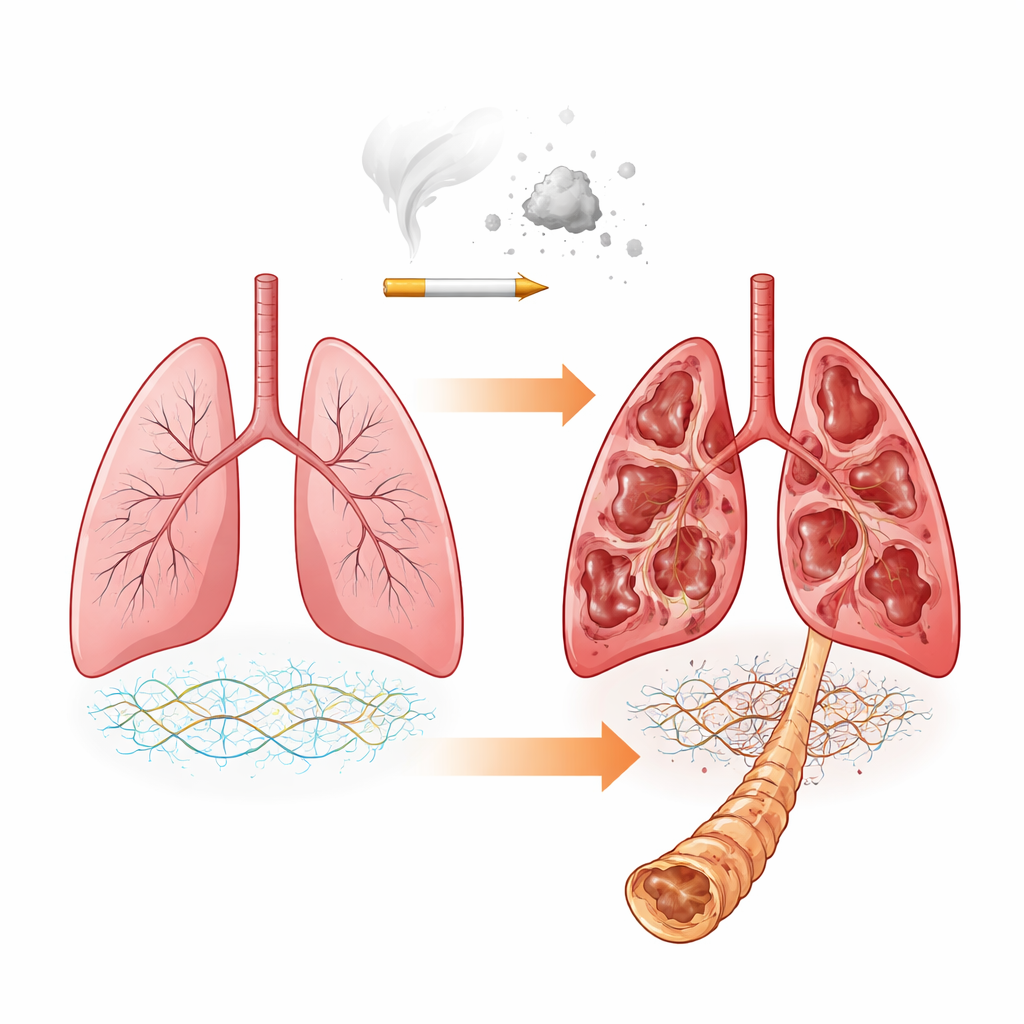
Le réseau de soutien caché du poumon
Nos poumons reposent sur un réseau de soutien complexe appelé matrice extracellulaire. Il est constitué de protéines, comme le collagène, et de molécules particulières nommées protéoglycanes qui portent de longues chaînes de sucres appelées glycosaminoglycanes (GAG). Ces GAG, notamment le chondroïtine sulfate, le dermatane sulfate et l’héparane sulfate, contribuent à déterminer la rigidité ou l’élasticité des tissus et à moduler les interactions avec les facteurs de croissance et les enzymes qui dégradent la matrice. Dans la BPCO, des travaux antérieurs ont montré que la composition globale des protéines de la matrice change. Ici, les chercheurs posent une question plus fine : même si les charpentes protéiques principales restent similaires, les chaînes de sucres attachées changent-elles de composition et de décor chimique à mesure que la maladie s’aggrave ?
Comparaison des poumons sains, de fumeurs et de patients BPCO
L’équipe a analysé des tissus pulmonaires prélevés chez des non-fumeurs, des fumeurs sans BPCO, et des patients atteints de BPCO modérée et sévère. À l’aide de méthodes chimiques sensibles, ils ont mesuré la quantité totale et la structure fine des GAG dans les régions distales des poumons, où se fait l’échange gazeux. Ils ont également réexaminé des jeux de données protéiques et transcriptomiques existants provenant de patients similaires. Si les protéines de base des protéoglycanes n’affichaient pas de grandes différences dans le petit jeu de données protéique, la quantité totale de GAG était plus élevée dans la BPCO, en particulier dans les stades avancés. Les GAG les plus abondants étaient le chondroïtine et le dermatane sulfates, déjà augmentés chez les patients atteints de BPCO modérée par rapport aux témoins sains.
Ajustements chimiques des chaînes de sucres dans les poumons malades
Au-delà des niveaux totaux, les scientifiques se sont penchés sur la modification des unités sucrées individuelles au sein des chaînes de GAG. Dans la BPCO sévère, l’héparane sulfate présentait davantage de groupes sulfate ajoutés en positions spécifiques, une modification susceptible d’altérer sa capacité à lier des molécules de signalisation. Les changements les plus marquants concernaient toutefois le chondroïtine et le dermatane sulfate. Les sucres portant un type particulier de sulfate en position 4 sont devenus plus fréquents à tous les stades de la BPCO, et une fraction de ces sucres a été convertie en une forme légèrement différente (acide iduronique) connue pour influencer les interactions de la matrice avec les enzymes et les facteurs de croissance. Ces empreintes structurales concordaient avec une augmentation de l’activité de plusieurs gènes impliqués dans la synthèse et la modification de ces chaînes, notamment CHST11, qui participe à l’ajout du groupe 4-sulfate.
Un basculement de signalisation qui conduit au remodelage
Pour identifier ce qui pourrait activer ces enzymes modifiant les sucres, les chercheurs se sont tournés vers des données transcriptomiques à grande échelle et des expériences cellulaires. Dans les échantillons pulmonaires de patients, les gènes surexprimés dans la BPCO étaient enrichis en gènes connus pour répondre à la molécule de signalisation TGF-β, un moteur clé de la fibrose et du remodelage dans de nombreux tissus. L’expression de CHST11 et de plusieurs enzymes apparentées suivait un score d’activité TGF-β calculé. Dans des fibroblastes pulmonaires humains en culture, une exposition directe au TGF-β augmentait la production de chondroïtine/dermatane sulfate, favorisait les sucres 4-sulfatés observés chez les patients et élevait les niveaux de CHST11. Ensemble, ces résultats relient un signal de remodelage bien établi au remaniement chimique précis des chaînes de GAG observé dans les poumons atteints de BPCO.
Ce que cela implique pour les traitements futurs
Pour les personnes vivant avec la BPCO, ces résultats suggèrent que le « squelette » pulmonaire ne se contente pas de se dégrader ; il est chimiquement reconfiguré de façon spécifique au stade de la maladie. Les groupes sulfate ajoutés et les formes de sucres modifiées dans les chaînes de chondroïtine/dermatane et d’héparane sulfate devraient modifier la manière dont la matrice fixe les enzymes, les facteurs de croissance et les molécules inflammatoires, contribuant potentiellement aux lésions et à la fibrose en cours. Parce que ces changements sont liés à des enzymes spécifiques comme CHST11 et à la signalisation TGF-β, ils pointent vers de nouvelles cibles thérapeutiques plus précises : plutôt que de bloquer l’inflammation de façon globale, des thérapies futures pourraient viser à rééquilibrer doucement la construction et la modification des chaînes sucrées pulmonaires, afin de stabiliser le tissu et ralentir la progression de la BPCO.
Citation: Alsafadi, H.N., Nybom, A., Wagner, D. et al. Change in the chondroitin/dermatan structure in distal lung tissue from COPD patients. Sci Rep 16, 9721 (2026). https://doi.org/10.1038/s41598-026-44120-4
Mots-clés: BPCO, matrice pulmonaire, glycosaminoglycanes, remodelage extracellulaire, signalisation TGF-bêta