Clear Sky Science · de
Veränderung der Chondroitin-/Dermatan-Struktur im distalen Lungengewebe von COPD-Patienten
Warum das für Menschen mit COPD wichtig ist
Chronisch obstruktive Lungenerkrankung (COPD) wird üblicherweise als Problem verengter Atemwege und geschädigter Lungenbläschen beschrieben. Hinter diesen vertrauten Symptomen verbirgt sich jedoch ein unsichtbares Gerüst aus Zuckern und Proteinen, das das Lungengewebe zusammenhält und Entzündungen steuert. Diese Studie untersucht dieses Gerüst in menschlichen Lungen genauer und zeigt, dass seine Zuckerketten chemisch umgebaut werden, wenn die COPD fortschreitet. Das Verständnis dieser feinen Veränderungen könnte neue Wege eröffnen, um Schäden in der Lunge zu verlangsamen, statt nur die Symptome zu behandeln.
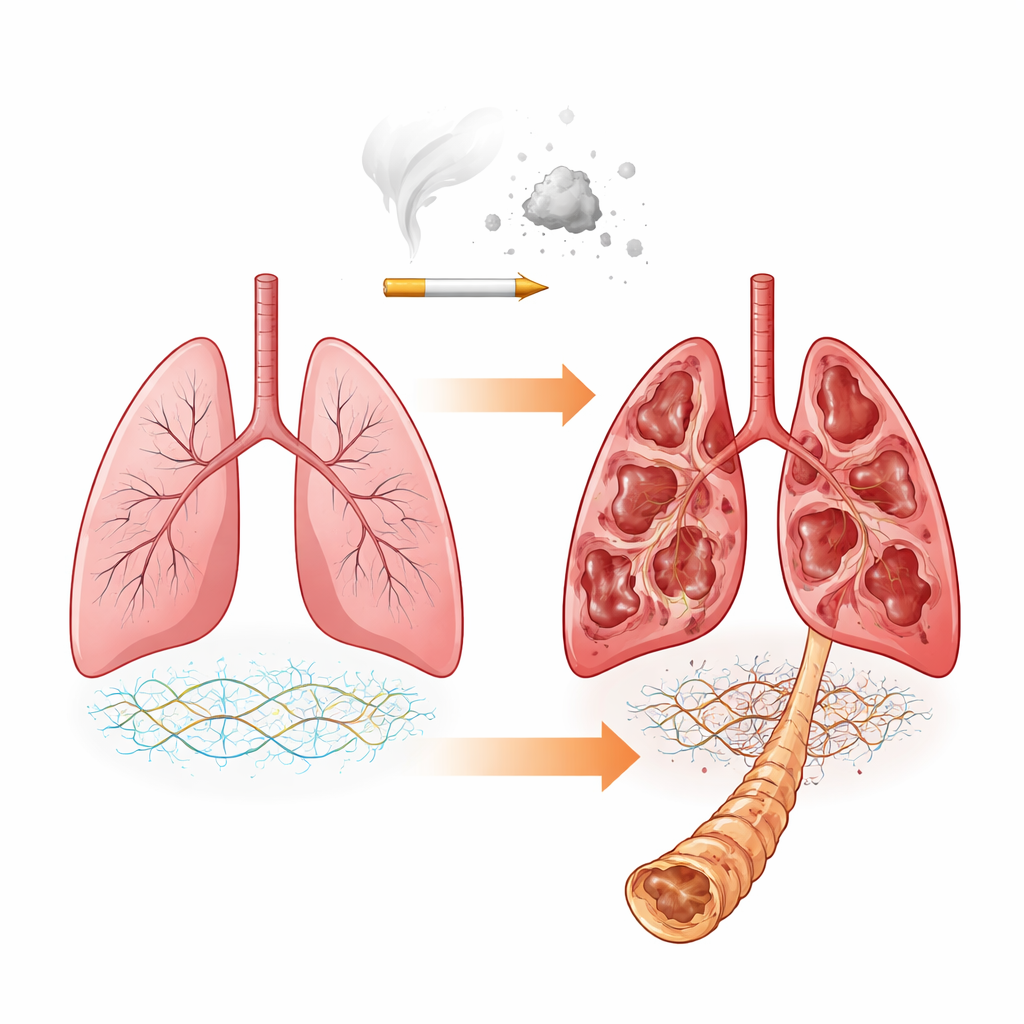
Das verborgene Stütznetz der Lunge
Unsere Lungen sind um ein komplexes Stütznetz herum aufgebaut, die extrazelluläre Matrix. Sie besteht aus Proteinen wie Kollagen und speziellen Molekülen, den Proteoglykanen, die lange Zuckerketten tragen, sogenannte Glykosaminoglycane (GAGs). Diese GAGs — darunter Chondroitinsulfat, Dermatansulfat und Heparansulfat — bestimmen mit, wie steif oder elastisch das Gewebe ist und wie es mit Wachstumsfaktoren und Matrix-abbauenden Enzymen interagiert. Frühere Arbeiten zeigten, dass sich die Gesamtzusammensetzung der Matrixproteine bei COPD verändert. Die hier untersuchte Frage geht ins Detail: Selbst wenn die Hauptprotein-Gerüste ähnlich bleiben, verändern sich die angehängten Zuckerketten in Zusammensetzung und chemischer Modifikation, wenn die Erkrankung schlimmer wird?
Vergleich gesunder, rauchender und COPD-Lungen
Das Team analysierte Lungengewebe von Nichtrauchern, Rauchern ohne COPD sowie Patienten mit moderater und schwerer COPD. Mithilfe sensitiver chemischer Methoden bestimmten sie die Gesamtmenge und die Feinstruktur der GAGs in den distalen Lungenbereichen, wo der Gasaustausch stattfindet. Außerdem werteten sie vorhandene Protein- und Genaktivitätsdaten aus ähnlichen Patientengruppen erneut aus. Während die Kern-Proteoglykan-Proteine in dem kleineren Proteindatensatz keine großen Unterschiede zeigten, war die Gesamtmenge an GAGs bei COPD erhöht, besonders in fortgeschritteneren Stadien. Am häufigsten waren Chondroitin- und Dermatan sulfate, die bereits bei Patienten mit moderater COPD gegenüber gesunden Kontrollen höher lagen.
Chemische Veränderungen der Zuckerketten in erkrankter Lunge
Über die Gesamtmengen hinaus untersuchten die Forscher, wie einzelne Zuckerbausteine innerhalb der GAG-Ketten modifiziert waren. Bei schwerer COPD zeigte Heparansulfat vermehrt Sulfatgruppen an spezifischen Positionen, eine Änderung, die seine Bindung an Signalmoleküle beeinflussen kann. Noch auffälliger waren die Änderungen bei Chondroitin- und Dermatansulfat. Zucker mit einer bestimmten Sulfatierung an Position 4 wurden in allen COPD-Stadien häufiger, und ein Teil dieser Zucker wurde in eine leicht andere Form (Iduronsäure) umgewandelt, die bekannt dafür ist, wie die Matrix mit Enzymen und Wachstumsfaktoren interagiert. Diese strukturellen Merkmale stimmten mit einer erhöhten Aktivität mehrerer Gene überein, die diese Ketten bauen und modifizieren — besonders mit CHST11, das die 4-Sulfatgruppe anbringt.
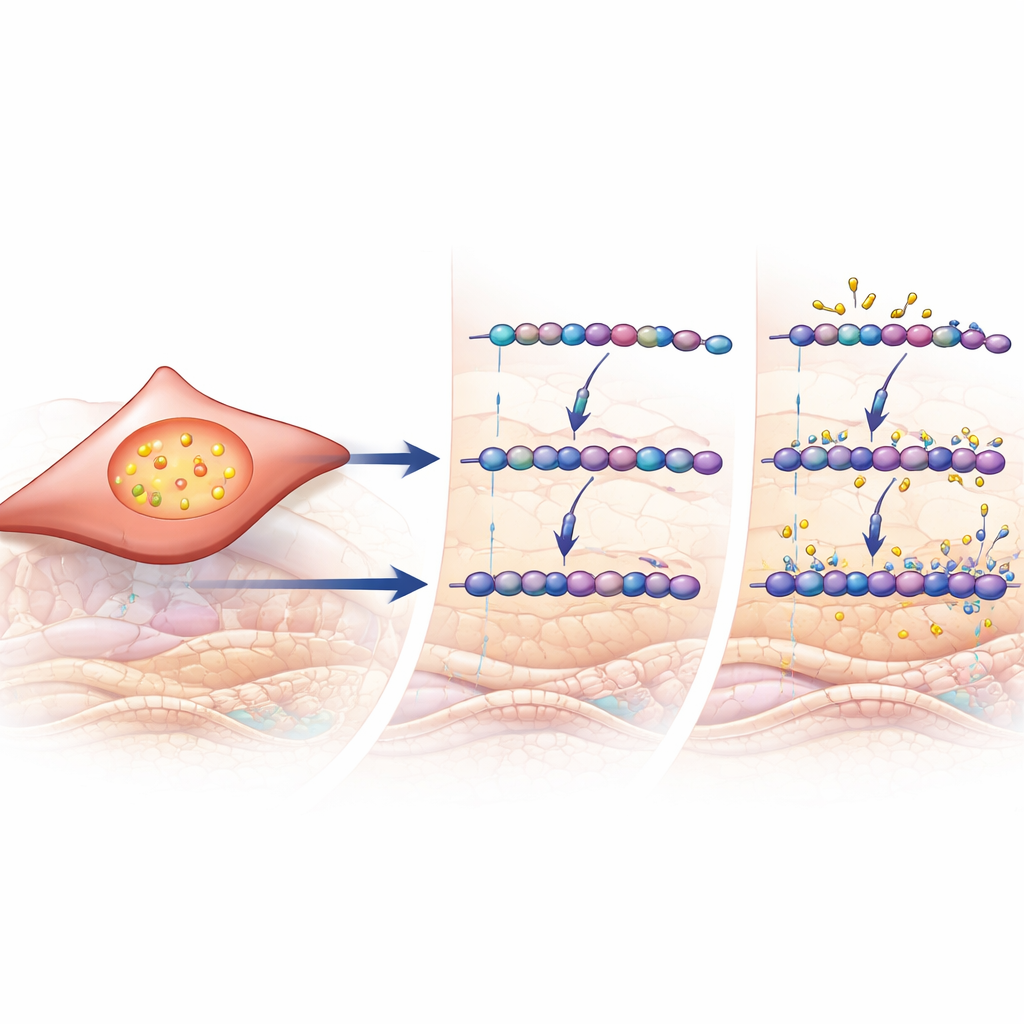
Ein Signalwechsel, der Remodeling antreibt
Um herauszufinden, was diese zuckermodifizierenden Enzyme einschaltet, betrachteten die Forschenden groß angelegte Gen-Daten und Zellenversuche. In Lungenproben von Patienten fanden sich bei COPD gehäuft Gene, die auf das Signalmolekül TGF-β reagieren — ein zentraler Treiber von Vernarbung und Remodeling in vielen Geweben. Die Expression von CHST11 und mehreren verwandten Enzymen korrelierte mit einem berechneten TGF-β-Aktivitätsscore. In kultivierten humanen Lungenfibroblasten führte direkte TGF-β-Exposition zu einer erhöhten Produktion von Chondroitin-/Dermatansulfat, zu einem Anstieg der speziellen 4-sulfatierten Zucker, die in Patientenlungen beobachtet wurden, und zu höheren CHST11-Werten. Zusammen verknüpfen diese Befunde ein bekanntes Remodeling-Signal mit der präzisen chemischen Umgestaltung der GAG-Ketten in COPD-Lungen.
Was das für künftige Therapien bedeutet
Für Menschen mit COPD deuten diese Ergebnisse darauf hin, dass das Lungen-Gerüst nicht nur zerfällt, sondern krankheitsstadien-spezifisch chemisch umprogrammiert wird. Die zusätzlich eingebrachten Sulfatgruppen und veränderten Zuckerformen in Chondroitin-/Dermatan- und Heparansulfatketten werden wahrscheinlich beeinflussen, wie die Matrix Enzyme, Wachstumsfaktoren und Entzündungsmoleküle bindet — und könnten so zu anhaltenden Gewebeschäden und Vernarbung beitragen. Da diese Veränderungen mit bestimmten Enzymen wie CHST11 und mit der TGF-β-Signalgebung verknüpft sind, eröffnen sie präzisere pharmakologische Ansatzpunkte: Statt die Entzündung breit zu blockieren, könnten künftige Therapien darauf abzielen, den Aufbau und die Modifikation der Lungen-Zuckerketten gezielt zu rekonfigurieren, um das Gewebe zu stabilisieren und das Fortschreiten der COPD zu verlangsamen.
Zitation: Alsafadi, H.N., Nybom, A., Wagner, D. et al. Change in the chondroitin/dermatan structure in distal lung tissue from COPD patients. Sci Rep 16, 9721 (2026). https://doi.org/10.1038/s41598-026-44120-4
Schlüsselwörter: COPD, Lungenmatrix, Glykosaminoglycane, extrazelluläres Remodeling, TGF-beta-Signalgebung