Clear Sky Science · zh
通过蓝光 LED 驱动的不饱和酰胺硒化,获取β-乙酰氧基硒化物、全氢化吲哚酮和抗癌哌啶酮
为未来癌症药物提供光驱动化学
化学家与生物学家携手利用简单的蓝光 LED 构建新的含硒分子,这些分子在未来作为抗癌候选药物方面显示出希望。通过精细调整这类光驱动的化学反应,他们能够将相同的起始物导向截然不同的产物,并测试哪些产物在实验室中最有效地抑制癌细胞的生长。
把蓝光照在新分子上
这项研究以一类称为酰胺的有机分子为中心,可以将其视为易于修改的“骨架”。研究者在含有硒试剂与常见酸(如醋酸和蚁酸)的条件下,用蓝光 LED 照射这些起始物。反应无需苛刻条件或有毒添加剂,在空气中并依赖可见光进行,因而相对温和且易于操作。通过调整酰胺的类型和溶剂,团队发现相同的成分可以被引导生成不同的产物,范围从开链分子到紧凑的环形结构。
像交通引导反应进程
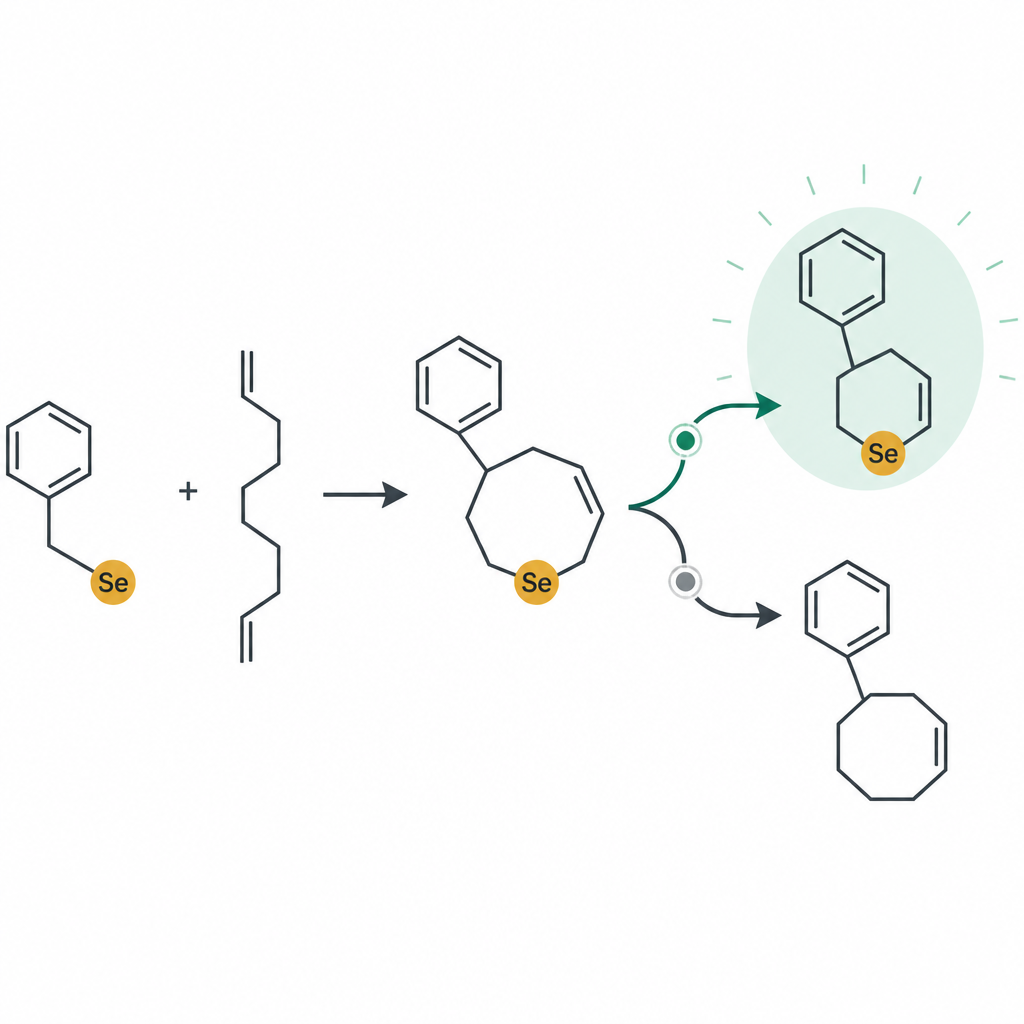
这项工作的一个关键见解是反应在原子层面上像一个小型交通网络。当蓝光照射到硒试剂时,它裂解并产生高度活泼的片段,这些片段迅速加成到起始酰胺的碳–碳双键上。接下来发生的事情取决于该双键周围的“环境”:氮侧基的性质、酸的强弱和类型,以及是否存在某些盐。在某些情况下,酸促使乙酰氧基插入,生成由三个组分组成的产物,称为β-乙酰氧基硒化物。在其他情形下,酰胺发生弯折并闭合成五元或六元环,形成全氢化吲哚酮和哌啶酮,并在确定的位置携带一个硒原子。
氧气与微妙作用力如何塑造结果
团队通过在不同条件下重复反应来探究这种光驱动化学的实际机制。当他们从混合物中移除氧气时,反应停止,表明空气在活化硒试剂中起着关键作用。加入常见的自由基捕捉剂并没有阻止产物形成,这提示只有最初的步骤涉及短寿命的自由基物种,随后体系转入更有序的离子过程。不同产物之间的平衡对微小变化极为敏感。较强的酸会将反应从以氧为主的闭合转向以氮为主的环化,而含有弱相互作用阴离子的盐有助于促使难以反应的底物形成六元内酰胺环。这些实验共同促成了一个详细的机理提议,说明了反应如何通过带电中间体推进以及为何某些路径被优先选择。
从试管到癌细胞
在产生的多种含硒哌啶酮中,有一种标记为 12ea 的化合物在生物学测试中脱颖而出。研究者将包括宫颈癌和结直肠癌细胞在内的几种人类癌细胞系暴露于不同剂量的各化合物,并测量其抑制细胞生长的强度。化合物 12ea 在多种癌细胞系中于低微摩尔浓度下抑制生长,同时对正常肺成纤维细胞的影响较弱,提示具有一定选择性。后续实验证明,受处理的癌细胞并非单纯因不可控损伤而死亡;相反,它们经历了程序性细胞死亡(即凋亡)。该过程的标志包括被称为半胱天冬酶的执行酶的激活、通过荧光探针检测到的膜特征改变,以及细胞核内 DNA 损伤斑点的形成。
在三维肿瘤类簇中测试
为更好地模拟真实肿瘤,团队将癌细胞作为三维球体培养,这些紧密簇团再现了体内的一些氧气与营养梯度。当用先导化合物 12ea 处理这些球体时,其生长显著减慢,簇团在数天内变得更小且密度降低。荧光染色显示在较高剂量下球体内部广泛存在凋亡信号,说明该化合物能够在更类似肿瘤的环境中穿透并保持活性。这一点很重要,因为许多在平面细胞层面有效的药物在三维模型中往往大幅降低疗效。
这对未来治疗意味着什么
总体而言,该研究向非专业读者传达了两点主要信息。首先,它表明简单的蓝光 LED 与审慎选择的反应条件可以让化学家精确控制分子的组装方式,使得可以以更清洁、更可持续的方式构建复杂的含硒环。其次,它鉴定出一种产物——化合物 12ea,作为通过受控细胞死亡作用且在三维肿瘤模型中仍然有效的具有选择性和高效性的某些癌细胞杀伤剂。尽管该分子距离成为药物还有很长的路要走,且尚未在动物或人体中测试,但它为设计更佳的类似物并探索如何在未来的抗癌治疗中利用含硒化学提供了明确的起点。
引用: Vaskevych, A., Maciejewska, N., Mysiak, A. et al. Access to β-acetoxyselenides, perhydroindolones and anticancer piperidinones via blue LED-driven selenylation of unsaturated carboxamides. Sci Rep 16, 14963 (2026). https://doi.org/10.1038/s41598-026-44112-4
关键词: 有机硒化学, 蓝光 LED 硒化反应, 哌啶酮 抗癌, 癌细胞凋亡, 三维肿瘤球体