Clear Sky Science · it
Accesso a β-acetossipelenuri, peridroindolone e piperidinoni anticancro tramite selenilazione di carbossammidi insature attivata da LED blu
Chimica alimentata dalla luce per i futuri farmaci anticancro
Chimici e biologi hanno collaborato per sfruttare semplici LED blu nella costruzione di nuove molecole a base di selenio che mostrano potenzialità come futuri candidati anticancro. Affinando questa chimica guidata dalla luce, possono indirizzare gli stessi materiali di partenza verso prodotti molto diversi e quindi testare quali rallentano più efficacemente la crescita delle cellule tumorali in laboratorio.
Illuminare nuove molecole con luce blu
Lo studio si concentra su una famiglia di molecole organiche chiamate carbossammidi, che possono essere viste come «scheletri» flessibili facili da modificare. I ricercatori hanno esposto questi materiali di partenza a luce LED blu in presenza di reagenti contenenti selenio e acidi comuni come l’acetico e il formico. Invece di usare condizioni aggressive o additivi tossici, le reazioni avvengono all’aria e si basano sulla luce visibile, rendendole relativamente miti e semplici da eseguire. Variando il tipo di ammide e il solvente, il gruppo ha scoperto che gli stessi ingredienti possono essere indotti a formare prodotti diversi, che vanno da molecole a catena aperta a strutture compatte ad anello.
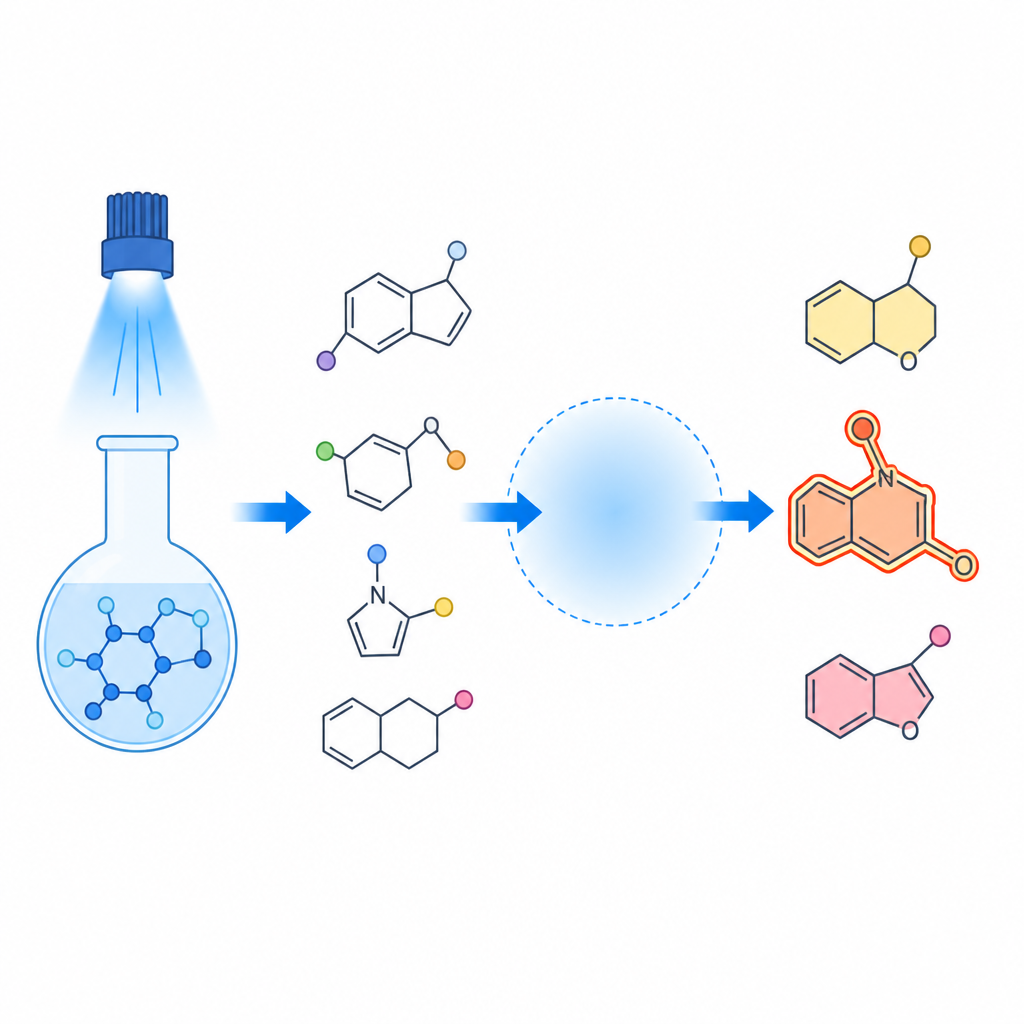
Instradare le reazioni come il traffico
Un’idea chiave del lavoro è che la reazione si comporta come una piccola rete di traffico a livello atomico. Quando la luce blu colpisce il reagente al selenio, questo si scinde generando frammenti altamente reattivi che si aggiungono rapidamente al doppio legame carbonio–carbonio nella ammide di partenza. Ciò che accade dopo dipende dall’«ambiente» intorno a quel legame: la natura del gruppo laterale sull’azoto, la forza e il tipo di acido, e la presenza di certi sali. In alcuni casi, l’acido favorisce l’ingresso di un gruppo acetato, dando prodotti a tre componenti noti come β-acetossipelenuri. In altre situazioni, l’ammide si ripiega su se stessa chiudendo in anelli a cinque o sei membri noti come peridroindoloni e piperidinoni, incorporando un atomo di selenio in una posizione definita.
Come ossigeno e forze sottili plasmano l’esito
Il team ha indagato il funzionamento di questa chimica guidata dalla luce ripetendo le reazioni in condizioni diverse. Rimuovendo l’ossigeno dalla miscela, il processo si è arrestato, dimostrando che l’aria gioca un ruolo essenziale nell’attivazione del reagente al selenio. L’aggiunta di una trappola per radicali comune non ha fermato la formazione del prodotto, il che suggerisce che solo il primo passo coinvolge specie radicaliche di breve durata prima che il sistema si stabilizzi in un processo ionico più ordinato. L’equilibrio tra i diversi prodotti si è rivelato altamente sensibile a piccole variazioni. Un acido più forte ha spostato la reazione lontano dalla chiusura mediata dall’ossigeno verso la formazione di anelli con l’azoto, mentre un sale contenente un anione debolmente interagente ha favorito substrati recalcitranti a formare lattame a sei membri. Nel complesso, questi test hanno portato a una proposta dettagliata di come la reazione procede attraverso intermedi caricati e perché certe vie siano favorite.
Dal provettone alle cellule tumorali
Tra i molti piperidinoni contenenti selenio prodotti, un composto, etichettato 12ea, è emerso nei test biologici. I ricercatori hanno esposto diverse linee cellulari tumorali umane, incluse cellule di tumore cervicale e colorettale, a quantità crescenti di ciascun composto e hanno misurato quanto efficacemente riducevano la crescita cellulare. Il composto 12ea ha inibito la crescita a basse concentrazioni micromolari in più linee tumorali, influenzando meno intensamente i fibroblasti polmonari normali, suggerendo un certo grado di selettività. Esperimenti di follow-up hanno mostrato che le cellule tumorali trattate non morivano semplicemente per danno incontrollato; al contrario, subirono morte cellulare programmata, ovvero apoptosi. I marcatori di questo processo includevano l’attivazione di enzimi esecutori chiamati caspasi, cambiamenti nelle caratteristiche di membrana rilevati da sonde fluorescenti e la formazione di focolai di danno al DNA all’interno dei nuclei cellulari.
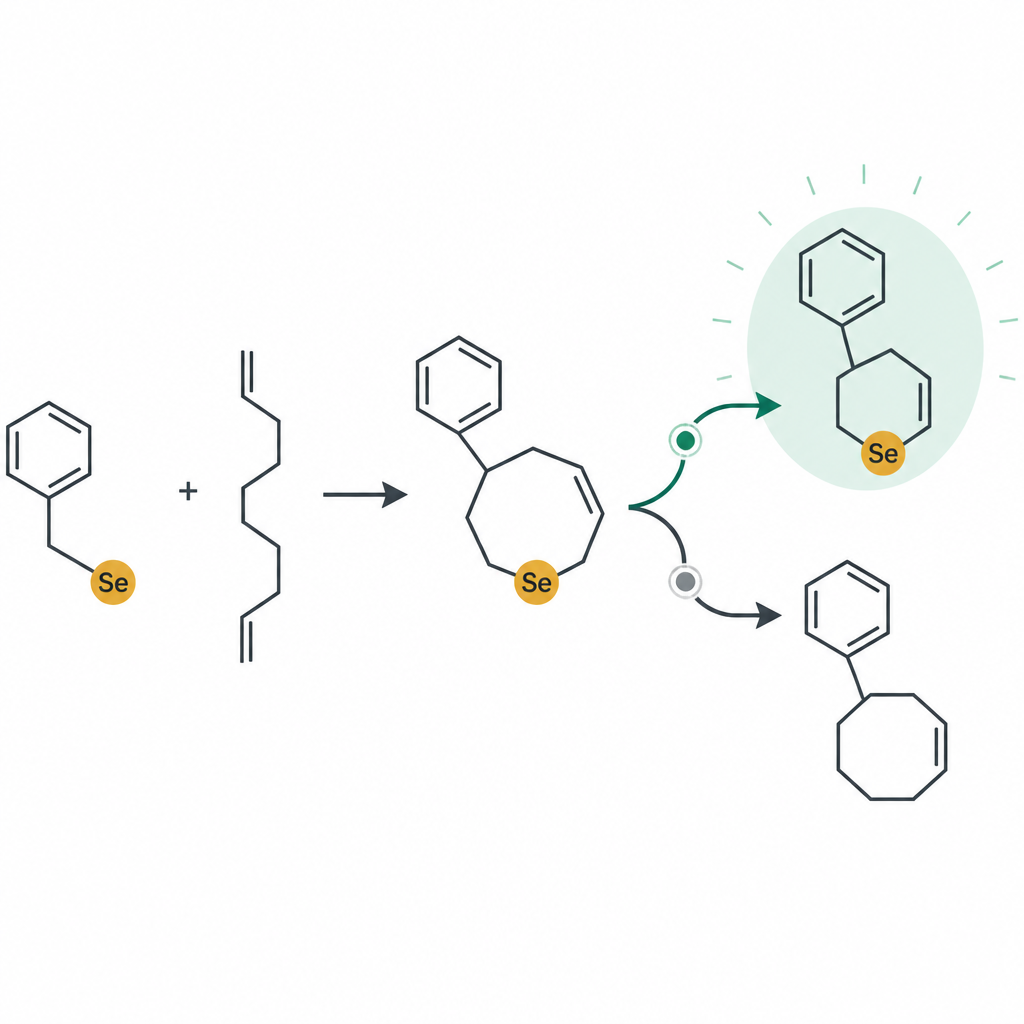
Test in aggregati tumorali 3D
Per imitare meglio i tumori reali, il gruppo ha coltivato le cellule tumorali come sferoidi tridimensionali, cluster compatti che riproducono alcuni dei gradienti di ossigeno e nutrienti presenti nell’organismo. Quando questi sferoidi sono stati trattati con il composto principale 12ea, la loro crescita si è rallentata drasticamente e i cluster sono diventati più piccoli e meno densi nel corso di alcuni giorni. La colorazione fluorescente ha rivelato segnali forti di morte cellulare apoptotica in tutto lo sferoide a dosi più alte, dimostrando che il composto può penetrare e rimanere attivo in un contesto più realistico simile a un tumore. Questo è importante, perché molti farmaci efficaci su monostrati cellulari perdono gran parte del loro effetto nei modelli 3D.
Cosa potrebbe significare per trattamenti futuri
Complessivamente, lo studio offre due messaggi principali per i non specialisti. Primo, dimostra che una semplice luce LED blu e una scelta oculata delle condizioni permettono ai chimici di controllare con precisione come le molecole si assemblano, consentendo la costruzione di anelli complessi contenenti selenio in modo più pulito e sostenibile. Secondo, identifica uno di questi prodotti, il composto 12ea, come un agente selettivo e potente contro certe cellule tumorali che agisce tramite morte cellulare controllata e resta efficace in modelli tumorali 3D. Pur essendo ancora lontano dall’essere un farmaco e non essendo stato testato in animali o in persone, questo composto fornisce un punto di partenza ben definito per progettare analoghi migliori ed esplorare come la chimica a base di selenio possa essere sfruttata in future terapie anticancro.
Citazione: Vaskevych, A., Maciejewska, N., Mysiak, A. et al. Access to β-acetoxyselenides, perhydroindolones and anticancer piperidinones via blue LED-driven selenylation of unsaturated carboxamides. Sci Rep 16, 14963 (2026). https://doi.org/10.1038/s41598-026-44112-4
Parole chiave: chimica organoseleniata, selenilazione con LED blu, piperidinone anticancro, apoptosi nelle cellule tumorali, sfere tumorali 3D