Clear Sky Science · de
Zugang zu β‑Acetoxyseleniden, Perhydroindolonen und antitumoralen Piperidinonen durch blauem LED‑getriebene Selenylierung ungesättigter Carboxamide
Mit Licht betriebene Chemie für künftige Krebsmedikamente
Chemiker und Biologen haben sich zusammengetan, um mithilfe einfachen blauen LED‑Lichts neue selenhaltige Moleküle zu bauen, die als mögliche künftige Wirkstoffkandidaten gegen Krebs vielversprechend sind. Durch das feine Abstimmen dieser lichtgesteuerten Chemie können sie dieselben Ausgangsstoffe in sehr unterschiedliche Produkte lenken und anschließend prüfen, welche davon im Labor das Krebszellwachstum am stärksten hemmen.
Neuen Molekülen mit blauem Licht auf der Spur
Die Studie konzentriert sich auf eine Familie organischer Moleküle, die als Carboxamide bezeichnet werden und als flexible „Rückgrate“ dienen, die sich leicht modifizieren lassen. Die Forschenden setzten diese Ausgangsstoffe blauem LED‑Licht in Anwesenheit von selenhaltigen Reagenzien und einfachen Säuren wie Essig‑ und Ameisensäure aus. Anstatt harter Bedingungen oder toxischer Zusatzstoffe zu verwenden, laufen die Reaktionen an Luft und beruhen auf sichtbarem Licht, was sie vergleichsweise mild und unkompliziert macht. Durch die Anpassung der Amid‑Art und des Lösungsmittels entdeckte das Team, dass sich dieselben Zutaten dazu bringen ließen, verschiedene Produkte zu bilden – von offenkettigen Molekülen bis zu kompakten ringförmigen Strukturen.
Reaktionen wie den Verkehr lenken
Eine zentrale Erkenntnis der Arbeit ist, dass sich die Reaktion wie ein kleines Verkehrsnetzwerk auf atomarer Ebene verhält. Wenn blaues Licht das Selenreagenz trifft, spaltet es dieses und erzeugt hochreaktive Fragmente, die sich schnell an die Doppelbindung zwischen Kohlenstoffatomen im Ausgangsamid anlagern. Was danach passiert, hängt von der „Umgebung“ um diese Bindung ab: der Natur der Stickstoff‑Seiten‑gruppe, der Stärke und Art der Säure und davon, ob bestimmte Salze vorhanden sind. In einigen Fällen hilft die Säure einer Acetatgruppe hereinzuspringen, wodurch Dreikomponentenprodukte entstehen, die als β‑Acetoxyselenide bekannt sind. In anderen Situationen klappt das Amid um sich selbst herum und schließt sich zum Schwanz beißend, wodurch fünf‑ oder sechsgliedrige Ringe entstehen – Perhydroindolone und Piperidinone – die ein Selenatom an einer definierten Position tragen.
Wie Sauerstoff und subtile Kräfte das Ergebnis formen
Das Team untersuchte, wie diese lichtgetriebene Chemie tatsächlich funktioniert, indem es die Reaktionen unter verschiedenen Bedingungen wiederholte. Entfernten sie den Sauerstoff aus dem Gemisch, stoppte der Prozess, was zeigt, dass Luft eine wesentliche Rolle bei der Aktivierung des Selenreagenz spielt. Das Hinzufügen einer üblichen Radikalfänger‑Verbindung stoppte die Produktbildung nicht, was darauf hindeutet, dass nur der allererste Schritt kurzlebige Radikalarten involviert, bevor das System in einen geordneteren ionischen Prozess übergeht. Das Gleichgewicht zwischen den unterschiedlichen Produkten erwies sich als sehr empfindlich gegenüber kleinen Änderungen. Eine stärkere Säure verschob die Reaktion weg von einem über Sauerstoff vermittelten Verschluss hin zur ringbildenden Reaktion über Stickstoff, während ein Salz mit einer schwach wechselwirkenden Anion half, hartnäckige Substrate zur Bildung sechsgliedriger Lactamringe zu treiben. Zusammen führten diese Tests zu einem detaillierten Vorschlag, wie die Reaktion über geladene Zwischenstufen verläuft und warum bestimmte Pfade begünstigt werden.
Vom Reagenzglas zu Krebszellen
Unter den vielen selenhaltigen Piperidinonen, die erzeugt wurden, stach eine Verbindung, bezeichnet als 12ea, in biologischen Tests hervor. Die Forschenden setzten mehrere menschliche Krebszelllinien, darunter Gebärmutterhals‑ und Darmkrebszellen, steigenden Konzentrationen der einzelnen Verbindungen aus und maßen, wie stark diese das Zellwachstum reduzierten. Verbindung 12ea hemmte das Wachstum in niedrigen Mikromolarbereichen in mehreren Krebszelllinien, während normale Lungenfibroblasten weniger stark betroffen waren, was auf ein gewisses Maß an Selektivität hindeutet. Folgeexperimente zeigten, dass die behandelten Krebszellen nicht einfach durch unkontrollierte Schäden starben; vielmehr durchliefen sie programmierten Zelltod, die Apoptose. Marker dieses Prozesses umfassten die Aktivierung von Effektorenzymen, den sogenannten Caspasen, Veränderungen an Membranmerkmalen, die durch fluoreszierende Sonden nachgewiesen wurden, und die Bildung von DNA‑Schadensfoci im Zellkern.
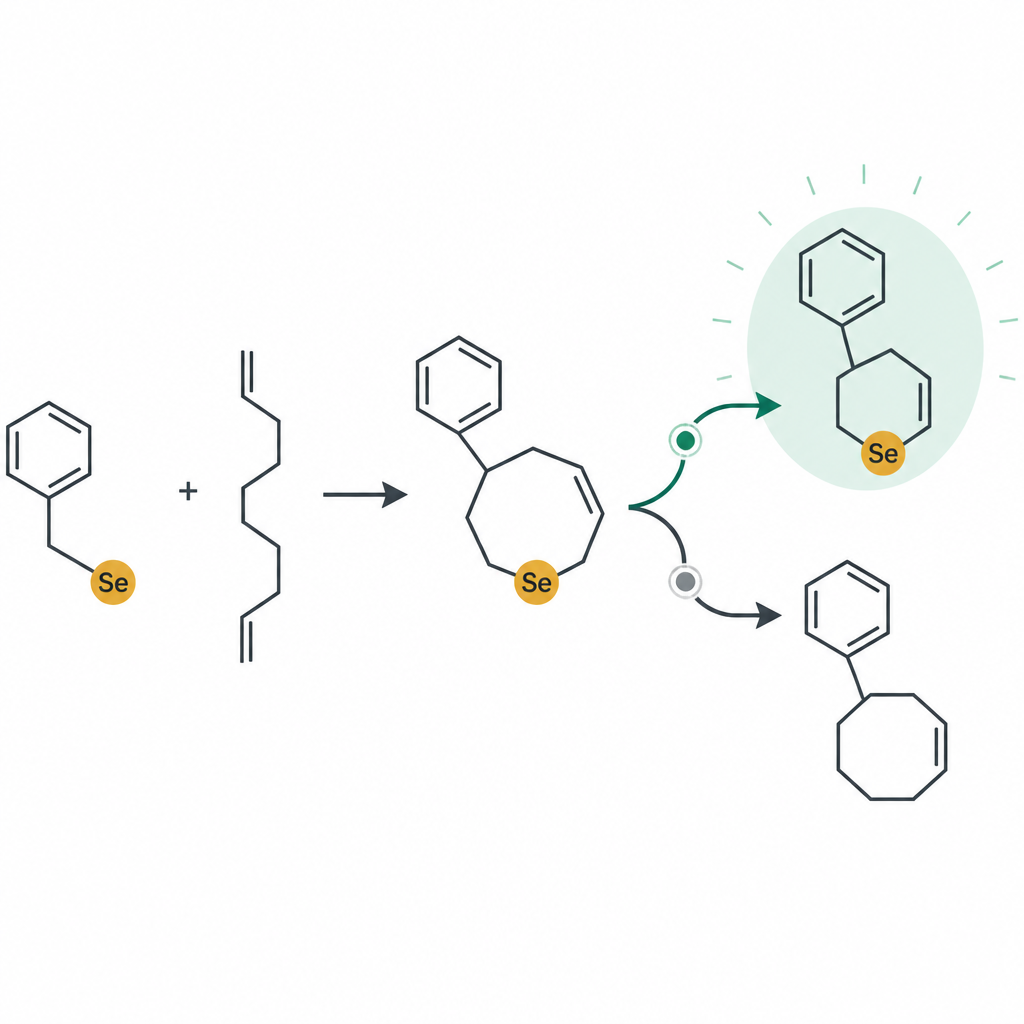
Tests in dreidimensionalen tumorähnlichen Verbänden
Um reale Tumoren besser nachzuahmen, züchtete das Team die Krebszellen als dreidimensionale Sphäroide – kompakte Verbände, die einige der Sauerstoff‑ und Nährstoffgradienten im Körper nachbilden. Wurden diese Sphäroide mit der Leitverbindung 12ea behandelt, verlangsamte sich ihr Wachstum dramatisch, und die Cluster wurden über mehrere Tage kleiner und weniger dicht. Fluoreszenzfärbungen zeigten starke Signale für apoptotischen Zelltod im gesamten Sphäroid bei höheren Dosen, was belegt, dass die Verbindung in ein realistischeres tumorähnliches Umfeld eindringen und dort aktiv bleiben kann. Das ist wichtig, weil viele Wirkstoffe, die auf zweidimensionalen Zellkulturen gut wirken, in 3D‑Modellen stark an Wirkung verlieren.
Was das für künftige Therapien bedeuten könnte
Insgesamt vermittelt die Studie zwei Hauptbotschaften für Nicht‑Fachleute. Erstens zeigt sie, dass einfaches blaues LED‑Licht und die kluge Wahl der Reaktionsbedingungen Chemikern eine feine Kontrolle darüber geben können, wie Moleküle sich zusammenfügen, sodass sie komplexe selenhaltige Ringe auf sauberere und nachhaltigere Weise bauen können. Zweitens identifiziert sie eines dieser Produkte, die Verbindung 12ea, als selektiven und potenten Killer bestimmter Krebszellen, der über kontrollierten Zelltod wirkt und auch in 3D‑Tumormodellen wirksam bleibt. Obwohl dieses Molekül weit davon entfernt ist, ein Arzneimittel zu sein, und noch nicht in Tieren oder Menschen getestet wurde, liefert es einen klar definierten Ausgangspunkt für die Entwicklung besserer Analoga und für die Erforschung, wie selenbasierte Chemie künftig in der Antikrebstherapie genutzt werden kann.
Zitation: Vaskevych, A., Maciejewska, N., Mysiak, A. et al. Access to β-acetoxyselenides, perhydroindolones and anticancer piperidinones via blue LED-driven selenylation of unsaturated carboxamides. Sci Rep 16, 14963 (2026). https://doi.org/10.1038/s41598-026-44112-4
Schlüsselwörter: Organoselen‑Chemie, blaue LED‑Selenylierung, Piperidinon Antikrebs, Apoptose in Krebszellen, 3D Tumor‑Sphäroide