Clear Sky Science · pl
Dostęp do β-acetoksyselenidów, perhydroindolonów i piperydinonów przeciwnowotworowych przez selenylację nienasyconych karboksamidów napędzaną niebieskimi diodami LED
Chemia napędzana światłem na rzecz przyszłych leków przeciwnowotworowych
Chemicy i biolodzy połączyli siły, by przy użyciu prostego niebieskiego światła LED zbudować nowe związki zawierające selen, które wykazują obiecujące właściwości jako przyszłe kandydaty na leki przeciwnowotworowe. Poprzez dopracowanie tej reakcji napędzanej światłem potrafią nakierować te same materiały wyjściowe na bardzo różne produkty, a następnie testować, które z nich najskuteczniej hamują wzrost komórek nowotworowych w laboratorium.
Naświetlanie nowych cząsteczek niebieskim światłem
Badanie koncentruje się na rodzinie związków organicznych zwanych karboksamidami, które można uznać za elastyczne „kręgosłupy” łatwe do modyfikacji. Badacze wystawili te substraty na działanie niebieskiego światła LED w obecności reagentów zawierających selen oraz powszechnych kwasów, takich jak kwas octowy i mrówkowy. Zamiast stosować ostre warunki lub toksyczne dodatki, reakcje przebiegały na powietrzu i opierały się na świetle widzialnym, co czyni je względnie łagodnymi i prostymi do przeprowadzenia. Poprzez zmianę typu amidu i rozpuszczalnika zespół odkrył, że te same składniki można skierować do tworzenia różnych produktów, od łańcuchów otwartych po zwarte struktury pierścieniowe.
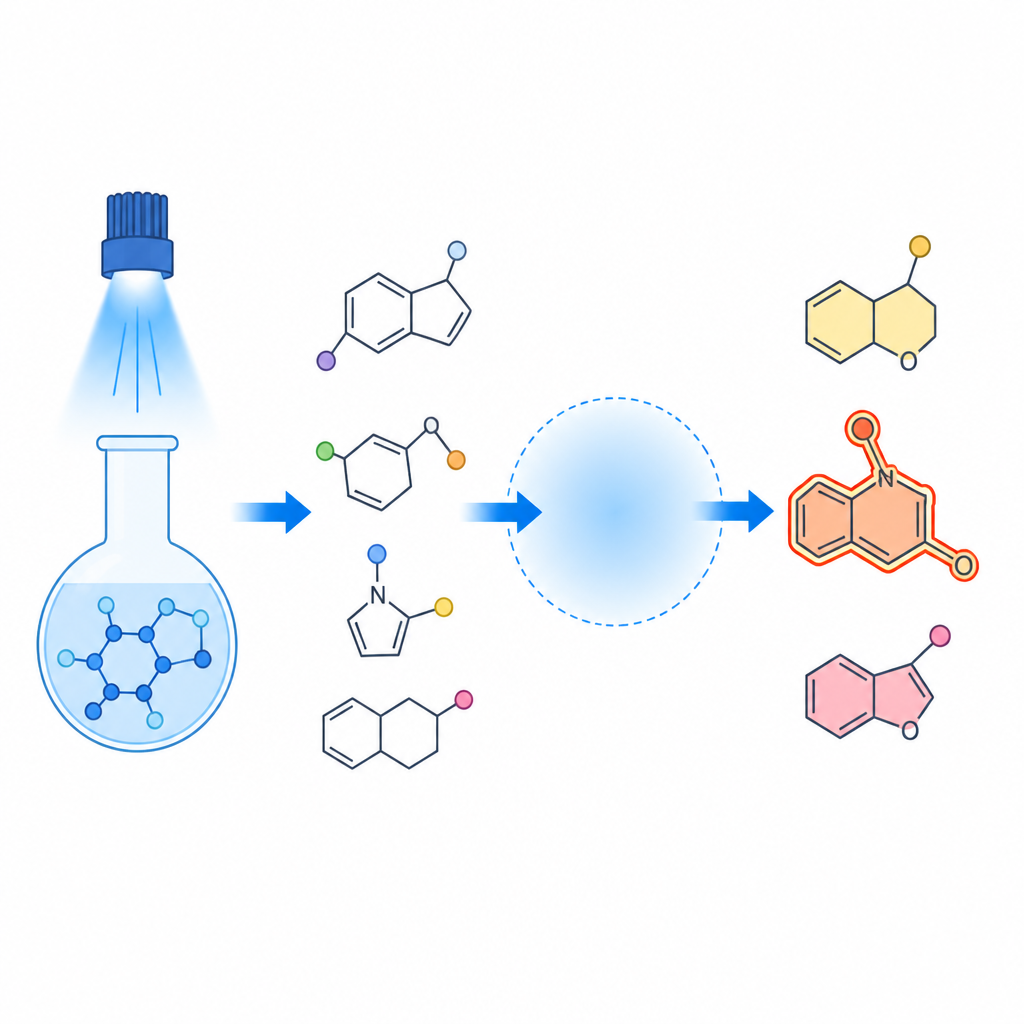
Kierowanie reakcji jak ruchem drogowym
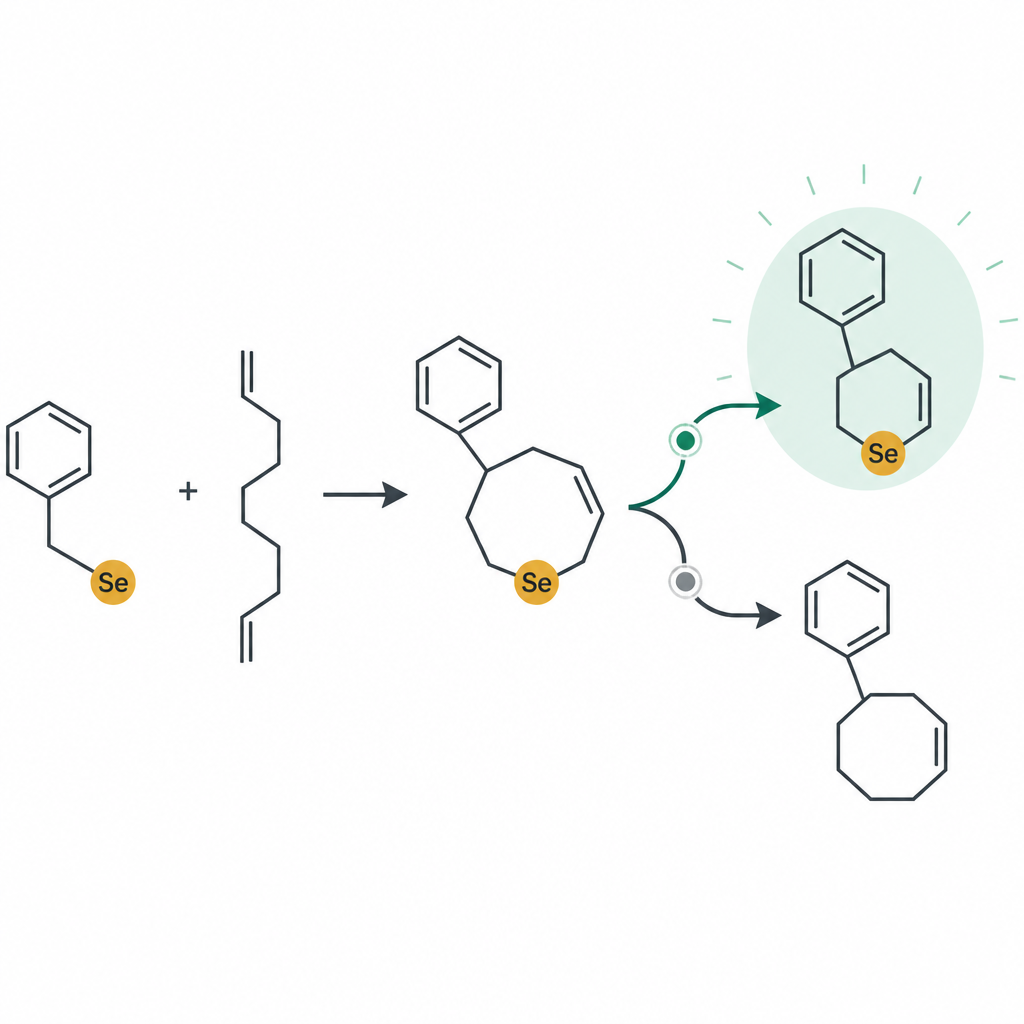
Kluczowym wnioskiem pracy jest to, że reakcja zachowuje się jak mała sieć ruchu drogowego na poziomie atomowym. Gdy niebieskie światło pada na reagent selenu, rozpada się on, generując wysoce reaktywne fragmenty, które szybko addycjonują do podwójnego wiązania węgiel–węgiel w amidzie wyjściowym. Co stanie się dalej, zależy od „otoczenia” wokół tego wiązania: natury grupy bocznej przy azocie, siły i rodzaju kwasu oraz tego, czy obecne są określone sole. W niektórych przypadkach kwas pomaga wstawieniu grupy octanowej, dając trzyskładnikowe produkty znane jako β-acetoksyselenidy. W innych sytuacjach amid zaginając się „gryzie własny ogon”, zamyka się w pierścienie pięcio- lub sześcioczłonowe znane jako perhydroindolony i piperydinony, przenosząc przy tym atom selenu w określonej pozycji.
Jak tlen i subtelne siły kształtują wynik
Zespół zbadał, jak ta reakcja napędzana światłem rzeczywiście przebiega, powtarzając doświadczenia w różnych warunkach. Gdy usunęli tlen z mieszaniny, proces zatrzymał się, co pokazuje, że powietrze odgrywa zasadniczą rolę w aktywacji reagentu selenu. Dodanie powszechnej pułapki na rodniki nie zatrzymało powstawania produktów, co sugeruje, że zaledwie pierwszy krok obejmuje krótkotrwałe gatunki rodnikowe, zanim układ ustabilizuje się w bardziej uporządkowanym procesie jonowym. Równowaga między różnymi produktami okazała się wysoce czuła na niewielkie zmiany. Silniejszy kwas przesuwał reakcję z zamknięcia zależnego od tlenu w stronę formowania pierścienia zależnego od azotu, podczas gdy sól zawierająca słabo oddziałującą anionę pomagała skierować oporne substraty do tworzenia sześcioczłonowych laktonów (laktamów). Razem te testy doprowadziły do szczegółowej propozycji, jak reakcja przebiega przez naładowane pośredniki i dlaczego pewne ścieżki są preferowane.
Z probówki do komórek nowotworowych
Wśród wielu piperydinonów zawierających selen jeden związek, oznaczony jako 12ea, wyróżnił się w testach biologicznych. Badacze wystawili kilka ludzkich linii komórek nowotworowych, w tym komórki raka szyjki macicy i jelita grubego, na rosnące stężenia każdego związku i mierzyli, jak silnie hamują one wzrost komórek. Związek 12ea hamował wzrost w niskich stężeniach mikro-molowych w wielu liniach nowotworowych, wpływając słabiej na normalne fibroblasty płucne, co sugeruje pewien stopień selektywności. Dalsze eksperymenty wykazały, że traktowane komórki nowotworowe nie ginęły po prostu wskutek niekontrolowanego uszkodzenia; zamiast tego przechodziły zaprogramowaną śmierć komórkową, czyli apoptozę. Markerami tego procesu była aktywacja enzymów egzekucyjnych zwanych kaspazami, zmiany właściwości błony wykryte przez sondy fluorescencyjne oraz powstawanie ognisk uszkodzeń DNA w jądrach komórkowych.
Testy w trójwymiarowych skupiskach przypominających guzy
Aby lepiej odzwierciedlić prawdziwe guzy, zespół hodował komórki nowotworowe jako trójwymiarowe sfyroidy, czyli zwarte skupiska odtwarzające niektóre gradienty tlenu i składników odżywczych spotykane w organizmie. Gdy te sfyroidy były traktowane wiodącym związkiem 12ea, ich wzrost znacznie się spowolnił, a skupiska stały się mniejsze i mniej gęste w ciągu kilku dni. Barwienie fluorescencyjne ujawniło silne sygnały apoptozy w całych sfyroidach przy wyższych dawkach, pokazując, że związek może przenikać i pozostawać aktywny w bardziej realistycznym, przypominającym guz środowisku. To istotne, ponieważ wiele leków skutecznych na płaskich monowarstwach komórkowych traci dużą część swojej efektywności w modelach 3D.
Co to może znaczyć dla przyszłych terapii
Podsumowując, badanie przekazuje dwa główne komunikaty dla osób niebędących specjalistami. Po pierwsze, pokazuje, że proste niebieskie światło LED i rozważny dobór warunków pozwalają chemikom precyzyjnie kontrolować sposób, w jaki cząsteczki się składają, umożliwiając budowę złożonych pierścieni zawierających selen w czyściejszy i bardziej zrównoważony sposób. Po drugie, identyfikuje jeden z tych produktów, związek 12ea, jako selektywnego i silnego zabójcę niektórych komórek nowotworowych działającego poprzez kontrolowaną śmierć komórkową i pozostającego skutecznym w modelach guza 3D. Choć ta cząsteczka jest daleka od stania się lekiem i nie była jeszcze testowana na zwierzętach ani ludziach, stanowi dobrze zdefiniowany punkt wyjścia do projektowania lepszych analogów i badania, jak chemia selenu może być wykorzystana w przyszłych terapiach przeciwnowotworowych.
Cytowanie: Vaskevych, A., Maciejewska, N., Mysiak, A. et al. Access to β-acetoxyselenides, perhydroindolones and anticancer piperidinones via blue LED-driven selenylation of unsaturated carboxamides. Sci Rep 16, 14963 (2026). https://doi.org/10.1038/s41598-026-44112-4
Słowa kluczowe: chemia organoselenu, selenylacja za pomocą niebieskich diod LED, piperydinon przeciwnowotworowy, apoptoza w komórkach nowotworowych, guzowe sfyroidy 3D