Clear Sky Science · he
גישה ל-β-אצטוקסיסלנידים, פריהדרואינדולונים ופיפרידינונים אנטי‑סרטניים באמצעות סלנילציה מונעת LED כחול של קרבואמידים בלתי־רוויים
כימיה מונעת אור לעתיד תרופות נגד סרטן
כימאים וביולוגים חברו יחד כדי לנצל אור LED כחול פשוט לבניית מולקולות חדשות מבוססות סלניום שמראות הבטחה כמועמדות לתרופות עתידיות נגד סרטן. באמצעות כוונון עדין של הכימיה המונעת אור הזו, הם יכולים להוביל את אותם חומרי מוצא למוצרים שונים מאוד ואז לבדוק אילו מהם מאטים בצורה היעילה ביותר את גדילת תאים סרטניים במעבדה.
מכוונים אור כחול לעבר מולקולות חדשות
המחקר מתמקד במשפחת מולקולות אורגניות הנקראות קרבואמידים, שניתן לתארן כ"עמודים" גמישים שקל לשנות. החוקרים חשפו חומרי מוצא אלה לאור LED כחול בנוכחות מגיבים המכילים סלניום וחומצות נפוצות כגון חומצה אצטית וחומצה פורמית. במקום להשתמש בתנאים קשים או בתוספים רעילים, התגובות מתנהלות באוויר ותלויות באור הנראה, מה שהופך אותן לפשרות יחסית עדינות וישימות. על ידי שינוי סוג האמיד והמסיסה, הצוות גילה כי ניתן לעודד את אותם מרכיבים להיווצר למוצרים שונים, מטבעות פתוחות ועד מבנים טבעתיים קומפקטיים.
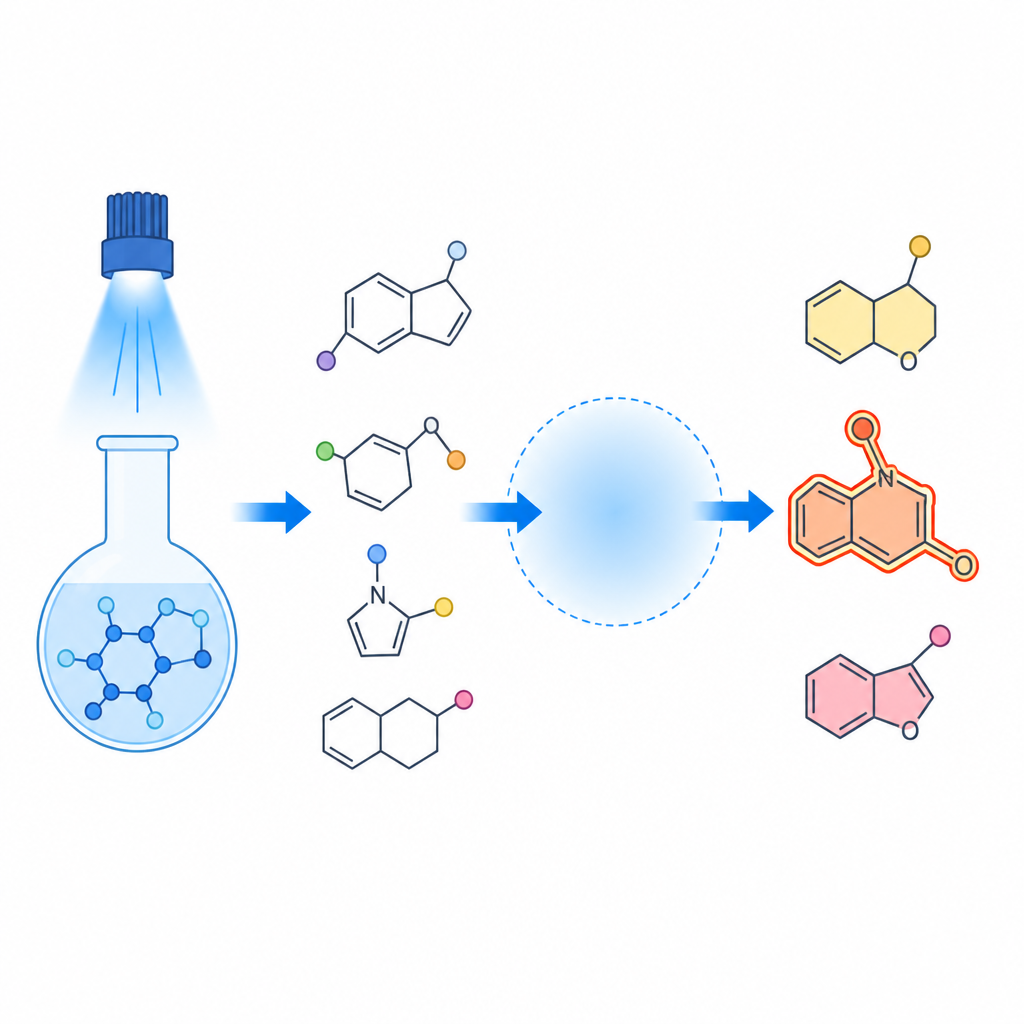
מכוונים תגובות כמו תנועה בכביש
תובנה מרכזית בעבודה היא שהתגובה מתנהגת כמו רשת תנועה קטנה ברמה האטומית. כאשר אור כחול פוגע במגיב הסלניום, הוא מתפרק ומייצר שברים רעילים מאוד שנצמדים במהירות לקשר כפול פחמן–פחמן באמיד המוצא. מה שקורה בהמשך תלוי ב"הסביבה" סביב הקשר הזה: טבעת קבוצת הצד על החנקן, חוזק וסוג החומצה, והאם קיימים מלחים מסוימים. במקרים מסוימים החומצה מסייעת לקבוצת אצטט להיכנס, ולגרום להיווצרות מוצרים תלת־רכיביים הידועים כ-β‑אצטוקסיסלנידים. במצבים אחרים האמיד מתכופף ונחסם על עצמו, סוגר לטבעות של חמש או שש אטומים הידועות כפריהדרואינדולונים ופיפרידינונים, תוך שהוא נושא אטום סלניום במיקום מוגדר.
כיצד חמצן וכוחות עדינים מעצבים את התוצאה
הצוות חקר כיצד הכימיה המונעת אור עובדת על ידי חזרה על התגובות בתנאים שונים. כאשר הסירו חמצן מהתערובת, התהליך נעצר, מה שמראה שלאוויר יש תפקיד חיוני בהפעלת מגיב הסלניום. הוספת מלכודת רדיקלים נפוצה לא עצרה את יצירת המוצר, מה שמרמז שרק הצעד הראשון מעורב בו סוגי רדיקלים קצרים לפני שהמערכת מתייצבת לתהליך יוני מסודר יותר. האיזון בין המוצרים השונים התגלה כרגיש מאוד לשינויים קטנים. חומצה חזקה יותר העבירה את התגובה הרחק מסגירה מבוססת חמצן ולקראת היווצרות טבעת מבוססת חנקן, בעוד שמלח המכיל אניון עם אינטראקציה חלשה סייע לדחוף מצעי תגובה עקשנים ליצור טבעות לקטאם שישיות. יחד, ניסויים אלה הובילו להצעה מפורטת כיצד התגובה מתקדמת דרך בינוניים טעונים ומדוע נתיבים מסוימים מועדפים.
מצבחון לתאי סרטן
מבין פיפרידינונים רבים המכילים סלניום שהופקו, אחד מהתרכובות, המסומן 12ea, בלט במבחנים ביולוגיים. החוקרים חשפו מספר קווי תאים סרטניים אנושיים, כולל תאי סרטן צוואר הרחם ומעי גס, לכמויות גדלות של כל תרכובת ומדדו עד כמה חזק הן צמצמו את הגדילה. תרכובת 12ea עיכבה גדילה בריכוזים מיקרומולריים נמוכים במספר קווי סרטן תוך שהשפיעה פחות על פיברובלסטים רגילים של ריאה, דבר שמרמז על מידה מסוימת של סלקטיביות. ניסויים המשך הראו שהתאים המטופלים לא מתו פשוט מנזק בלתי מבוקר; במקום זאת עברו מוות תאי מתוכנת, או אפופטוזיס. סימני התהליך כללו הפעלת אנזימים מבצעים הנקראים קספזות, שינויים במאפייני ממברנה שנתגלו בעזרת חיישנים פלואורסצנטיים, והיווצרות מוקדי נזק DNA בתוך גרעיני התאים.
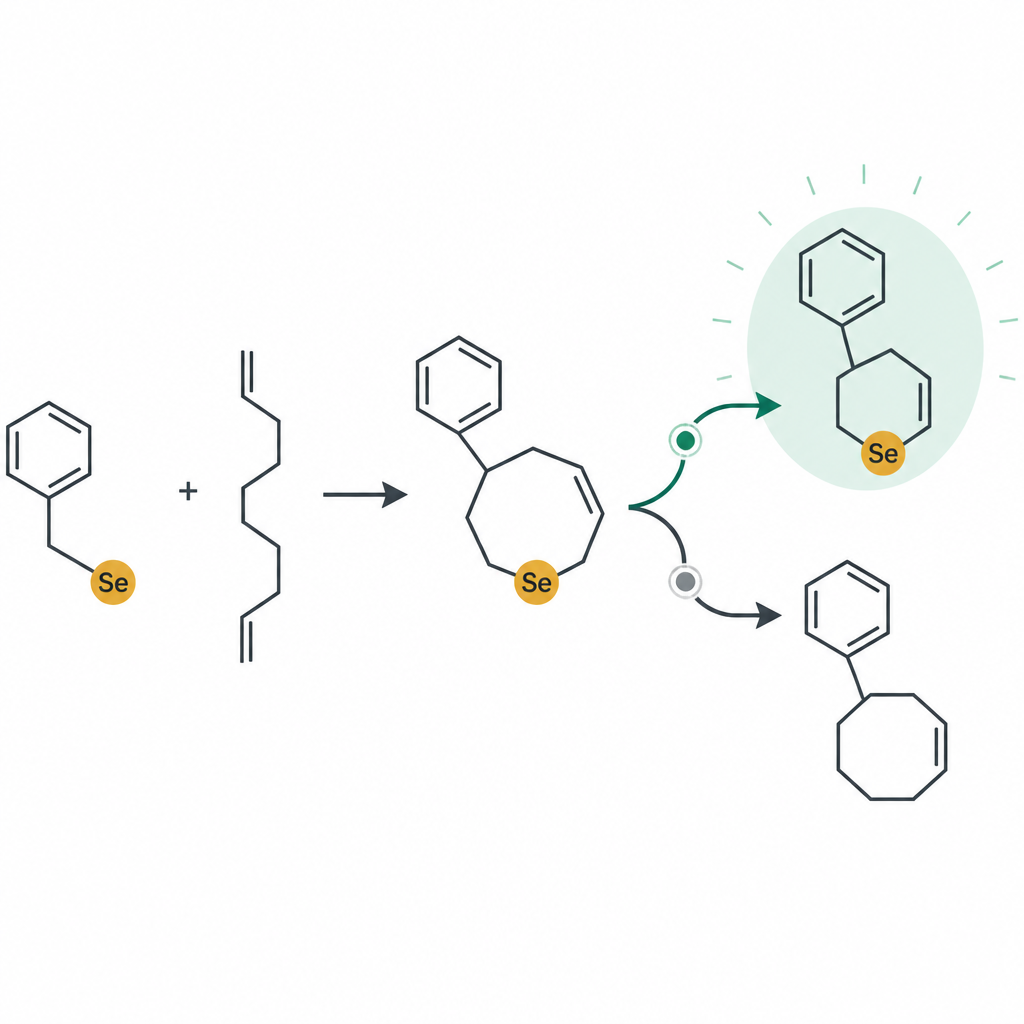
מבחנים בצברי גידול תלת־ממדיים
כדי לדמות טוב יותר גידולים אמיתיים, הצוות גידל את התאים הסרטניים כספירות תלת־ממדיות, שהן צברים קומפקטיים המשחזרים חלק מתבניות החמצן והנוטריינטים בגוף. כאשר טיפלו בספירות אלה עם תרכובת המוביל 12ea, גדילתם האטה משמעותית והצברים הפכו לקטנים ופחות צפופים לאורך מספר ימים. צביעה פלואורסצנטית חשפה אותות חזקים של מוות תאי אפופטוטי בכל רחבי הספירות במינונים גבוהים יותר, מה שמראה כי התרכובת יכולה לחדור ולהישאר פעילה בסביבה המדומה יותר של גידול. זה חשוב, כי תרופות רבות שעובדות היטב על שכבות תאים שטוחות מאבדות חלק גדול מהאפקט במודלים תלת־ממדיים.
מה זה עשוי לומר לגבי טיפולים עתידיים
בסך הכל, המחקר מעביר שתי מסריות עיקריות לקהל שאינו מומחה. ראשית, הוא מדגים שאור LED כחול פשוט ובחירה מושכלת של תנאים יכולים לתת לכימאים שליטה עדינה על אופן הרכבת המולקולות, ולאפשר בנייה של טבעות מורכבות המכילות סלניום בצורה נקייה וברת‑קיימא יותר. שנית, הוא מזהה אחד מהמוצרים הללו, תרכובת 12ea, כקטלנית סלקטיבית וחזקה של סוגים מסוימים של תאים סרטניים הפועלת דרך מוות תאי מבוקר ונשארה אפקטיבית במודלים תלת‑ממדיים של גידול. אף שעדיין הדרך ארוכה לפני שהמולקולה הזו תהפוך לתרופה ולא נבדקה עדיין בבעלי חיים או באנשים, היא מספקת נקודת מוצא מוגדרת היטב לעיצוב אנלוגים טובים יותר ולחקור כיצד ניתן לרתום כימיית סלניום לטיפולים אנטי‑סרטניים עתידיים.
ציטוט: Vaskevych, A., Maciejewska, N., Mysiak, A. et al. Access to β-acetoxyselenides, perhydroindolones and anticancer piperidinones via blue LED-driven selenylation of unsaturated carboxamides. Sci Rep 16, 14963 (2026). https://doi.org/10.1038/s41598-026-44112-4
מילות מפתח: כימיית אורגנוסלניום, סלנילציה ב-LED כחול, פיפרידינון אנטי‑סרטן, אפופטוזיס בתאים סרטניים, ספירות גידול בתלת־ממד