Clear Sky Science · ru
Доступ к β-ацетоксиселенидам, пергидроиндолонам и антираковым пиперидинонам через селенилирование ненасыщенных карбоксамидов под действием синих светодиодов
Химия на свету для будущих противораковых препаратов
Химики и биологи объединили усилия, чтобы с помощью простого синего светодиода синтезировать новые молекулы на основе селена, которые выглядят перспективными как будущие противораковые кандидаты. Тонко настраивая эту фотоинициируемую химию, они умеют направлять одни и те же стартовые материалы на получение различных продуктов и затем проверять, какие из них наиболее эффективно замедляют рост опухолевых клеток в лаборатории.
Освещая новые молекулы синим светом
В основе исследования — семейство органических молекул, называемых карбоксама́ми, которые можно рассматривать как гибкие «основы», легко поддающиеся модификации. Исследователи подвергали эти стартовые субстраты действию синего светодиода в присутствии селенсодержащих реагентов и обычных кислот, таких как уксусная и муравьиная. Вместо использования жестких условий или токсичных добавок реакции протекали на воздухе и опирались на видимый свет, что делает их относительно мягкими и простыми в выполнении. Меняя тип амидной группы и растворитель, команда обнаружила, что те же ингредиенты можно «склонить» к образованию различных продуктов — от разомкнутых молекул до компактных кольцевых структур.
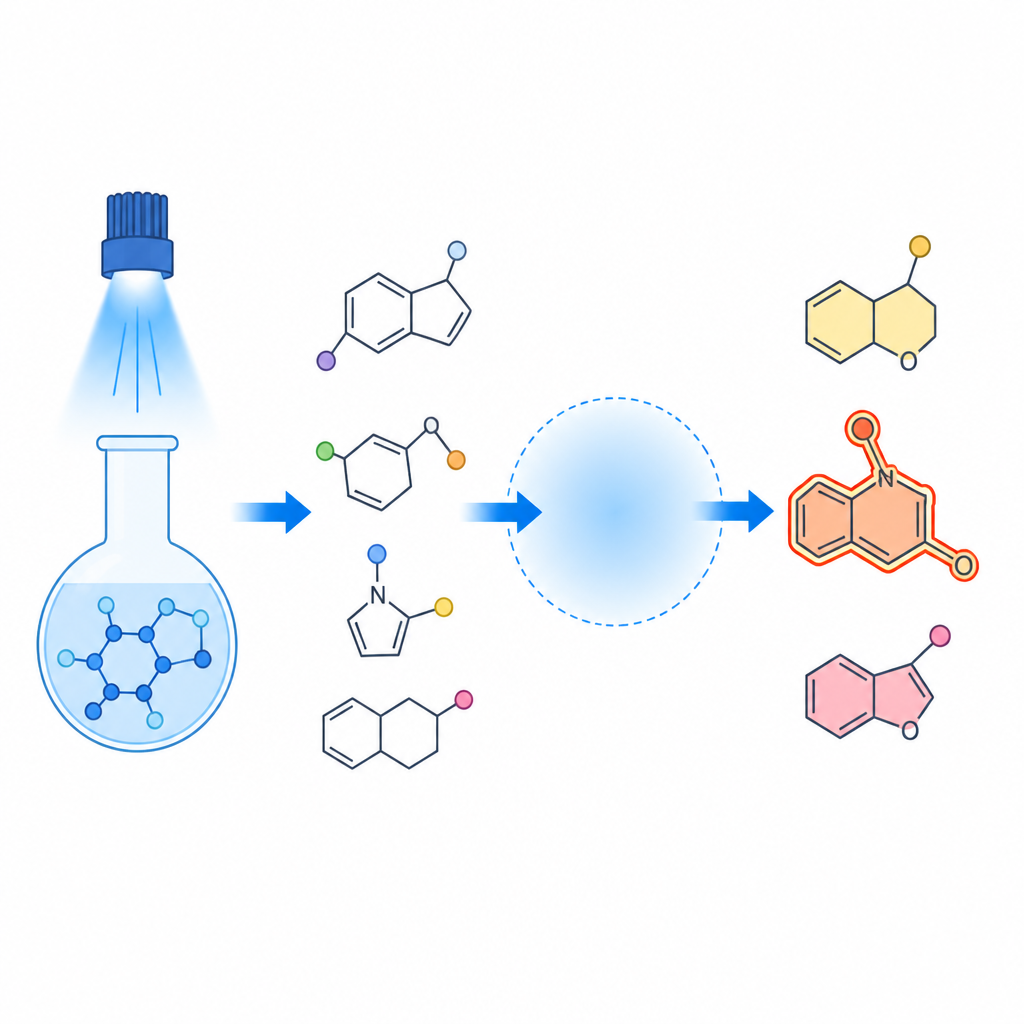
Направляя реакции как дорожное движение
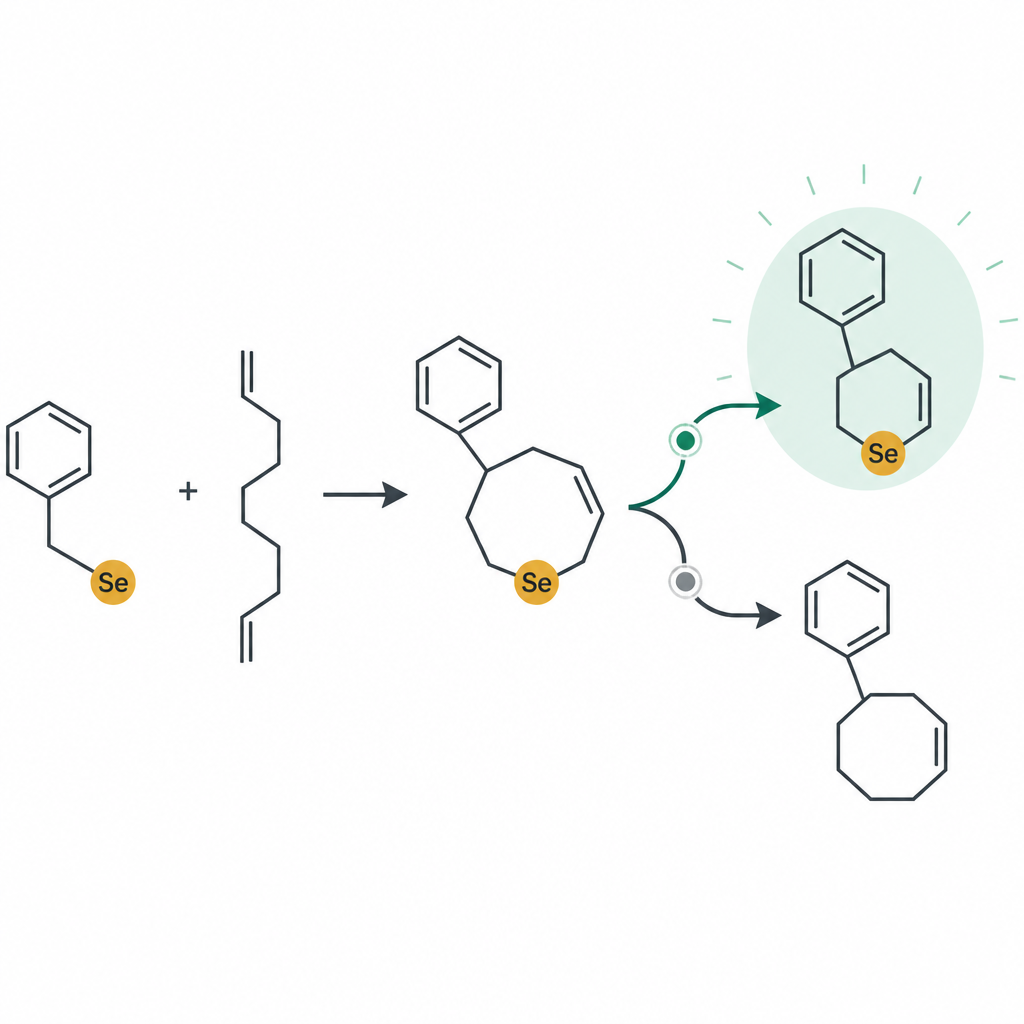
Ключевая идея работы — представить реакцию как небольшую сеть движения на атомном уровне. Когда синий свет попадает на селеновый реагент, он фоторезонансно распадается и генерирует высокореактивные фрагменты, которые быстро присоединяются к двойной связи углерод–углерод в исходном амиде. Дальнейший ход событий зависит от «окружения» вокруг этой связи: природы азотной боковой группы, силы и типа кислоты и наличия определённых солей. В одних случаях кислота помогает ацетатной группе вмешаться, давая трёхкомпонентные продукты, известные как β-ацетоксиселениды. В других ситуациях амид «сгибается» и замыкается сам на себя, образуя пяти- или шестичленные кольца — пергидроиндолоны и пиперидиноны — с атомом селена в определённом положении.
Как кислород и тонкие силы формируют исход
Команда исследовала механистику этой фотоинициируемой химии, повторяя реакции в разных условиях. При удалении кислорода процесс останавливался, что показывает существенную роль воздуха в активации селенового реагента. Добавление обычного ловителя радикалов не остановило образование продукта, что указывает на то, что только самый первый шаг включает кратковременные радикальные частицы, после чего система переходит в более упорядоченный ионный механизм. Баланс между различными продуктами оказался очень чувствителен к небольшим изменениям. Более сильная кислота сместила ход реакции от замыкания с участием кислорода в сторону образования азотсодержащих колец, тогда как соль с слабо взаимодействующим анионом помогла «заставить» упорные субстраты образовать шестичленные лактамы. В совокупности эти тесты привели к подробному предложению о том, как реакция проходит через заряженные интермедиаты и почему те или иные пути оказываются предпочтительными.
Из пробирки в раковые клетки
Среди множества селенсодержащих пиперидинонов одно соединение, обозначенное как 12ea, выделилось в биологических испытаниях. Исследователи подвергли несколько человеческих раковых линий, включая клетки шейки матки и толстой кишки, дозированию разными концентрациями каждого соединения и измеряли, насколько сильно они подавляют рост. Соединение 12ea ингибировало рост при низких микромолярных концентрациях в нескольких опухолевых линиях, при этом менее сильно воздействуя на нормальные лёгочные фибробласты, что говорит о некоторой степени селективности. Последующие эксперименты показали, что обработанные раковые клетки умирали не в результате неконтролируемого разрушения, а через программируемую гибель — апоптоз. Маркерами этого процесса были активация каспаз-исполнителей, изменения мембранных признаков, выявляемые флуоресцентными зондами, и образование очагов повреждения ДНК в ядрах клеток.
Испытания в 3D-кластерных моделях опухолей
Чтобы лучше имитировать настоящие опухоли, команда выращивала раковые клетки в виде трёхмерных сфероидов — компактных кластеров, воспроизводящих некоторые градиенты кислорода и питательных веществ, встречающиеся в организме. При обработке этих сфероидов лидирующим соединением 12ea их рост резко замедлялся, кластеры становились меньше и менее плотными в течение нескольких дней. Флуоресцентное окрашивание показало сильные сигналы апоптоза по всему объёму сфероидов при более высоких дозах, демонстрируя, что соединение способно проникать и оставаться активным в более реалистичной опухолевой среде. Это важно, поскольку многие препараты, эффективные на плоских клеточных монослоях, сильно теряют свою активность в 3D-моделях.
Что это может значить для будущего лечения
В целом исследование даёт два основных посыла для неспециалистов. Во‑первых, оно показывает, что простой синий светодиод и продуманное сочетание условий дают химикам тонкий контроль над сборкой молекул, позволяя строить сложные селенсодержащие кольца более чисто и устойчиво. Во‑вторых, оно выделяет одно из этих соединений, 12ea, как селективный и мощный убийцу некоторых раковых клеток, действующий через контролируемую клеточную гибель и сохраняющий активность в 3D-моделях опухолей. Хотя это соединение далеко от статуса лекарства и пока не тестировалось на животных или людях, оно предоставляет чётко определённую отправную точку для разработки улучшенных аналогов и изучения того, как органоселеновая химия может быть использована в будущих противораковых терапиях.
Цитирование: Vaskevych, A., Maciejewska, N., Mysiak, A. et al. Access to β-acetoxyselenides, perhydroindolones and anticancer piperidinones via blue LED-driven selenylation of unsaturated carboxamides. Sci Rep 16, 14963 (2026). https://doi.org/10.1038/s41598-026-44112-4
Ключевые слова: органоселеновая химия, селенилирование синим светодиодом, пиперидинон антираковый, апоптоз в раковых клетках, 3D опухолевые сфероиды