Clear Sky Science · sv
Tillgång till β-acetoxyselenider, perhydroindoloner och anticancera piperidinoner via blå LED‑driven selenylering av omättade karboxamider
Ljusdriven kemi för framtida cancerläkemedel
Kemister och biologer har samarbetat för att använda enkelt blått LED‑ljus för att bygga nya selenbaserade molekyler som visar löfte som framtida anticancer‑kandidater. Genom att finjustera denna ljusdrivna kemi kan de styra samma utgångsmaterial mot mycket olika produkter och därefter testa vilka som mest effektivt bromsar tillväxten av cancerceller i laboratoriet.
Lyser blått ljus på nya molekyler
Studien fokuserar på en familj organiska molekyler kallade karboxamider, som kan ses som flexibla ”ryggrader” som är lätta att modifiera. Forskarna utsatte dessa utgångsmaterial för blått LED‑ljus i närvaro av seleninnehållande reagenser och vanliga syror som ättiksyra och myrsyra. Istället för att använda hårda förhållanden eller giftiga tillsatser körs reaktionerna i luft och förlitar sig på synligt ljus, vilket gör dem relativt milda och enkla att utföra. Genom att justera typen av amid och lösningsmedlet upptäckte teamet att samma ingredienser kunde lockas att bilda olika produkter, allt från öppna kedjemolekyler till kompakta ringformade strukturer.
Styr reaktioner som trafik
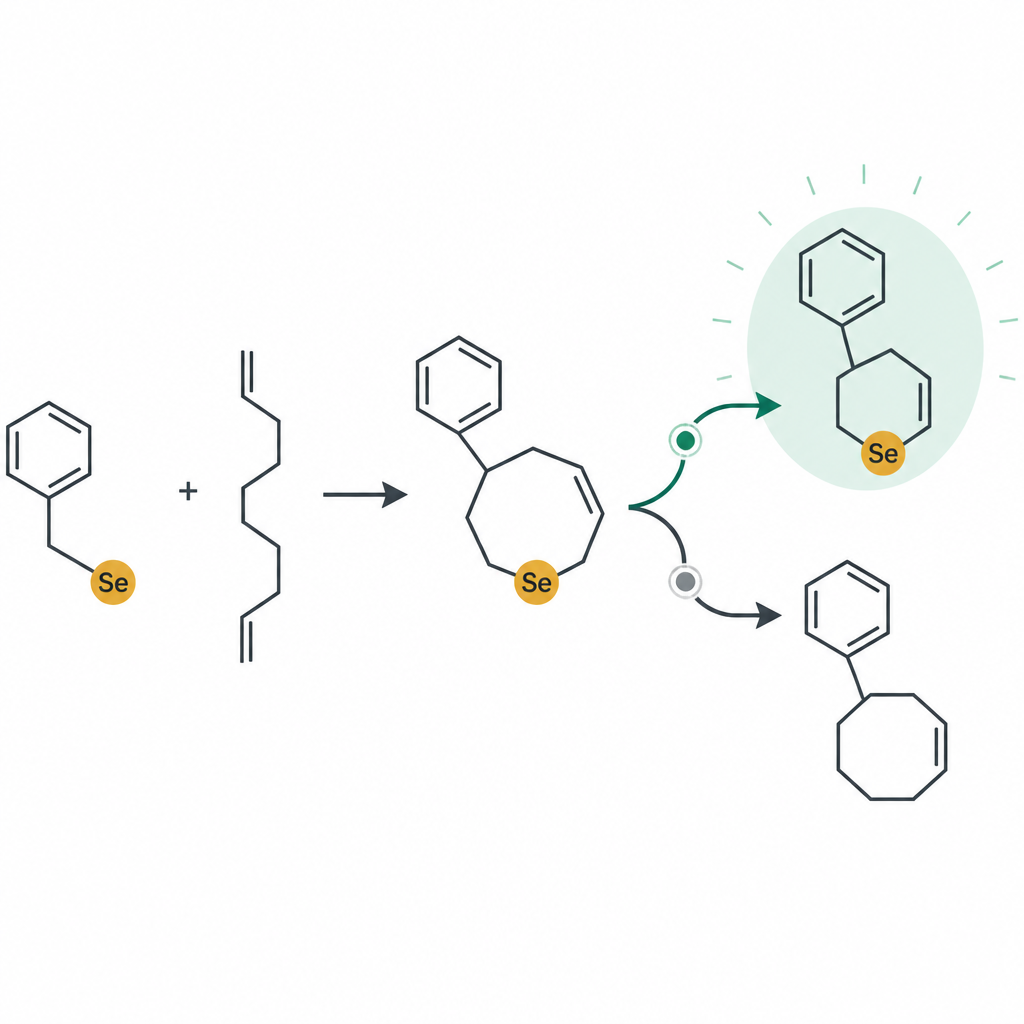
En viktig insikt i arbetet är att reaktionen beter sig som ett litet trafiknät på atomnivå. När blått ljus träffar selenreagenset splittras det och genererar mycket reaktiva fragment som snabbt adderar till kol‑kol‑dubbelbindningen i startamid. Vad som händer därefter beror på ”miljön” runt den bindningen: arten av kvävesidogruppen, syrans styrka och typ, och om vissa salter är närvarande. I vissa fall hjälper syran en acetatgrupp att hoppa in, vilket ger tredelade produkter kända som beta‑acetoxyselenider. I andra situationer böjer sig amiden runt och biter sin egen svans, sluter sig till fem‑ eller sexledade ringar kända som perhydroindoloner och piperidinoner, samtidigt som en selenatom placeras i en definierad position.
Hur syre och subtila krafter formar utfallet
Teamet undersökte hur denna ljusdrivna kemi egentligen fungerar genom att upprepa reaktionerna under olika förhållanden. När de avlägsnade syre från blandningen upphörde processen, vilket visar att luft spelar en väsentlig roll i aktiveringen av selenreagenset. Tillsats av en vanlig radikalfångare stoppade inte produktbildningen, vilket antyder att endast det allra första steget involverar kortlivade radikala arter innan systemet stabiliseras till en mer ordnad jonisk process. Balansen mellan olika produkter visade sig vara mycket känslig för små förändringar. En starkare syra försköt reaktionen bort från syrebaserad slutning och mot kvävebaserad ringbildning, medan ett salt med en svagt interagerande anjon hjälpte envisa substrat att bilda sexledade lakton‑/laktamringar. Tillsammans ledde dessa tester till ett detaljerat förslag för hur reaktionen fortskrider via laddade mellanprodukter och varför vissa vägar prioriteras.
Från provrör till cancerceller
Bland de många seleninnehållande piperidinonerna som producerades stack en förening, märkt 12ea, ut i biologiska tester. Forskarna exponerade flera humana cancercellinjer, inklusive cervix‑ och kolorektalcancerceller, för ökande mängder av varje förening och mätte hur starkt de minskade celltillväxten. Föreningen 12ea hämmande tillväxt vid låga mikromolära koncentrationer i flera cancerlinjer samtidigt som normala lungfibroblaster påverkades svagare, vilket tyder på viss grad av selektivitet. Uppföljande experiment visade att behandlade cancerceller inte helt enkelt dog genom okontrollerad skada; istället genomgick de programmerad celldöd, eller apoptos. Markörer för denna process inkluderade aktivering av exekutiva enzymer kallade kaspaser, förändringar i membranegenskaper upptäckta med fluorescerande prober, och bildning av DNA‑skadefoci inne i cellkärnorna.
Testning i 3D‑tumörlika kluster
För att bättre efterlikna verkliga tumörer odlade teamet cancercellerna som tredimensionella sfäroider, vilka är kompakta kluster som återskapar vissa av de syre‑ och näringsgradienter som finns i kroppen. När dessa sfäroider behandlades med ledföreningen 12ea, bromsades deras tillväxt dramatiskt och klustren blev mindre och mindre täta över flera dagar. Fluorescerande färgning visade starka signaler för apoptotisk celldöd genom hela sfäroiderna vid högre doser, vilket visar att föreningen kan penetrera och förbli aktiv i en mer realistisk tumörliknande miljö. Detta är viktigt, eftersom många läkemedel som fungerar väl på plana cellager tappar mycket av sin effekt i 3D‑modeller.
Vad detta kan innebära för framtida behandlingar
Sammanfattningsvis levererar studien två huvudbudskap för icke‑specialister. För det första demonstrerar den att enkelt blått LED‑ljus och ett väl avvägt val av förhållanden kan ge kemister fin kontroll över hur molekyler sätts ihop, vilket gör det möjligt att bygga komplexa seleninnehållande ringar på ett renare och mer hållbart sätt. För det andra identifierar den en av dessa produkter, föreningen 12ea, som en selektiv och potent dödare av vissa cancerceller som verkar genom kontrollerad celldöd och förblir effektiv i 3D‑tumörmodeller. Även om denna molekyl är långt från att bli ett läkemedel och ännu inte har testats i djur eller människor, utgör den en väl definierad utgångspunkt för att designa bättre analoger och utforska hur selenbaserad kemi kan utnyttjas i framtida anticancerterapier.
Citering: Vaskevych, A., Maciejewska, N., Mysiak, A. et al. Access to β-acetoxyselenides, perhydroindolones and anticancer piperidinones via blue LED-driven selenylation of unsaturated carboxamides. Sci Rep 16, 14963 (2026). https://doi.org/10.1038/s41598-026-44112-4
Nyckelord: organoselenkemi, blå LED‑selenylering, piperidinon anticancer, apoptos i cancerceller, 3D tumörsfäroider