Clear Sky Science · fr
Accès aux β-acétoxyséléniures, pérhydroindolones et pipéridinones anticancéreuses via une sélénylation de carboxamides insaturés activée par LED bleue
La chimie alimentée par la lumière pour les médicaments anticancéreux de demain
Des chimistes et des biologistes ont uni leurs efforts pour utiliser une simple lumière LED bleue afin de construire de nouvelles molécules à base de sélénium qui montrent un potentiel comme candidats médicaments anticancéreux. En réglant finement cette chimie activée par la lumière, ils peuvent orienter les mêmes matières premières vers des produits très différents, puis tester lesquels ralentissent le plus efficacement la croissance des cellules cancéreuses en laboratoire.
Éclairer de la lumière bleue de nouvelles molécules
L’étude porte sur une famille de molécules organiques appelées carboxamides, que l’on peut considérer comme des « ossatures » flexibles faciles à modifier. Les chercheurs ont exposé ces matériaux de départ à une lumière LED bleue en présence de réactifs contenant du sélénium et d’acides courants tels que l’acide acétique et l’acide formique. Plutôt que d’employer des conditions agressives ou des additifs toxiques, les réactions se déroulent en atmosphère d’air et reposent sur la lumière visible, ce qui les rend relativement douces et simples à mettre en œuvre. En ajustant le type d’amide et le solvant, l’équipe a découvert que les mêmes ingrédients pouvaient être amenés à former des produits différents, allant de molécules à chaîne ouverte à des structures compactes en anneau.
Diriger les réactions comme la circulation
Un enseignement clé du travail est que la réaction se comporte comme un petit réseau routier au niveau atomique. Quand la lumière bleue atteint le réactif sélénié, celui‑ci se scinde et génère des fragments hautement réactifs qui se fixent rapidement sur la double liaison carbone–carbone de l’amide de départ. La suite dépend de « l’environnement » autour de cette liaison : la nature du groupe azoté, la force et le type d’acide, et la présence éventuelle de certains sels. Dans certains cas, l’acide facilite l’intervention d’un groupe acétate, donnant des produits à trois composants connus sous le nom de β‑acétoxyséléniures. Dans d’autres situations, l’amide se replie et se ferme sur lui‑même, formant des cycles à cinq ou six membres appelés pérhydroindolones et pipéridinones, tout en portant un atome de sélénium en position définie.
Comment l’oxygène et des forces subtiles orientent le résultat
L’équipe a sondé le fonctionnement réel de cette chimie activée par la lumière en répétant les réactions dans différentes conditions. Lorsqu’ils ont retiré l’oxygène du mélange, le processus s’est arrêté, montrant que l’air joue un rôle essentiel dans l’activation du réactif au sélénium. L’ajout d’un piège à radicaux courant n’a pas interrompu la formation des produits, ce qui suggère que seule la toute première étape implique des espèces radicalaires de courte durée avant que le système ne bascule vers un processus ionique plus ordonné. L’équilibre entre les différents produits s’est révélé très sensible à de petits changements. Un acide plus fort a déplacé la réaction loin de la fermeture impliquant l’oxygène vers la formation de cycles centrés sur l’azote, tandis qu’un sel contenant un anion faiblement interagissant a aidé à pousser des substrats récalcitrants à former des lactames à six membres. Ensemble, ces tests ont conduit à une proposition détaillée de la façon dont la réaction progresse via des intermédiaires chargés et pourquoi certaines voies sont favorisées.
Du tube à essai aux cellules cancéreuses
Parmi les nombreuses pipéridinones contenant du sélénium produites, un composé, nommé 12ea, s’est distingué dans les tests biologiques. Les chercheurs ont exposé plusieurs lignées cellulaires cancéreuses humaines, y compris des cellules du col de l’utérus et du côlon, à des concentrations croissantes de chaque composé et ont mesuré dans quelle mesure elles réduisaient la croissance cellulaire. Le composé 12ea a inhibé la croissance à de faibles concentrations micromolaires dans plusieurs lignées cancéreuses tout en affectant moins fortement des fibroblastes pulmonaires normaux, suggérant un certain degré de sélectivité. Des expériences complémentaires ont montré que les cellules cancéreuses traitées ne mouraient pas simplement par dommages incontrôlés ; elles ont subi une mort cellulaire programmée, ou apoptose. Parmi les marqueurs de ce processus figuraient l’activation d’enzymes exécutrices appelées caspases, des modifications des caractéristiques membranaires détectées par des sondes fluorescentes, et la formation de foyers de dommages à l’ADN à l’intérieur des noyaux cellulaires.
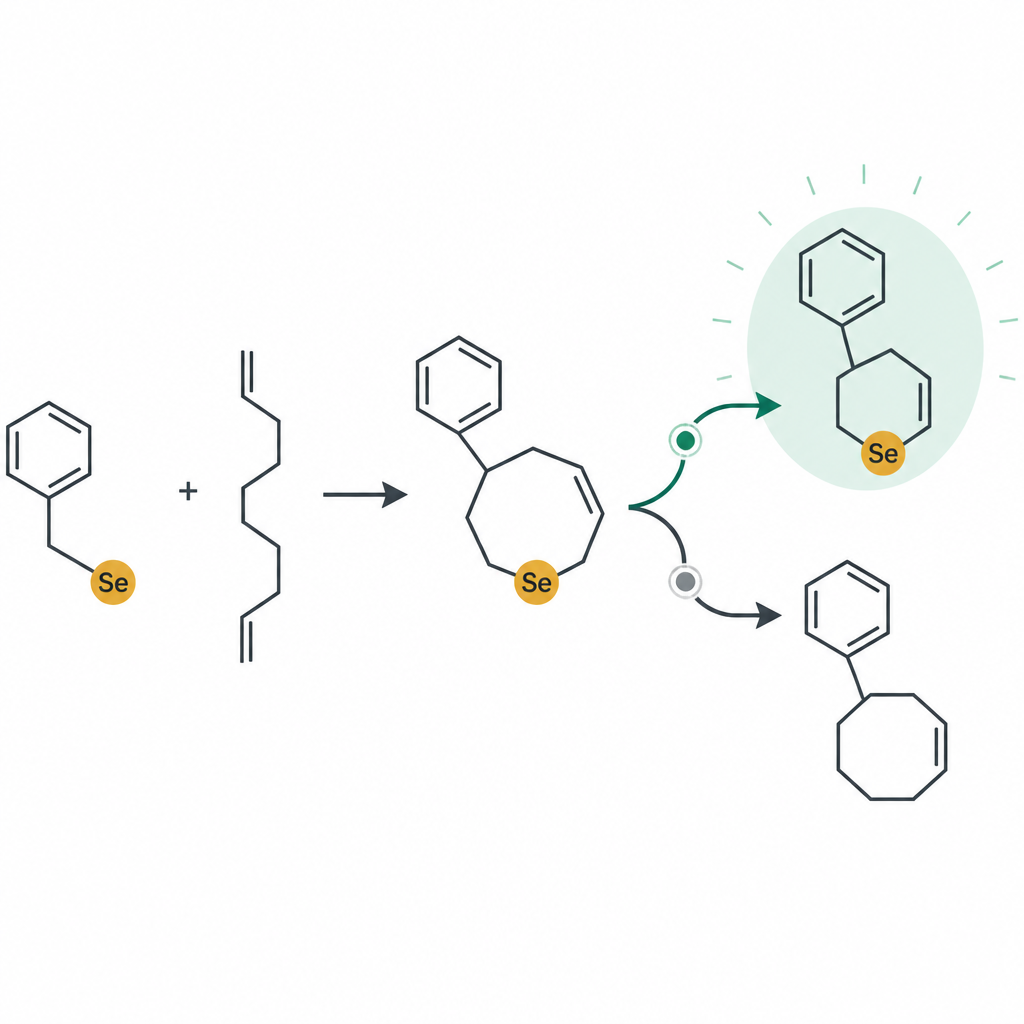
Tests sur des amas tumoraux 3D
Pour mieux imiter les tumeurs réelles, l’équipe a cultivé les cellules cancéreuses sous forme de sphéroïdes tridimensionnels, qui sont des amas compacts reproduisant certains gradients d’oxygène et de nutriments présents dans l’organisme. Lorsque ces sphéroïdes ont été traités avec le composé principal 12ea, leur croissance a fortement ralenti et les amas sont devenus plus petits et moins denses sur plusieurs jours. La coloration fluorescente a révélé des signaux forts d’apoptose à l’intérieur des sphéroïdes à des doses plus élevées, montrant que le composé peut pénétrer et rester actif dans un environnement tumoral plus réaliste. C’est important, car de nombreux médicaments efficaces sur des couches cellulaires plates perdent une grande partie de leur effet dans des modèles 3D.
Ce que cela pourrait signifier pour les traitements futurs
Globalement, l’étude délivre deux messages principaux pour le grand public. Premièrement, elle démontre que de simples LED bleues et un choix judicieux de conditions permettent aux chimistes de contrôler finement l’assemblage moléculaire, leur permettant de construire des cycles complexes contenant du sélénium de manière plus propre et plus durable. Deuxièmement, elle identifie l’un de ces produits, le composé 12ea, comme un tueur sélectif et puissant de certaines cellules cancéreuses agissant par mort cellulaire programmée et restant efficace dans des modèles tumoraux 3D. Bien que cette molécule soit loin d’être un médicament et n’ait pas encore été testée chez l’animal ou l’humain, elle fournit un point de départ bien défini pour concevoir de meilleurs analogues et explorer comment la chimie à base de sélénium peut être exploitée dans de futures thérapies anticancéreuses.
Citation: Vaskevych, A., Maciejewska, N., Mysiak, A. et al. Access to β-acetoxyselenides, perhydroindolones and anticancer piperidinones via blue LED-driven selenylation of unsaturated carboxamides. Sci Rep 16, 14963 (2026). https://doi.org/10.1038/s41598-026-44112-4
Mots-clés: chimie organosélénium, sélénylation par LED bleue, pipéridinone anticancéreuse, apoptose dans les cellules cancéreuses, sphéroïdes tumoraux 3D