Clear Sky Science · zh
犬类退行性脊髓病血液与脊髓中免疫相关改变的分析——一种自发发生的肌萎缩侧索硬化症模型
为什么犬类疾病与人类有关
许多年长犬只,尤其是彭布罗克威尔士柯基,可能会患上一种致命的脊柱疾病,称为退行性脊髓病。该病会逐步剥夺它们行走甚至呼吸的能力。显著的是,它与人类的肌萎缩侧索硬化症(ALS,亦称路易·吉里格病)极为相似。由于犬类会自然发生这种疾病并且与部分ALS患者共享关键基因突变,研究犬只可以在真实环境中揭示神经系统损伤与机体防御之间的相互作用,这些信息是工程化小鼠模型无法全面反映的。
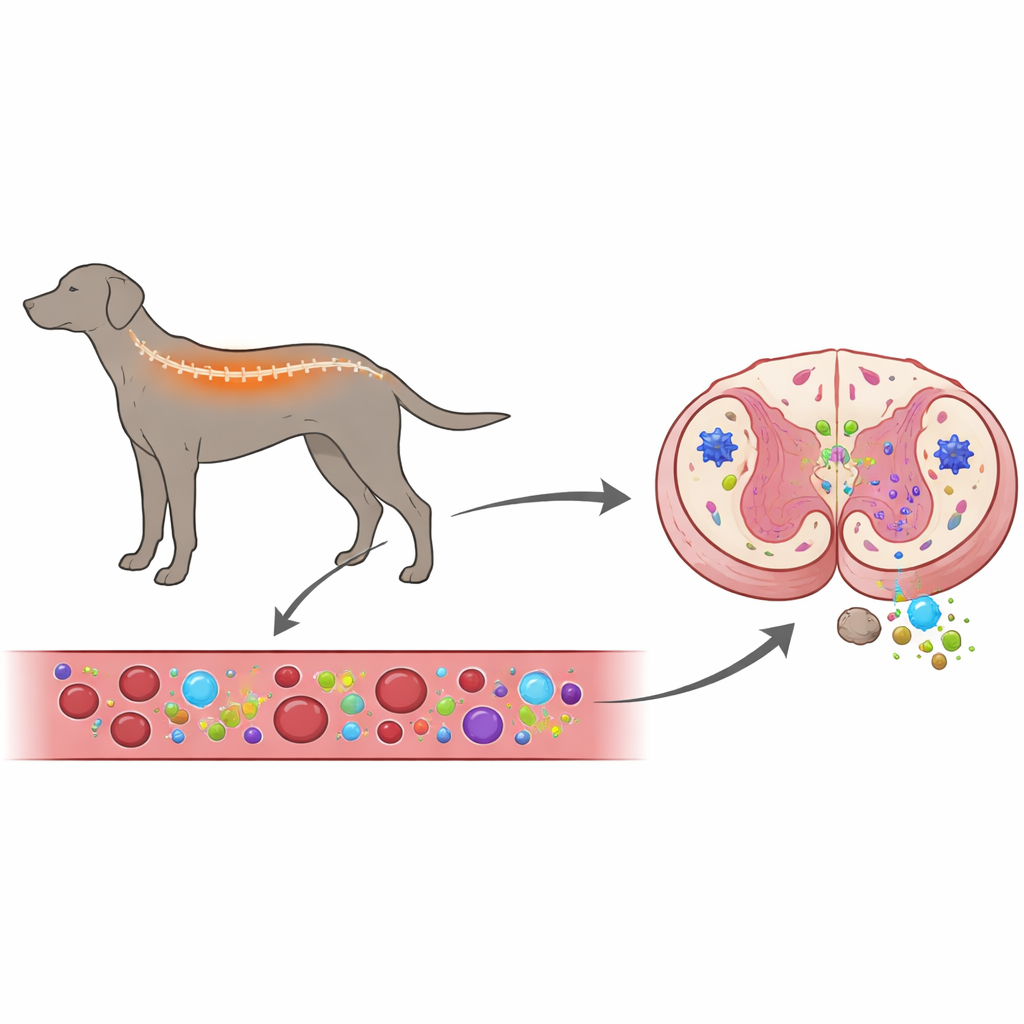
同时审视血液与脊髓
研究者旨在回答一个核心问题:机体免疫系统是在推动犬类该病的发展,还是主要对已经发生的神经损伤作出反应?为此,他们检查了患病犬只的血液与脊髓组织,并将其与健康犬和患有另一种脊柱问题——椎间盘突出(外部压迫脊髓)——的犬只进行比较。他们测量了血细胞与脊髓组织中与炎症相关基因的活性,并使用带荧光的抗体染色来观察脊髓中有哪些免疫细胞与支持细胞存在及其活跃程度。
血液中的免疫警报信号
在患病犬只的血液中,研究团队发现某些白细胞处于“警觉”状态的迹象。一组与炎症信使生成相关的分子报警系统——炎症小体(inflammasome)相关基因的活性高于对照动物。与此同时,一种通常起到抑制炎症作用的免疫“刹车”分子的基因也显示出更高的活性,表明机体在试图将该警报控制住。然而,常规血液检查结果并无异常:白细胞计数和一种常用炎症标志物C反应蛋白仍在典型范围内。这一模式指向一种微妙且受严格调控的免疫激活,而非全身性的大规模炎症爆发。
谁进入脊髓,谁被阻止在外
接下来的问题是,活化的血液细胞是否像某些小鼠ALS模型中那样大量涌入脊髓。研究者使用可区分定居脑内免疫细胞与来自血液的新来者的细胞标记,发现每个受累脊髓横截面中仅有少量可能的外来细胞。换言之,有证据表明部分血源性细胞确实进入了神经组织,但数量非常有限。与此同时,他们在脊髓中观察到一种通常可吸引血流中此类细胞的化学信号的表达增加,表明组织自身在发出求助信号,即便只有少数应答者抵达。
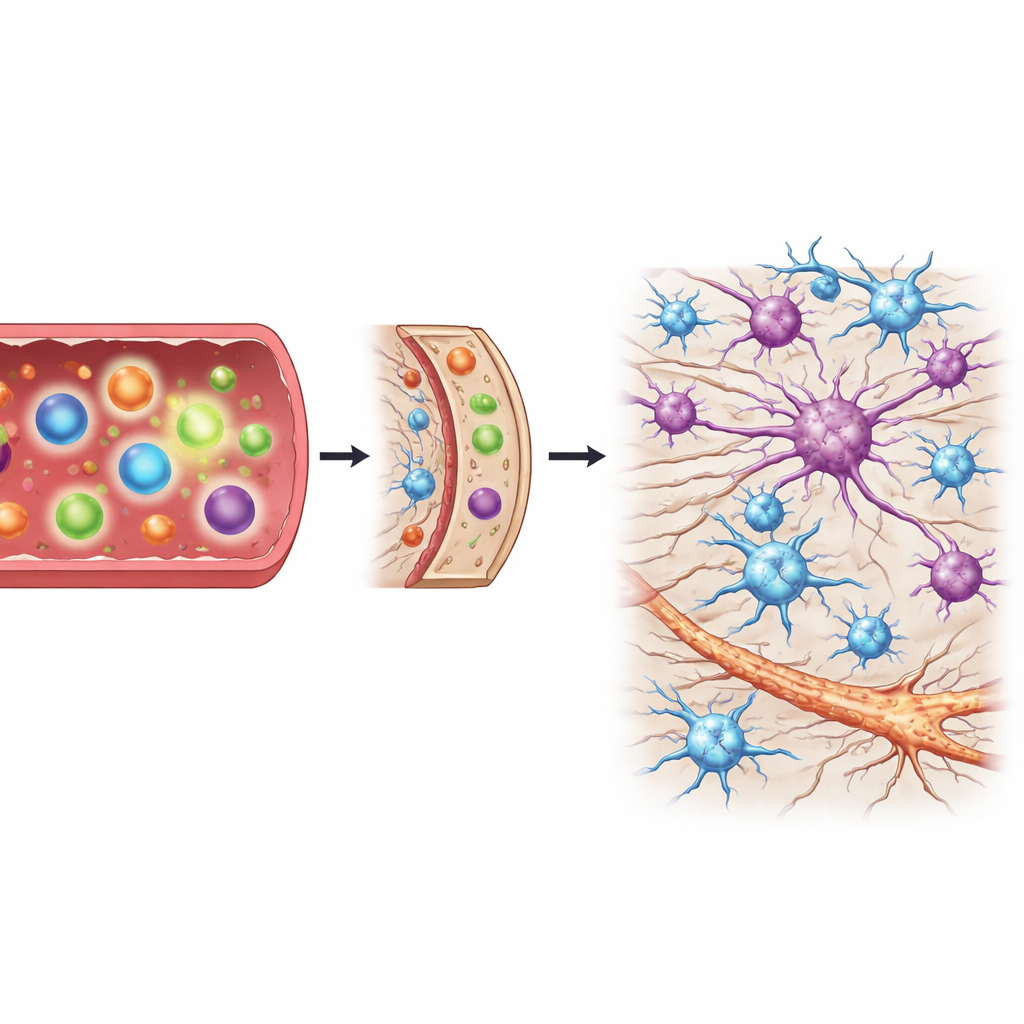
随着损伤加剧,支持细胞的反应
脊髓不仅拥挤着神经纤维,还包含被称为星形胶质细胞和小胶质细胞的支持细胞,它们的状态不同可对神经元起保护或损害作用。通过将脊髓样本按损伤程度分组——从无、轻度、中度到重度——研究团队得以追踪这些支持细胞随时间的变化。随着退化进展,标志有害和保护性星形胶质细胞的基因显著上升,招募免疫细胞的趋化因子也更为活跃。相比之下,小胶质细胞活化的标志在损伤尚轻时并未表现出明显的早期上调。这一时序表明,星形胶质细胞的大规模激活与免疫信号的增强出现在神经损伤已存在之后,而非疾病一开始就出现。
这对犬类和人类意味着什么
综合来看,结果描绘出这样一幅图景:退行性脊髓病涉及一种静默但复杂的免疫转变——血液细胞被“预激”,脊髓发出求助信号,本地支持细胞在损伤积累时强烈反应。然而,来自血液的免疫细胞实际侵入脊髓的情况仍然有限,显著的炎症改变主要出现在晚期。对养犬者而言,这意味着在明显症状出现时,免疫变化更多是对神经丧失的反应,而非其最初原因。对人类医学来说,这些自然发生的犬类病例提示,在类ALS疾病中,抑制炎症仍可能有益,但仅仅阻断免疫细胞进入神经系统的疗法不太可能从根本上阻止疾病。相反,治疗可能需要同时针对潜在的神经易损性,并在细致调控下而非简单关闭的情况下调整机体的免疫反应。
引用: Yokota, S., Kobatake, Y., Yoshida, K. et al. Analysis of immune-related alterations in blood and spinal cord of canine degenerative myelopathy, a spontaneous model of amyotrophic lateral sclerosis. Sci Rep 16, 13494 (2026). https://doi.org/10.1038/s41598-026-43838-5
关键词: 退行性脊髓病, 肌萎缩侧索硬化症, 神经炎症, 犬类模型, 免疫反应