Clear Sky Science · es
Análisis de alteraciones relacionadas con el sistema inmunitario en sangre y médula espinal de la mielopatía degenerativa canina, un modelo espontáneo de la esclerosis lateral amiotrófica
Por qué una enfermedad canina importa a las personas
Muchos perros mayores, en especial los Pembroke Welsh Corgis, pueden desarrollar una enfermedad espinal fatal llamada mielopatía degenerativa. Esta afección les arrebata lentamente la capacidad de caminar y, finalmente, de respirar. De manera notable, se asemeja estrechamente a la esclerosis lateral amiotrófica (ELA) en humanos, también conocida como la enfermedad de Lou Gehrig. Dado que los perros desarrollan de forma natural este problema y comparten una mutación genética clave con algunos pacientes de ELA, su estudio puede revelar cómo interactúan el daño del sistema nervioso y las defensas del organismo en un contexto real, más allá de lo que muestran los modelos de ratón modificados genéticamente.
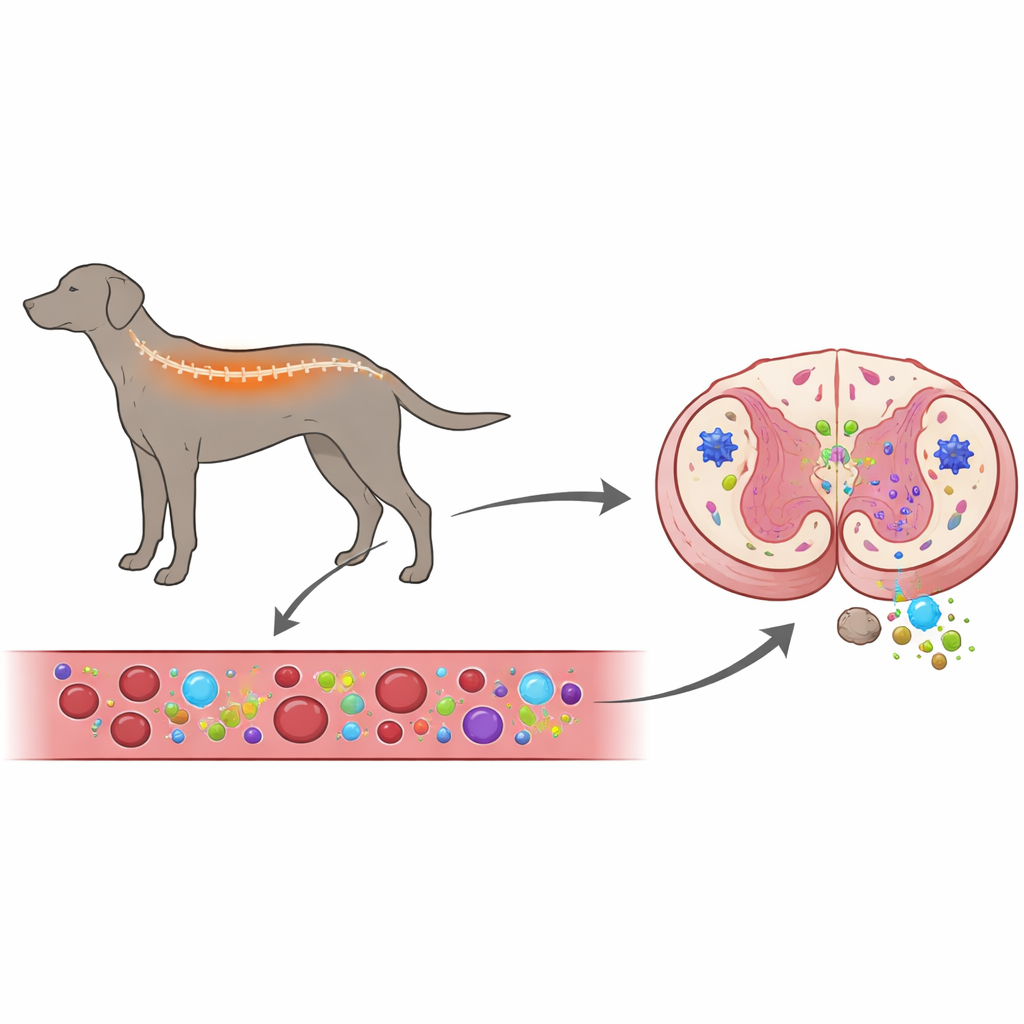
Estudiar sangre y médula espinal conjuntamente
Los investigadores se propusieron responder una pregunta central: ¿impulsa el sistema inmunitario la enfermedad en los perros, o más bien reacciona al daño nervioso que ya está en marcha? Para explorar esto, examinaron tanto la sangre como las médulas espinales de perros con mielopatía degenerativa y las compararon con perros sanos y con perros que padecían otro problema espinal, la hernia de disco intervertebral, que comprime la médula espinal desde fuera. Midieron la actividad de genes relacionados con la inflamación en células sanguíneas y en tejido medular, y usaron tinciones con anticuerpos fluorescentes para ver qué células inmunitarias y de soporte estaban presentes en la médula espinal y cuán activas eran.
Señales de alarma inmunitaria en la sangre
En la sangre de los perros afectados, el equipo encontró indicios de que ciertos leucocitos estaban en un estado de “alerta”. Los genes vinculados a un sistema molecular de alarma conocido como inflammasoma, que contribuye a producir mensajeros inflamatorios, mostraron mayor actividad que en los animales control. Al mismo tiempo, un gen de una molécula inmunitaria que actúa como “freno” y tiende a calmar la inflamación también estaba más activo, lo que sugiere que el organismo intentaba contener esa alarma. No obstante, las pruebas sanguíneas de rutina parecían normales: los recuentos de células blancas y un marcador habitual de inflamación llamado proteína C reactiva permanecieron dentro de los límites típicos. Este patrón apunta a una activación inmunitaria sutil y muy regulada en lugar de un estallido inflamatorio generalizado en todo el organismo.
Quién entra en la médula espinal y quién se queda fuera
La siguiente cuestión fue si las células sanguíneas activadas realmente penetran masivamente en la médula espinal, como ocurre en algunos modelos de ratón de la ELA. Utilizando marcadores celulares que distinguen las células inmunitarias residentes del sistema nervioso de las recién llegadas desde la sangre, los científicos observaron solo unas pocas células probablemente inmigrantes en cada sección transversal completa de médula afectada. En otras palabras, hubo evidencia de que algunas células derivadas de la sangre sí entraron en el tejido nervioso, pero en números muy reducidos. Al mismo tiempo, detectaron un aumento en la producción de una señal química en la médula espinal que normalmente atrae a esas células desde el torrente sanguíneo, lo que indica que el propio tejido estaba pidiendo ayuda aunque solo llegaran unos pocos respondedores.
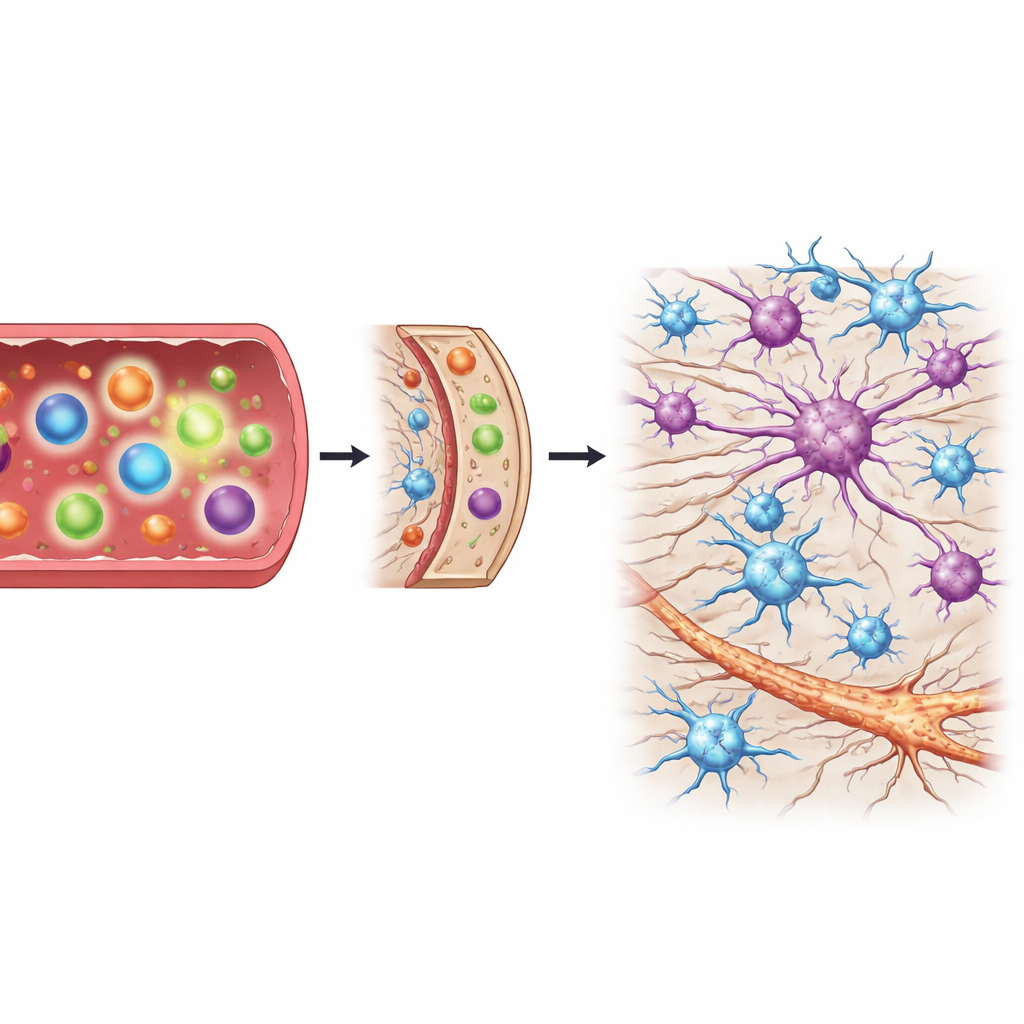
Las células de soporte responden a medida que el daño empeora
La médula espinal contiene no solo fibras nerviosas sino también células de soporte llamadas astrocitos y microglía, que pueden proteger o dañar a las neuronas según su estado. Al agrupar las muestras de médula espinal según el grado de daño—de ninguno, a leve, a moderado y a severo—el equipo pudo seguir cómo cambiaban estas células de soporte con el tiempo. A medida que la degeneración avanzaba, los genes que señalan tanto formas dañinas como protectoras de astrocitos aumentaron de forma pronunciada, y la quimiocina que recluta células inmunitarias se hizo más activa. En contraste, los marcadores de microglía activada no mostraron incrementos tempranos y marcados cuando el daño aún era leve. Ese calendario sugiere que la gran oleada de activación de astrocitos y de señalización inmune aparece después de que el daño nervioso ya está establecido, más que en el inicio del proceso.
Qué significa esto para perros y personas
En conjunto, los resultados dibujan un panorama en el que la mielopatía degenerativa implica un cambio inmunitario discreto pero complejo: las células sanguíneas están predispuestas, la médula espinal envía señales de angustia y las células de soporte locales reaccionan con fuerza a medida que se acumula el daño. Sin embargo, la invasión real de células inmunitarias procedentes de la sangre hacia la médula sigue siendo limitada, y los cambios inflamatorios dramáticos aparecen principalmente en etapas avanzadas. Para los propietarios de perros, esto significa que, cuando aparecen los signos evidentes de la enfermedad, los cambios inmunitarios son más una respuesta a la pérdida neuronal que su causa original. Para la medicina humana, estos casos caninos espontáneos sugieren que, en enfermedades similares a la ELA, reducir la inflamación puede seguir siendo útil, pero las terapias que solo se centran en bloquear la entrada de células inmunitarias al sistema nervioso probablemente no detendrán la enfermedad en su raíz. En su lugar, los tratamientos podrían necesitar apuntar a la vulnerabilidad neuronal subyacente mientras modulan con cuidado, en lugar de simplemente apagar, la respuesta inmunitaria del organismo.
Cita: Yokota, S., Kobatake, Y., Yoshida, K. et al. Analysis of immune-related alterations in blood and spinal cord of canine degenerative myelopathy, a spontaneous model of amyotrophic lateral sclerosis. Sci Rep 16, 13494 (2026). https://doi.org/10.1038/s41598-026-43838-5
Palabras clave: mielopatía degenerativa, esclerosis lateral amiotrófica, neuroinflamación, modelo canino, respuesta inmunitaria