Clear Sky Science · pt
Análise de alterações relacionadas ao sistema imunológico no sangue e na medula espinhal da mielopatia degenerativa canina, um modelo espontâneo de esclerose lateral amiotrófica
Por que uma doença de cão importa para as pessoas
Muitos cães idosos, especialmente Pembroke Welsh Corgis, podem desenvolver uma doença fatal da coluna chamada mielopatia degenerativa. Essa condição gradualmente lhes rouba a capacidade de andar e, eventualmente, de respirar. De forma notável, ela se assemelha fortemente à esclerose lateral amiotrófica (ELA) em humanos, também conhecida como doença de Lou Gehrig. Como os cães desenvolvem esse problema de maneira natural e compartilham uma mutação gênica chave com alguns pacientes de ELA, estudá‑los pode revelar como o dano ao sistema nervoso e as defesas do corpo interagem em um contexto real, além do que é observado em modelos de camundongos geneticamente modificados.
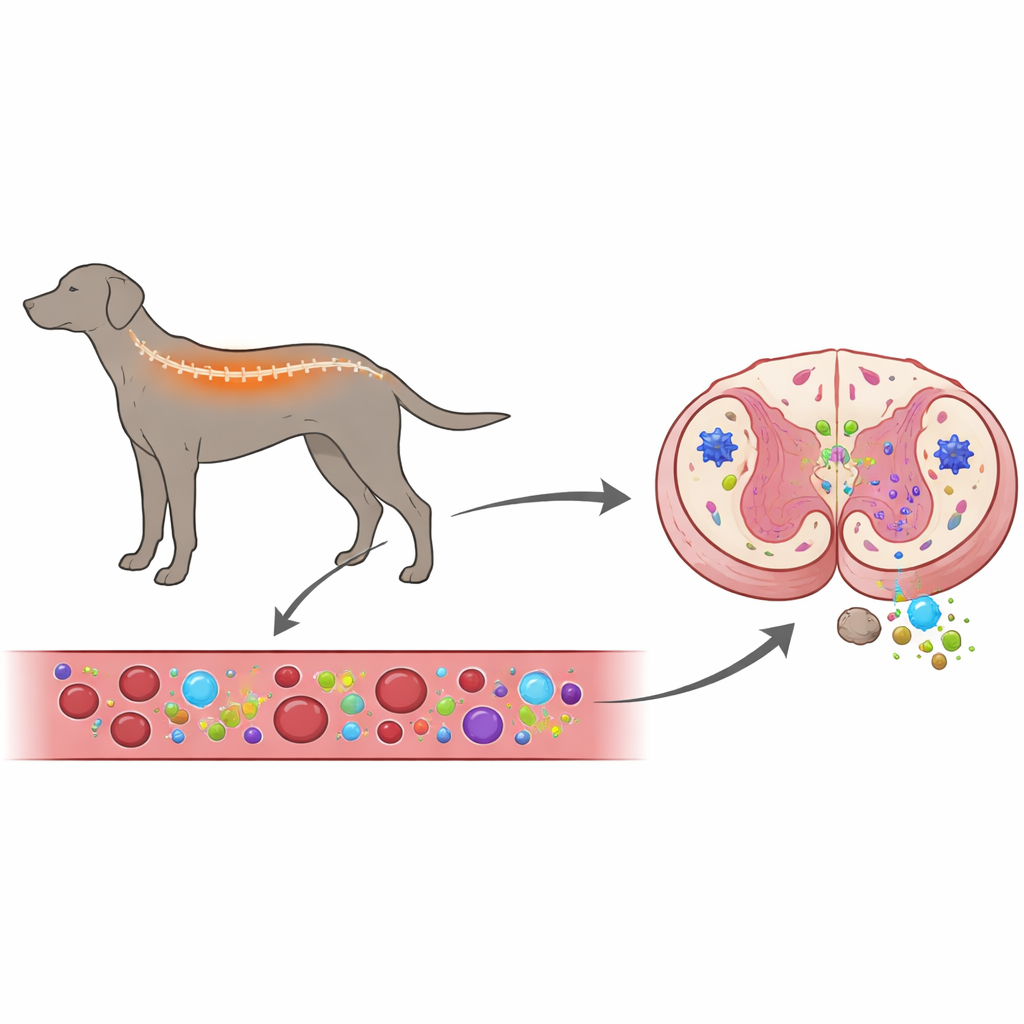
Analisando sangue e medula espinhal em conjunto
Os pesquisadores buscaram responder a uma questão central: o sistema imunológico contribui para impulsionar essa doença canina, ou ele reage principalmente ao dano nervoso já em curso? Para explorar isso, examinaram tanto o sangue quanto as medulas espinhais de cães com mielopatia degenerativa, comparando‑os com cães saudáveis e com cães que sofrem de outro problema espinhal, a hérnia de disco intervertebral, que comprime a medula espinhal externamente. Mediram a atividade de genes relacionados à inflamação em células sanguíneas e em tecido da medula, e usaram colorações com anticorpos fluorescentes para ver quais células imunes e de suporte estavam presentes na medula e quão ativas elas estavam.
Sinais de alarme imunológico no sangue
No sangue dos cães afetados, a equipe encontrou sinais de que certos glóbulos brancos estavam em um estado de “alerta”. Genes ligados a um sistema molecular de alarme conhecido como inflamasoma, que ajuda a produzir mensageiros inflamatórios, estavam mais ativos do que nos animais controle. Ao mesmo tempo, um gene de uma molécula “freio” imune que tende a acalmar a inflamação também estava mais ativo, sugerindo que o organismo tentava manter esse alarme sob controle. Exames sanguíneos de rotina, no entanto, pareciam normais: contagens de leucócitos e um marcador comum de inflamação chamado proteína C‑reativa permaneceram dentro de limites típicos. Esse padrão aponta para uma ativação imune sutil e rigidamente regulada, em vez de uma reação inflamatória generalizada e intensa.
Quem entra na medula espinhal e quem fica de fora
A questão seguinte foi se as células sanguíneas ativadas realmente invadem a medula espinhal, como ocorre em alguns modelos de camundongo de ELA. Usando marcadores celulares que distinguem células imunes residentes do cérebro de recém‑chegadas vindas do sangue, os cientistas viram apenas algumas prováveis células imigrantes em cada seção transversal inteira de medula afetada. Em outras palavras, havia evidência clara de que algumas células derivadas do sangue penetraram no tecido nervoso, mas em números muito pequenos. Ao mesmo tempo, observaram aumento da produção de um sinal químico na medula que normalmente atrai tais células da corrente sanguínea, indicando que o próprio tecido estava pedindo ajuda mesmo que poucos respondedores tenham chegado.
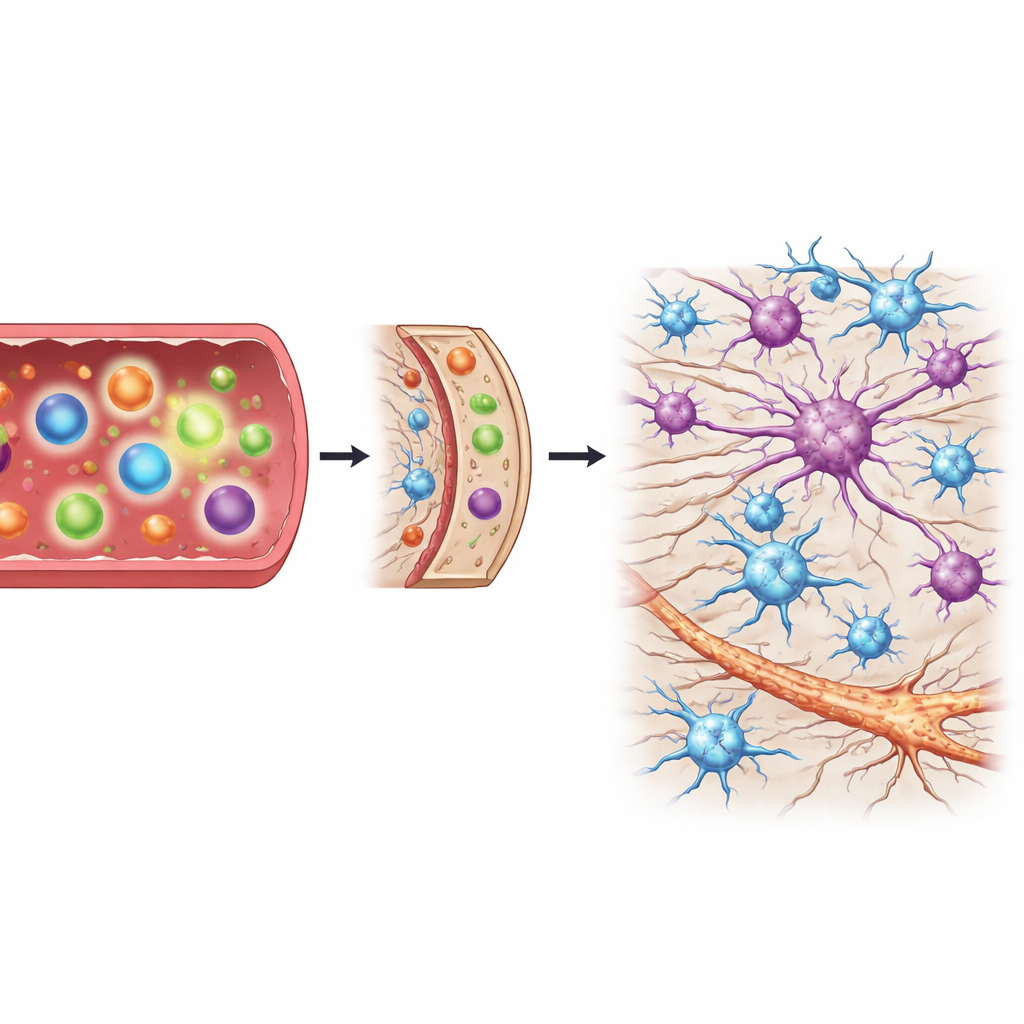
Células de suporte reagem à medida que o dano piora
A medula espinhal contém não apenas fibras nervosas, mas também células de suporte chamadas astrócitos e microglia, que podem proteger ou prejudicar os neurônios dependendo de seu estado. Ao agrupar amostras de medula conforme o grau de dano — de nenhum, a leve, moderado e severo — a equipe pôde acompanhar como essas células de suporte mudavam ao longo do tempo. À medida que a degeneração avançava, genes que marcam tanto formas prejudiciais quanto protetoras de astrócitos aumentaram acentuadamente, e a quimiocina que convoca células imunes tornou‑se mais ativa. Em contraste, marcadores de microglia ativada não mostraram aumentos fortes e precoces quando o dano ainda era leve. Esse padrão temporal sugere que a grande onda de ativação de astrócitos e de sinalização imune aparece depois que a lesão nervosa já está estabelecida, em vez de no início do processo.
O que isso significa para cães e pessoas
Em conjunto, os resultados desenham um quadro em que a mielopatia degenerativa envolve uma mudança imune discreta, porém complexa: células sanguíneas ficam preparadas, a medula espinhal envia sinais de socorro e as células de suporte locais reagem fortemente à medida que o dano se acumula. Ainda assim, a invasão real de células imunes do sangue para a medula permanece limitada, e mudanças inflamatórias dramáticas aparecem principalmente em estágios mais avançados. Para os donos de cães, isso significa que, quando sinais óbvios da doença se manifestam, as mudanças imunes são mais uma resposta à perda nervosa do que sua causa inicial. Para a medicina humana, esses casos naturais em cães sugerem que, em doenças semelhantes à ELA, reduzir a inflamação pode ainda ser útil, mas terapias que se concentrem apenas em bloquear a entrada de células imunes no sistema nervoso provavelmente não irão deter a doença em sua raiz. Em vez disso, tratamentos podem precisar direcionar a vulnerabilidade nervosa subjacente enquanto modulam cuidadosamente — e não simplesmente desligam — a resposta imune do organismo.
Citação: Yokota, S., Kobatake, Y., Yoshida, K. et al. Analysis of immune-related alterations in blood and spinal cord of canine degenerative myelopathy, a spontaneous model of amyotrophic lateral sclerosis. Sci Rep 16, 13494 (2026). https://doi.org/10.1038/s41598-026-43838-5
Palavras-chave: mielopatia degenerativa, esclerose lateral amiotrófica, neuroinflamação, modelo canino, resposta imune