Clear Sky Science · nl
Analyse van immuungerelateerde veranderingen in bloed en ruggenmerg van levensbedreigende degeneratieve myelopathie bij honden, een spontaan model voor amyotrofische laterale sclerose
Waarom een hondenziekte van belang is voor mensen
Veel oudere honden, vooral Pembroke Welsh Corgis, kunnen een dodelijke ruggenmergziekte ontwikkelen die degeneratieve myelopathie wordt genoemd. Deze aandoening ontneemt hen geleidelijk het vermogen om te lopen en uiteindelijk om te ademen. Opvallend is dat het sterk lijkt op amyotrofische laterale sclerose (ALS) bij mensen, ook bekend als de ziekte van Lou Gehrig. Omdat honden deze aandoening van nature ontwikkelen en een belangrijke genetische mutatie delen met sommige ALS-patiënten, kan het bestuderen van honden onthullen hoe zenuwstelselbeschadiging en de verdedigingsreacties van het lichaam in een reële situatie op elkaar inwerken, verdergaand dan wat te zien is in gemodificeerde muismodellen.
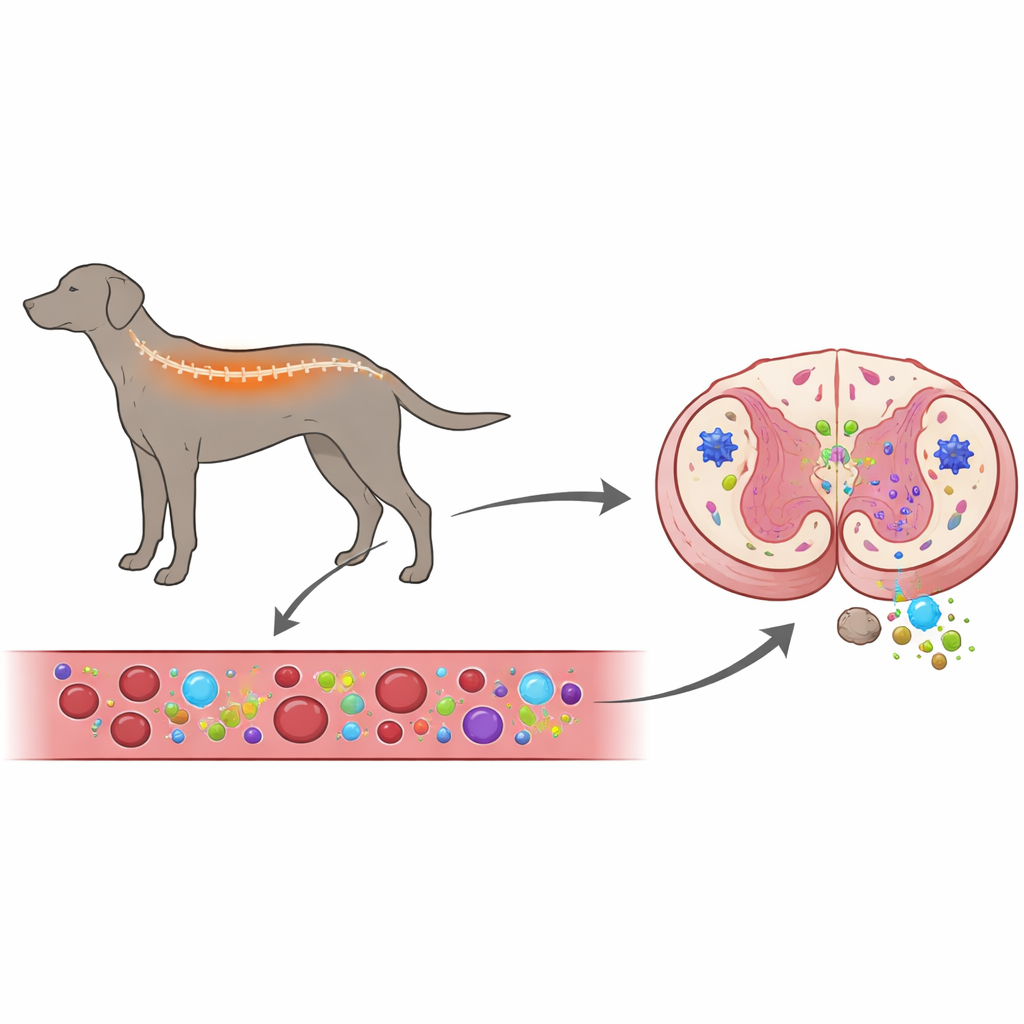
Bloed en ruggenmerg samen bekeken
De onderzoekers wilden een centrale vraag beantwoorden: drijft het immuunsysteem deze hondenziekte, of reageert het vooral op zenuwbeschadiging die al aan de gang is? Om dit te onderzoeken bekeken ze zowel het bloed als de ruggenmerg van honden met degeneratieve myelopathie en vergeleken die met gezonde honden en honden met een andere rugaandoening, een tussenwervelschijfbreuk, die het ruggenmerg van buitenaf samendrukt. Ze maten de activiteit van genen die met ontsteking samenhangen in bloedcellen en ruggenmergweefsel, en gebruikten fluorescent gekleurde antilichamen om te zien welke immuun- en ondersteunende cellen in het ruggenmerg aanwezig waren en hoe actief die waren.
Signalen van immuunalarm in het bloed
In het bloed van aangetaste honden vond het team aanwijzingen dat bepaalde witte bloedcellen in een "alarm"-toestand waren gezet. Genen die gekoppeld zijn aan een moleculair alarmsysteem dat het inflammasoom wordt genoemd en dat helpt bij de productie van ontstekingsboodschappers, waren actiever dan bij controledieren. Tegelijkertijd was ook een gen voor een immuunremmend molecuul, dat doorgaans ontsteking kalmeert, verhoogd actief, wat suggereert dat het lichaam probeerde dit alarm onder controle te houden. Routinebloedtesten zagen er echter normaal uit: het aantal witte bloedcellen en een algemeen ontstekingsmarker, C-reactief proteïne, bleven binnen gebruikelijke grenzen. Dit patroon duidt op een subtiele, strak gereguleerde immuunactivatie in plaats van een volledige, systemische ontstekingsopvlamming.
Wie het ruggenmerg binnenkomt, en wie buiten blijft
De volgende vraag was of geactiveerde bloedcellen daadwerkelijk het ruggenmerg binnenstromen, zoals gebeurt in sommige muismodellen van ALS. Met celmarkers die residentiële hersenimmuuncellen van nieuwkomers uit het bloed onderscheiden, zagen de onderzoekers slechts een handvol waarschijnlijke binnenkomende cellen in elke gehele dwarsdoorsnede van aangetast ruggenmerg. Met andere woorden, er was duidelijk bewijs dat enkele bloedafgeleide cellen het zenuwweefsel binnendrongen, maar in zeer kleine aantallen. Tegelijkertijd zagen ze verhoogde productie van een chemisch signaal in het ruggenmerg dat normaal zulke cellen uit de bloedbaan aantrekt, wat aangeeft dat het weefsel zelf om hulp riep, ook al arriveerden er maar weinig respondenten.
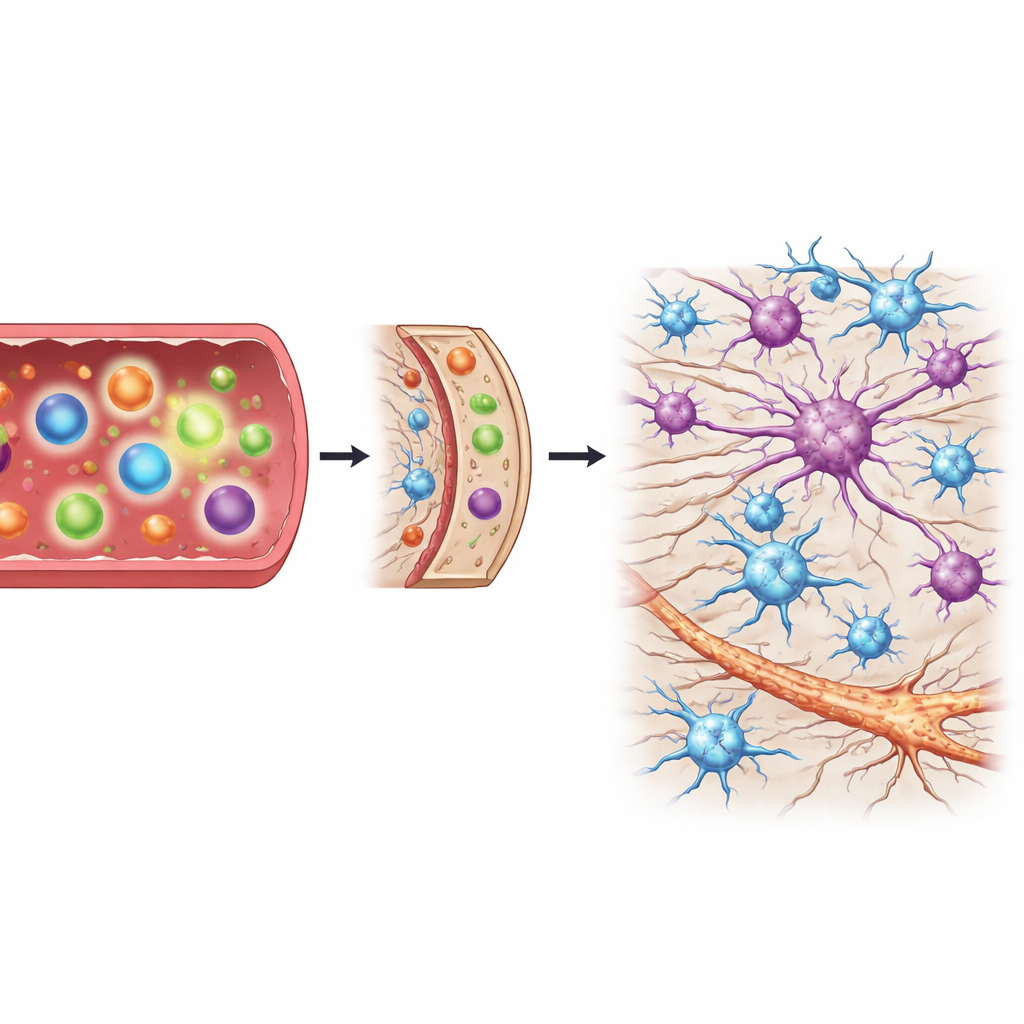
Ondersteunende cellen reageren naarmate schade verergert
Het ruggenmerg bevat niet alleen zenuwvezels maar ook ondersteunende cellen die astrocyten en microglia worden genoemd en die, afhankelijk van hun toestand, neuronen kunnen beschermen of schaden. Door ruggenmergmonsters te groeperen naar de ernst van de schade — van geen, tot mild, tot matig, tot ernstig — kon het team volgen hoe deze ondersteunende cellen in de tijd veranderden. Naarmate degeneratie vorderde, namen genen die zowel schadelijke als beschermende vormen van astrocyten markeren sterk toe, en werd de chemokine die immuuncellen aantrekt actiever. Ter vergelijking vertoonden markers voor geactiveerde microglia geen sterke, vroege stijgingen wanneer de schade nog mild was. Deze timing suggereert dat de grote golf van astrocytactivatie en immuunsignalisatie verschijnt nadat zenuwbeschadiging al was begonnen, in plaats van helemaal aan het begin.
Wat dit betekent voor honden en mensen
Gezamenlijk schetsen de resultaten het beeld van een stille maar complexe immuunverschuiving: bloedcellen zijn geprimed, het ruggenmerg stuurt noodsignalen en lokale ondersteunende cellen reageren krachtig naarmate schade zich ophoopt. Toch blijft de daadwerkelijke invasie van immuuncellen uit het bloed in het ruggenmerg beperkt en treden dramatische ontstekingsveranderingen vooral in latere stadia op. Voor hondenbezitters betekent dit dat, tegen de tijd dat duidelijke ziekteverschijnselen verschijnen, immuunveranderingen meer een reactie op zenuwverlies zijn dan de oorspronkelijke oorzaak. Voor de menselijke geneeskunde suggereren deze van nature voorkomende hondencases dat het terugschroeven van ontsteking nog steeds nuttig kan zijn bij ALS-achtige aandoeningen, maar dat therapieën die zich uitsluitend richten op het blokkeren van immuuncellen om het zenuwstelsel binnen te dringen waarschijnlijk de ziekte niet bij de wortel zullen stoppen. In plaats daarvan moeten behandelingen mogelijk de onderliggende kwetsbaarheid van zenuwen aanpakken en tegelijkertijd de immuunrespons zorgvuldig moduleren, in plaats van deze simpelweg uit te schakelen.
Bronvermelding: Yokota, S., Kobatake, Y., Yoshida, K. et al. Analysis of immune-related alterations in blood and spinal cord of canine degenerative myelopathy, a spontaneous model of amyotrophic lateral sclerosis. Sci Rep 16, 13494 (2026). https://doi.org/10.1038/s41598-026-43838-5
Trefwoorden: degeneratieve myelopathie, amyotrofische laterale sclerose, neuroinflammatie, canien model, immuunrespons