Clear Sky Science · fr
Analyse des altérations liées au système immunitaire dans le sang et la moelle épinière de la myélopathie dégénérative canine, un modèle spontané de la sclérose latérale amyotrophique
Pourquoi une maladie canine importe pour l’homme
De nombreux chiens âgés, en particulier les Pembroke Welsh Corgis, peuvent développer une maladie médullaire fatale appelée myélopathie dégénérative. Cette affection leur ôte progressivement la capacité de marcher puis, à terme, de respirer. Fait remarquable, elle ressemble étroitement à la sclérose latérale amyotrophique (SLA) chez l’humain, également connue sous le nom de maladie de Lou Gehrig. Parce que les chiens développent naturellement ce problème et partagent une mutation génétique clé avec certains patients atteints de SLA, les étudier peut révéler comment les lésions du système nerveux et les défenses de l’organisme interagissent dans un contexte réel, au-delà de ce que montrent les modèles murins génétiquement modifiés.
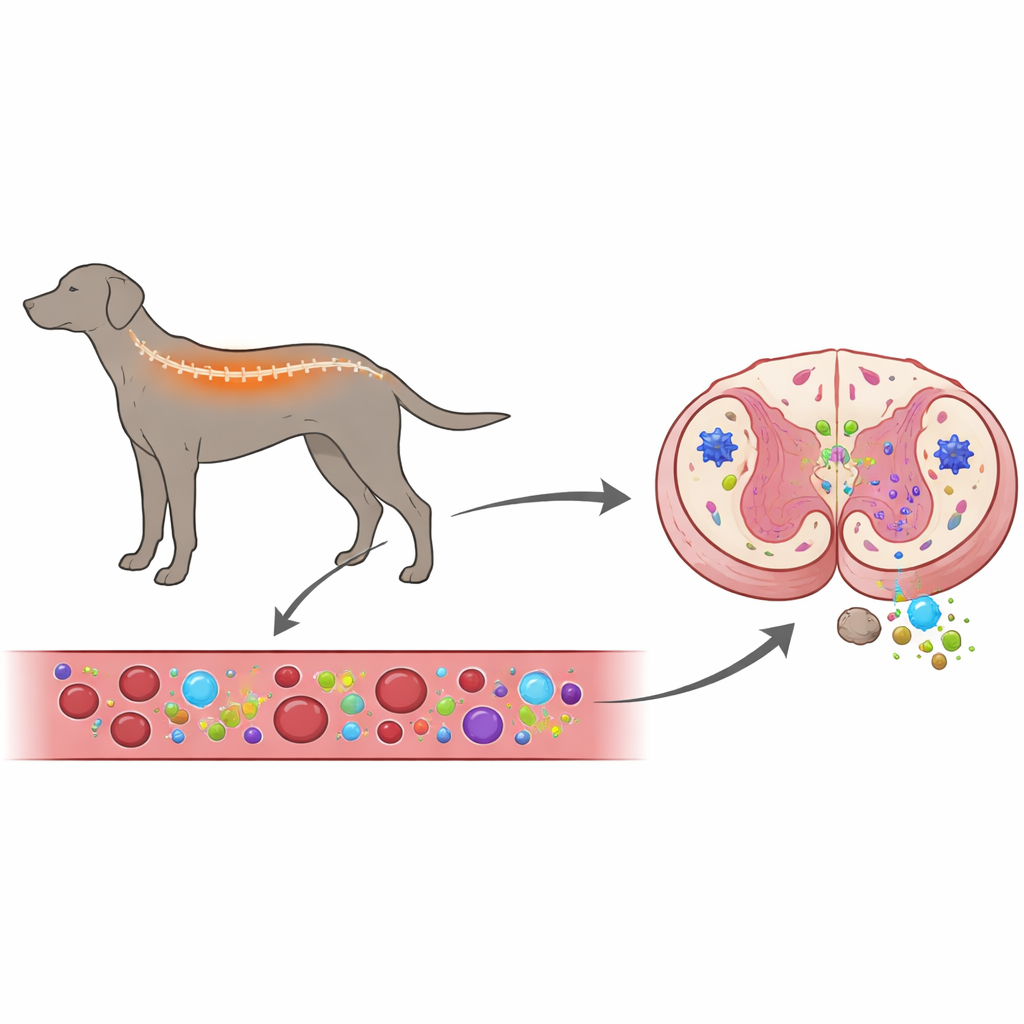
Examiner le sang et la moelle ensemble
Les chercheurs ont cherché à répondre à une question centrale : le système immunitaire contribue-t-il à déclencher cette maladie canine, ou réagit-il principalement à des lésions nerveuses déjà en cours ? Pour l’explorer, ils ont analysé à la fois le sang et la moelle épinière de chiens atteints de myélopathie dégénérative, et les ont comparés à des chiens sains et à des chiens souffrant d’un autre problème médullaire, la hernie discale intervertébrale, qui comprime la moelle de l’extérieur. Ils ont mesuré l’activité de gènes liés à l’inflammation dans les cellules sanguines et dans le tissu médullaire, et utilisé des marquages d’anticorps fluorescents pour voir quelles cellules immunitaires et de soutien étaient présentes dans la moelle épinière et à quel point elles étaient actives.
Signaux d’alerte immunitaire dans le sang
Dans le sang des chiens affectés, l’équipe a trouvé des indices montrant que certains globules blancs étaient passés à un état « d’alerte ». Des gènes associés à un système d’alerte moléculaire connu sous le nom d’inflammasome, qui participe à la production de médiateurs inflammatoires, étaient plus actifs que chez les animaux témoins. En même temps, un gène codant pour une molécule « frein » du système immunitaire, qui tend à calmer l’inflammation, était lui aussi plus exprimé, ce qui suggère que l’organisme tentait de maîtriser cette alarme. Les analyses sanguines de routine, cependant, semblaient normales : numération des leucocytes et un marqueur d’inflammation courant, la protéine C-réactive, restaient dans des limites habituelles. Ce schéma indique une activation immunitaire subtile et finement régulée plutôt qu’un épisode inflammatoire généralisé et franc.
Qui pénètre dans la moelle épinière, et qui reste à l’extérieur
La question suivante était de savoir si les cellules sanguines activées infiltraient massivement la moelle épinière, comme dans certains modèles murins de SLA. En utilisant des marqueurs cellulaires distinguant les cellules immunitaires résidentes du cerveau des nouveaux arrivants issus du sang, les scientifiques n’ont observé qu’une poignée de cellules probablement immigrantes par coupe transversale entière de moelle affectée. Autrement dit, il existait une preuve que certaines cellules dérivées du sang pénétraient dans le tissu nerveux, mais en très petit nombre. Parallèlement, ils ont constaté une augmentation de la production d’un signal chimique dans la moelle épinière qui attire normalement ces cellules depuis la circulation sanguine, ce qui indique que le tissu appelait de l’aide même si peu de répondeurs arrivaient.
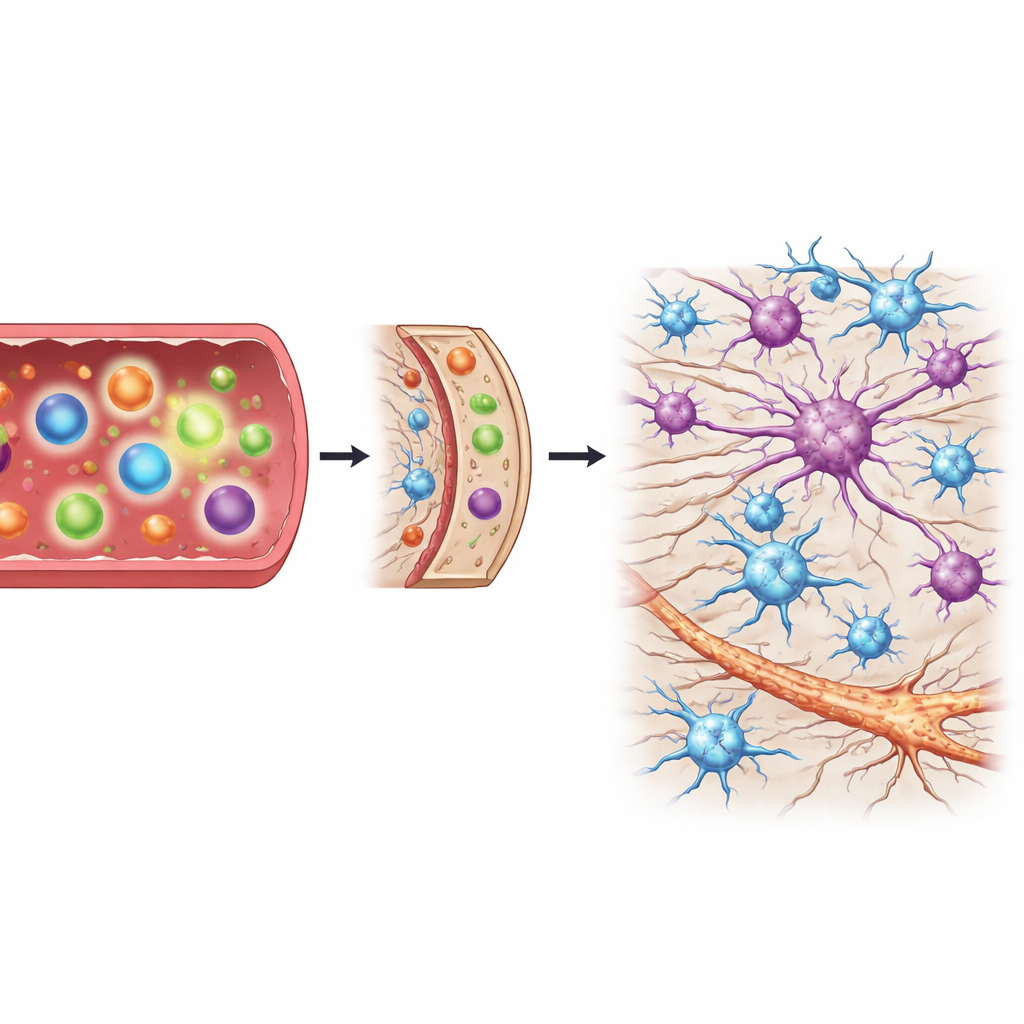
Les cellules de soutien réagissent à mesure que les lésions s’aggravent
La moelle épinière contient non seulement des fibres nerveuses mais aussi des cellules de soutien appelées astrocytes et microglies, qui peuvent protéger ou nuire aux neurones selon leur état. En regroupant les échantillons de moelle selon la sévérité des lésions — aucune, légère, modérée, sévère — l’équipe a pu suivre l’évolution de ces cellules de soutien au fil du temps. À mesure que la dégénérescence progressait, les gènes marquant à la fois des formes potentiellement nocives et protectrices d’astrocytes augmentaient fortement, et la chimiokine qui attire les cellules immunitaires devenait plus active. En revanche, les marqueurs d’activation des microglies n’affichaient pas de fortes augmentations précoces lorsque les lésions étaient encore légères. Ce calendrier suggère que la grande vague d’activation des astrocytes et de signalisation immunitaire apparaît après l’installation des lésions nerveuses, plutôt qu’au tout début.
Ce que cela signifie pour les chiens et les humains
Pris dans leur ensemble, les résultats dessinent le tableau d’un basculement immunitaire discret mais complexe : les cellules sanguines sont en état d’alerte, la moelle épinière envoie des signaux de détresse et les cellules locales de soutien réagissent fortement à mesure que les lésions s’accumulent. Pourtant, l’invasion effective de cellules immunitaires provenant du sang dans la moelle reste limitée, et des changements inflammatoires spectaculaires n’apparaissent principalement qu’aux stades avancés. Pour les propriétaires de chiens, cela signifie que, au moment où des signes cliniques évidents apparaissent, les modifications immunitaires sont davantage une réponse à la perte neuronale qu’une cause initiale. Pour la médecine humaine, ces cas canins survenant naturellement suggèrent que, dans des maladies de type SLA, réduire l’inflammation peut rester utile, mais que des thérapies visant uniquement à empêcher les cellules immunitaires d’entrer dans le système nerveux sont peu susceptibles d’empêcher la maladie à la source. Les traitements devront plutôt cibler la vulnérabilité neuronale sous-jacente tout en modulant avec précaution, plutôt qu’en supprimant complètement, la réponse immunitaire de l’organisme.
Citation: Yokota, S., Kobatake, Y., Yoshida, K. et al. Analysis of immune-related alterations in blood and spinal cord of canine degenerative myelopathy, a spontaneous model of amyotrophic lateral sclerosis. Sci Rep 16, 13494 (2026). https://doi.org/10.1038/s41598-026-43838-5
Mots-clés: myélopathie dégénérative, sclérose latérale amyotrophique, neuroinflammation, modèle canin, réponse immunitaire