Clear Sky Science · de
Analyse immunbezogener Veränderungen im Blut und Rückenmark bei caniner degenerativer Myelopathie, einem spontanen Modell der amyotrophen Lateralsklerose
Warum eine Hundekrankheit für Menschen wichtig ist
Viele ältere Hunde, insbesondere Pembroke Welsh Corgis, können eine tödliche Wirbelsäulenerkrankung namens degenerative Myelopathie entwickeln. Diese Erkrankung raubt ihnen allmählich die Fähigkeit zu laufen und schließlich zu atmen. Auffallend ist, dass sie der amyotrophen Lateralsklerose (ALS) des Menschen, auch bekannt als Lou-Gehrig-Krankheit, sehr ähnelt. Da Hunde dieses Problem auf natürliche Weise entwickeln und eine wichtige Genmutation mit einigen ALS-Patienten teilen, kann ihre Untersuchung zeigen, wie Nervenschäden und körpereigene Abwehrmechanismen in einem realen Umfeld zusammenspielen — jenseits dessen, was in gentechnisch veränderten Mausmodellen sichtbar ist.
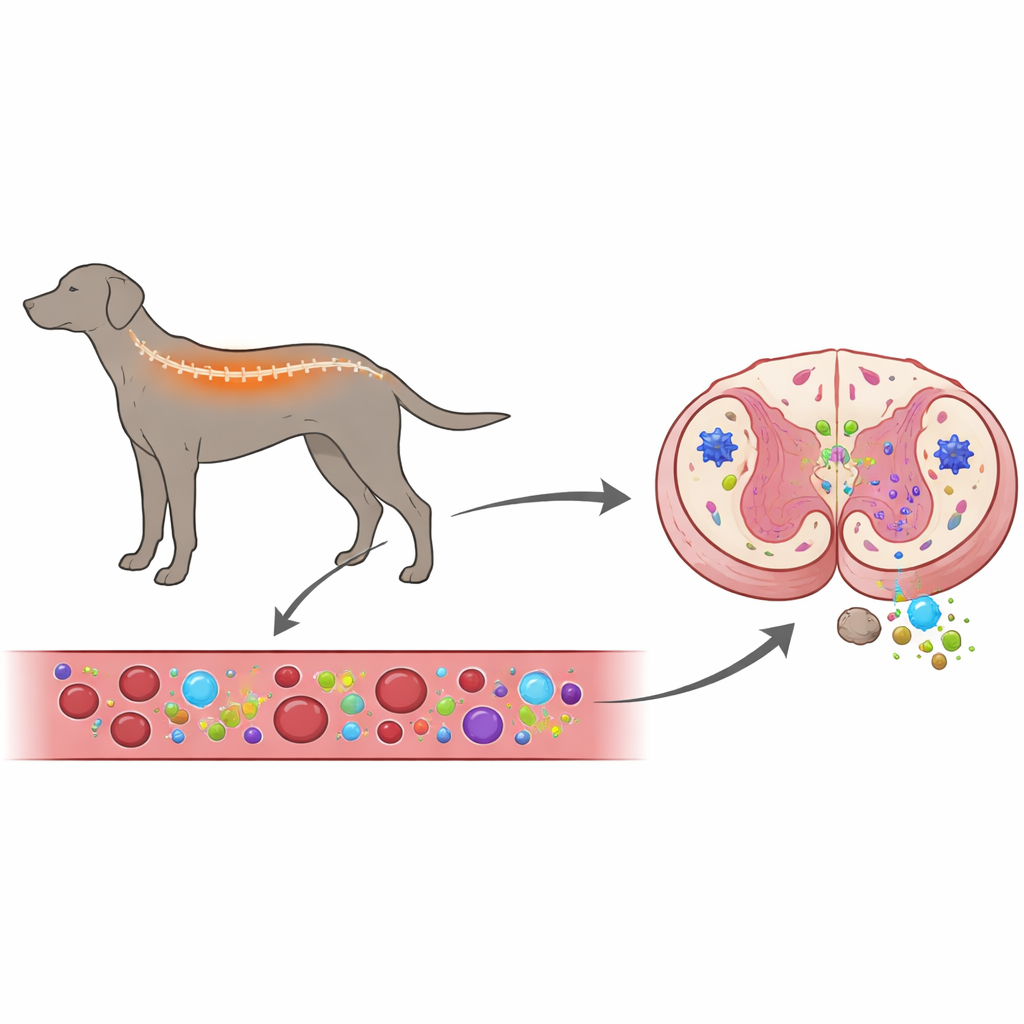
Blut und Rückenmark gemeinsam betrachten
Die Forschenden wollten eine zentrale Frage klären: Treibt das Immunsystem diese Hundekrankheit voran, oder reagiert es hauptsächlich auf bereits eingetretene Nervenschäden? Zur Untersuchung analysierten sie sowohl Blut als auch Rückenmark von Hunden mit degenerativer Myelopathie und verglichen diese mit gesunden Hunden und Hunden mit einem anderen Wirbelsäulenproblem, Bandscheibenvorfall, der das Rückenmark von außen komprimiert. Sie maßen die Aktivität von Entzündungsgenen in Blutzellen und Rückenmarkgewebe und nutzten fluoreszierende Antikörperfärbungen, um zu sehen, welche Immun- und Stützzellen im Rückenmark vorhanden waren und wie aktiv sie waren.
Hinweise auf Immunalarm im Blut
Im Blut der betroffenen Hunde fanden die Forschenden Anzeichen dafür, dass bestimmte weiße Blutkörperchen in einen „Alarmzustand“ versetzt waren. Gene, die mit einem molekularen Alarmsystem namens Inflammasom verbunden sind und an der Produktion entzündlicher Botenstoffe beteiligt sind, zeigten eine erhöhte Aktivität im Vergleich zu Kontrolltieren. Gleichzeitig war auch ein Gen für ein immunes "Bremse"-Molekül, das Entzündungen tendenziell dämpft, stärker aktiv, was darauf hindeutet, dass der Körper versuchte, diesen Alarm zu kontrollieren. Routinemäßige Bluttests sahen jedoch normal aus: Leukozytenzahlen und ein gängiger Entzündungsmarker, das C-reaktive Protein, blieben im üblichen Bereich. Dieses Muster deutet auf eine subtile, eng regulierte Immunaktivierung hin, statt auf einen großflächigen, systemischen Entzündungsschub.
Wer gelangt ins Rückenmark, und wer bleibt draußen
Als Nächstes stellten die Forschenden die Frage, ob aktivierte Blutzellen wie in einigen Mausmodellen der ALS massiv ins Rückenmark eindringen. Mit Zellmarkern, die Bewohner-Immunzellen des Gehirns von Neuankömmlingen aus dem Blut unterscheiden, fanden sie in jedem Rückenmarksquerschnitt betroffener Tiere nur eine Handvoll wahrscheinlich eingewanderter Zellen. Mit anderen Worten: Es gab klare Hinweise darauf, dass einige blutabgeleitete Zellen ins Nervengewebe gelangten, aber in sehr geringer Zahl. Gleichzeitig beobachteten sie im Rückenmark eine erhöhte Produktion eines chemischen Signals, das normalerweise solche Zellen aus dem Blut anlockt, was darauf hindeutet, dass das Gewebe selbst um Hilfe rief, auch wenn nur wenige Helfer eintrafen.
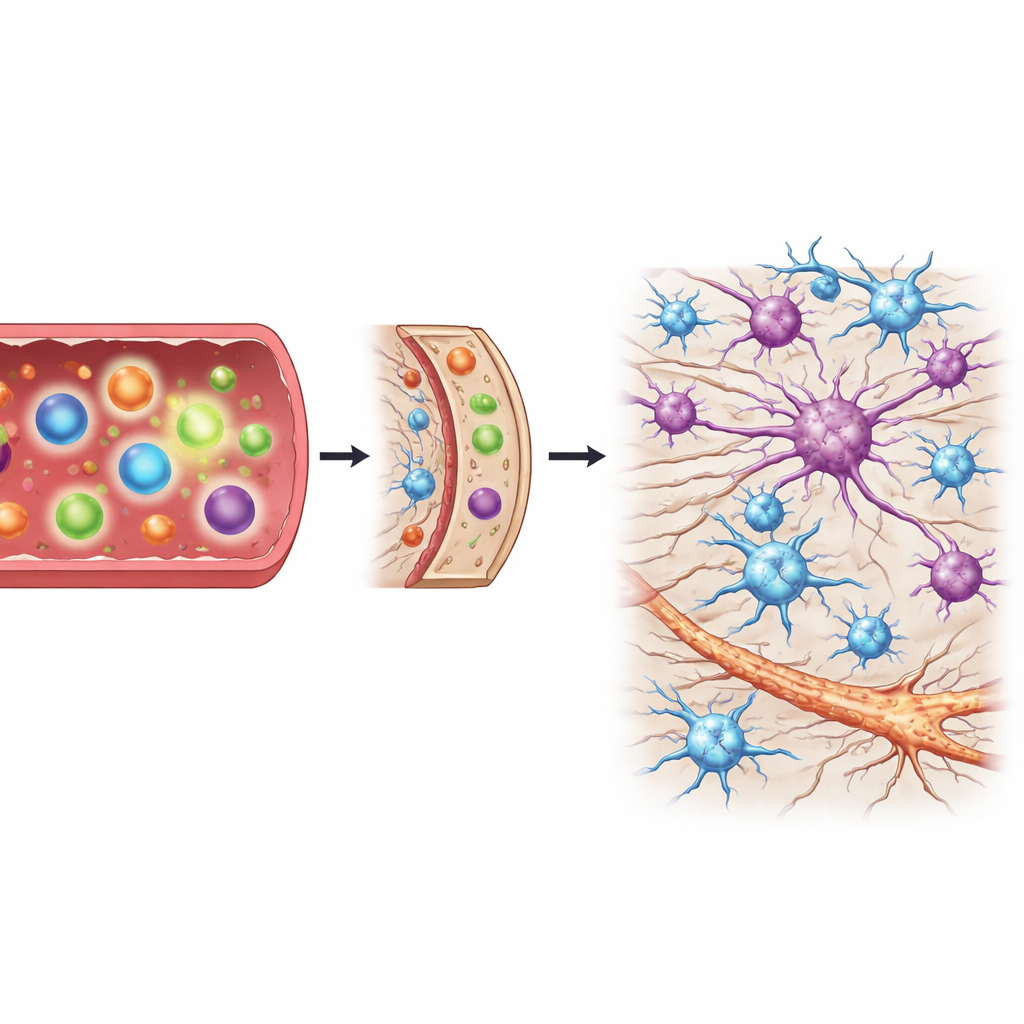
Stützzellen reagieren, während der Schaden zunimmt
Das Rückenmark besteht nicht nur aus Nervenfasern, sondern auch aus Stützzellen wie Astrozyten und Mikroglia, die je nach Zustand Neuronen schützen oder schädigen können. Indem die Forschenden Rückenmarksproben nach dem Schweregrad der Schäden gruppierten — von keinem über gering und mäßig bis schwer — konnten sie verfolgen, wie sich diese Stützzellen im Verlauf veränderten. Mit fortschreitender Degeneration stiegen Gene, die sowohl schädliche als auch schützende Astrozyten markieren, stark an, und die Chemokinproduktion, die Immunzellen anlockt, nahm zu. Dagegen zeigten Marker für aktivierte Mikroglia bei noch milden Schäden keine ausgeprägten Frühanstiege. Diese zeitliche Abfolge legt nahe, dass die große Welle der Astrozytenaktivierung und der Immunsignalgebung erst nach bereits bestehendem Nervenschaden auftritt und nicht ganz am Anfang.
Was das für Hunde und Menschen bedeutet
In der Gesamtschau zeichnen die Ergebnisse das Bild einer leisen, aber komplexen Immunverschiebung bei degenerativer Myelopathie: Blutzellen sind vorgemerkt, das Rückenmark sendet Notrufe, und lokale Stützzellen reagieren stark, während sich der Schaden anhäuft. Dennoch bleibt die tatsächliche Invasion von Immunzellen aus dem Blut ins Rückenmark begrenzt, und dramatische entzündliche Veränderungen treten vor allem in späteren Stadien auf. Für Hundebesitzer bedeutet dies, dass, wenn die offensichtlichen Krankheitszeichen auftreten, die Immunveränderungen eher als Reaktion auf den Nervverlust denn als dessen ursprüngliche Ursache zu sehen sind. Für die Humanmedizin deuten diese natürlich vorkommenden Hundefälle darauf hin, dass das Dämpfen von Entzündungen weiterhin nützlich sein kann, Therapien, die ausschließlich darauf abzielen, das Eindringen von Immunzellen in das Nervensystem zu blockieren, jedoch unwahrscheinlich sind, die Krankheit an ihrer Wurzel zu stoppen. Stattdessen müssten Behandlungen die zugrundeliegende Verwundbarkeit der Nerven adressieren und gleichzeitig die Immunantwort sorgfältig modulieren, statt sie einfach auszuschalten.
Zitation: Yokota, S., Kobatake, Y., Yoshida, K. et al. Analysis of immune-related alterations in blood and spinal cord of canine degenerative myelopathy, a spontaneous model of amyotrophic lateral sclerosis. Sci Rep 16, 13494 (2026). https://doi.org/10.1038/s41598-026-43838-5
Schlüsselwörter: degenerative Myelopathie, amyotrophe Lateralsklerose, Neuroinflammation, canines Modell, Immunantwort