Clear Sky Science · it
Analisi delle alterazioni immunitarie nel sangue e nel midollo spinale della mielopatia degenerativa canina, un modello spontaneo della sclerosi laterale amiotrofica
Perché una malattia dei cani importa alle persone
Molti cani anziani, in particolare i Pembroke Welsh Corgi, possono sviluppare una malattia spinale fatale chiamata mielopatia degenerativa. Questa condizione li priva gradualmente della capacità di camminare e, infine, di respirare. Notevolmente, somiglia molto alla sclerosi laterale amiotrofica (SLA) negli esseri umani, nota anche come malattia di Lou Gehrig. Poiché i cani sviluppano naturalmente questo problema e condividono una mutazione genica chiave con alcuni pazienti affetti da SLA, studiarli può rivelare come il danno al sistema nervoso e le difese dell’organismo interagiscono in un contesto naturale, oltre ciò che è osservabile nei modelli murini ingegnerizzati.
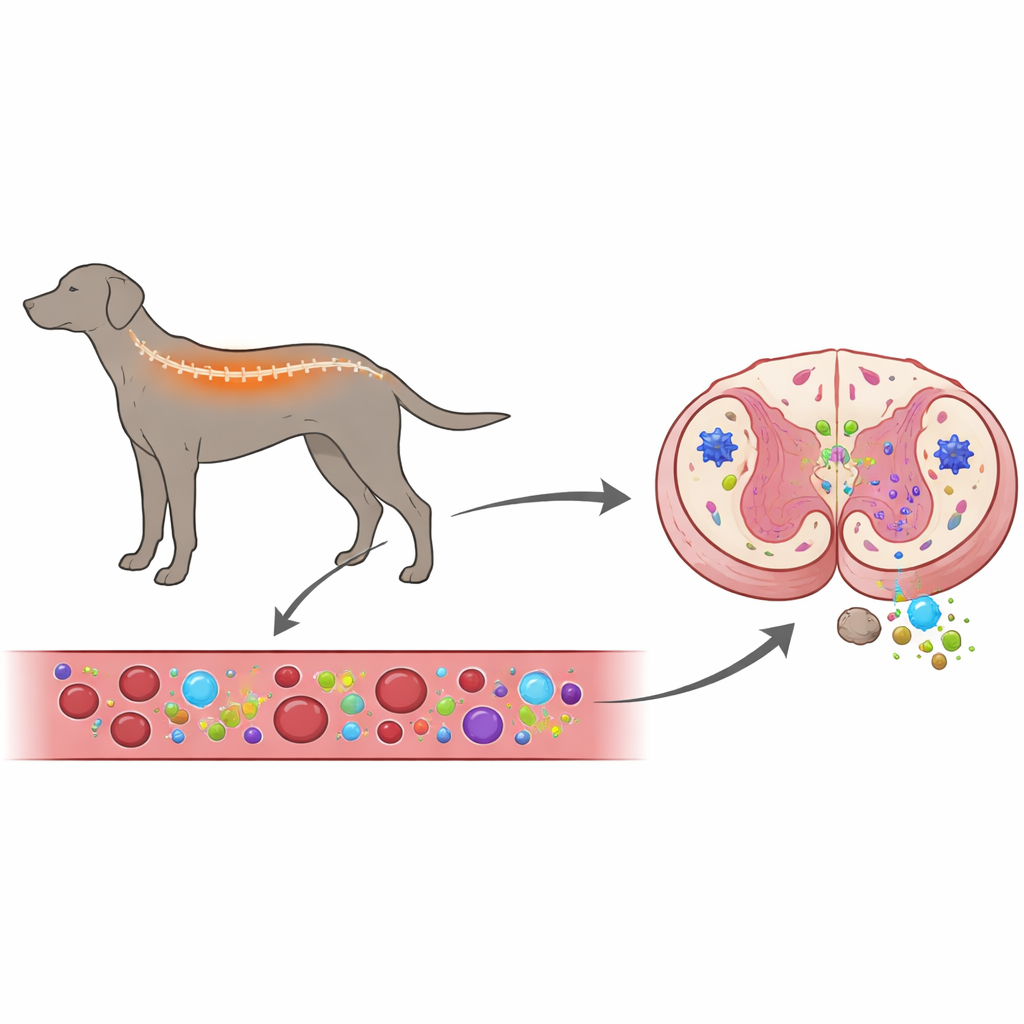
Osservare insieme sangue e midollo spinale
I ricercatori hanno voluto rispondere a una domanda centrale: il sistema immunitario contribuisce a causare questa malattia nei cani, oppure reagisce principalmente al danno nervoso già in atto? Per esplorarlo, hanno esaminato sia il sangue che i midolli spinali di cani con mielopatia degenerativa, confrontandoli con cani sani e con cani affetti da un altro problema spinale, l’ernia del disco intervertebrale, che comprime il midollo dall’esterno. Hanno misurato l’attività dei geni legati all’infiammazione nelle cellule del sangue e nei tessuti midollari, e hanno usato colorazioni con anticorpi fluorescenti per vedere quali cellule immunitarie e di supporto fossero presenti nel midollo e quanto fossero attive.
Segnali di allarme immunitario nel sangue
Nel sangue dei cani colpiti, il team ha rilevato segnali che alcune cellule bianche erano passate a uno stato di “allerta”. I geni collegati a un sistema d’allarme molecolare noto come inflammasoma, che promuove la produzione di mediatori infiammatori, erano più attivi rispetto agli animali di controllo. Allo stesso tempo, anche un gene per una molecola “freno” immunitaria che tende a calmare l’infiammazione risultava più attivo, suggerendo che l’organismo stava cercando di contenere questo allarme. Gli esami del sangue di routine, tuttavia, apparivano normali: conteggi leucocitari e un marcatore infiammatorio comune, la proteina C-reattiva, rimanevano nei limiti tipici. Questo quadro indica un’attivazione immunitaria sottile e finemente regolata piuttosto che una vera e propria esplosione infiammatoria sistemica.
Chi entra nel midollo spinale e chi resta fuori
La questione successiva era se le cellule del sangue attivate effettivamente penetrassero nel midollo spinale, come avviene in alcuni modelli murini di SLA. Utilizzando marcatori cellulari in grado di distinguere le cellule immunitarie residenti nel cervello dai nuovi arrivati dal sangue, gli scienziati hanno osservato solo una manciata di probabili cellule immigrate in ciascuna sezione trasversale del midollo affetto. In altre parole, c’erano prove che alcune cellule di origine ematica entrassero nel tessuto nervoso, ma in numeri molto ridotti. Allo stesso tempo, hanno riscontrato un aumento della produzione di un segnale chimico nel midollo che normalmente attrae tali cellule dal sangue, indicando che il tessuto stesso chiedeva aiuto anche se arrivavano solo pochi rispondenti.
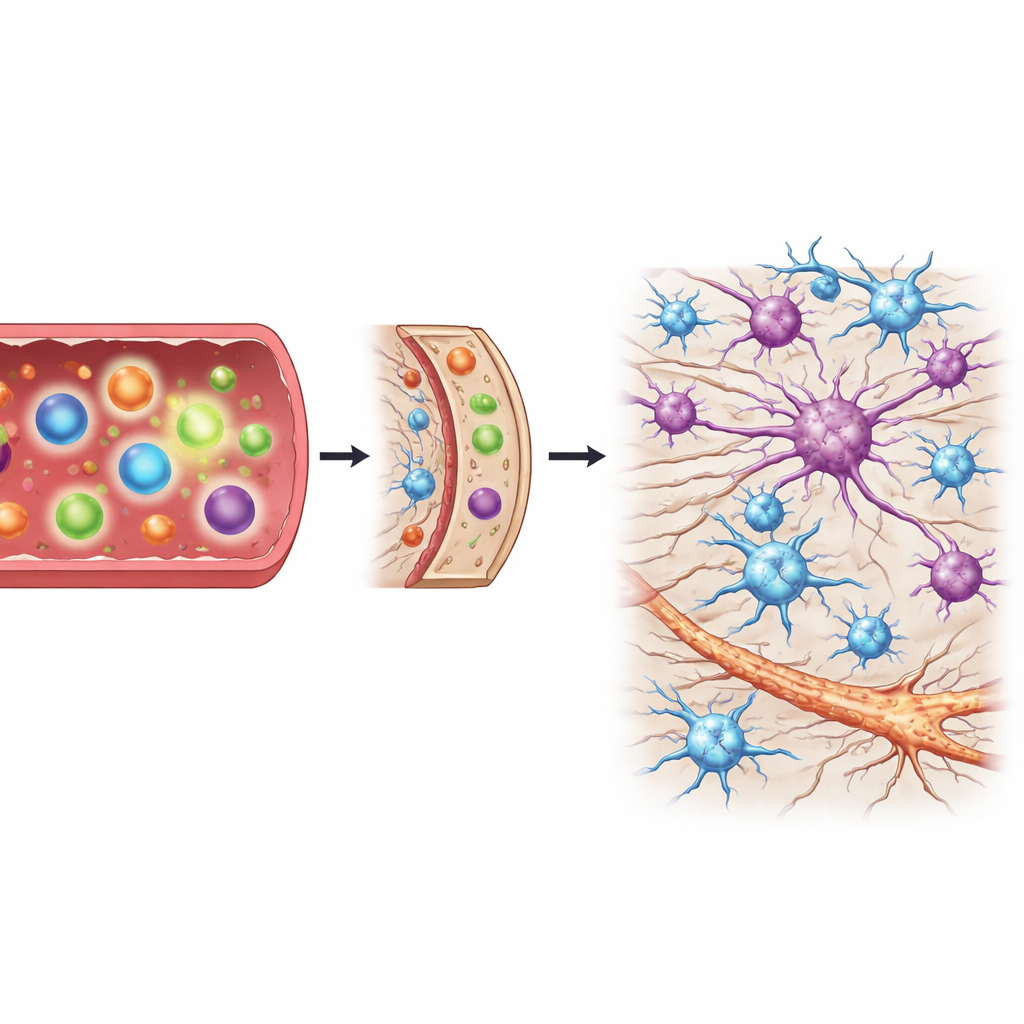
Le cellule di supporto reagiscono con l’aggravarsi del danno
Il midollo spinale contiene non solo fibre nervose ma anche cellule di supporto chiamate astrociti e microglia, che possono proteggere o danneggiare i neuroni a seconda del loro stato. Raggruppando i campioni di midollo in base al grado di danno — da assente, a lieve, a moderato, a grave — il team ha potuto tracciare come queste cellule di supporto cambiassero nel tempo. Con l’avanzare della degenerazione, i geni che contrassegnano sia le forme dannose sia quelle protettive di astrociti aumentavano nettamente, e la chemochina che richiama le cellule immunitarie diventava più attiva. Al contrario, i marcatori di microglia attivata non mostravano forti aumenti precoci quando il danno era ancora lieve. Questo calendario suggerisce che la grande ondata di attivazione degli astrociti e di segnalazione immunitaria compare dopo che il danno nervoso è già in atto, piuttosto che all’inizio del processo.
Cosa significa per cani e persone
Complessivamente, i risultati delineano un quadro in cui la mielopatia degenerativa coinvolge un cambiamento immunitario silenzioso ma complesso: le cellule del sangue sono pronte, il midollo spinale invia segnali di soccorso e le cellule di supporto locali reagiscono intensamente con l’accumularsi del danno. Tuttavia, l’invasione effettiva di cellule immunitarie dal sangue nel midollo rimane limitata, e i cambiamenti infiammatori drammatici emergono soprattutto nelle fasi avanzate. Per i proprietari di cani, questo significa che quando compaiono i segni evidenti della malattia, le modificazioni immunitarie sono più una risposta alla perdita neuronale che la causa originaria. Per la medicina umana, questi casi naturali nei cani suggeriscono che nelle malattie di tipo SLA modulare l’infiammazione può comunque essere utile, ma terapie che mirano solo a impedire l’ingresso delle cellule immunitarie nel sistema nervoso sono probabilmente insufficienti a fermare la malattia alla radice. Piuttosto, i trattamenti potrebbero dover mirare alla vulnerabilità nervosa sottostante, modulando con attenzione — e non semplicemente spegnendo — la risposta immunitaria dell’organismo.
Citazione: Yokota, S., Kobatake, Y., Yoshida, K. et al. Analysis of immune-related alterations in blood and spinal cord of canine degenerative myelopathy, a spontaneous model of amyotrophic lateral sclerosis. Sci Rep 16, 13494 (2026). https://doi.org/10.1038/s41598-026-43838-5
Parole chiave: mielopatia degenerativa, sclerosi laterale amiotrofica, neuroinfiammazione, modello canino, risposta immunitaria