Clear Sky Science · pl
Analiza zmian związanych z układem odpornościowym we krwi i rdzeniu kręgowym u psiej zwyrodnieniowej mielopatii, spontanicznego modelu stwardnienia zanikowego bocznego
Dlaczego choroba psów ma znaczenie dla ludzi
Wiele starszych psów, zwłaszcza Pembroke Welsh Corgi, może rozwijać śmiertelną chorobę kręgosłupa zwaną zwyrodnieniową mielopatią. Schorzenie to stopniowo odbiera im zdolność chodzenia, a ostatecznie także oddychania. Co istotne, bardzo przypomina stwardnienie zanikowe boczne (ALS) u ludzi, znane też jako choroba Lou Gehriga. Ponieważ psy naturalnie rozwijają tę chorobę i dzielą z niektórymi pacjentami ALS istotną mutację genową, badanie ich może ujawnić, jak uszkodzenie układu nerwowego i reakcje obronne organizmu oddziałują ze sobą w warunkach naturalnych, wykraczając poza obserwacje z inżynieryjnych modeli mysich.
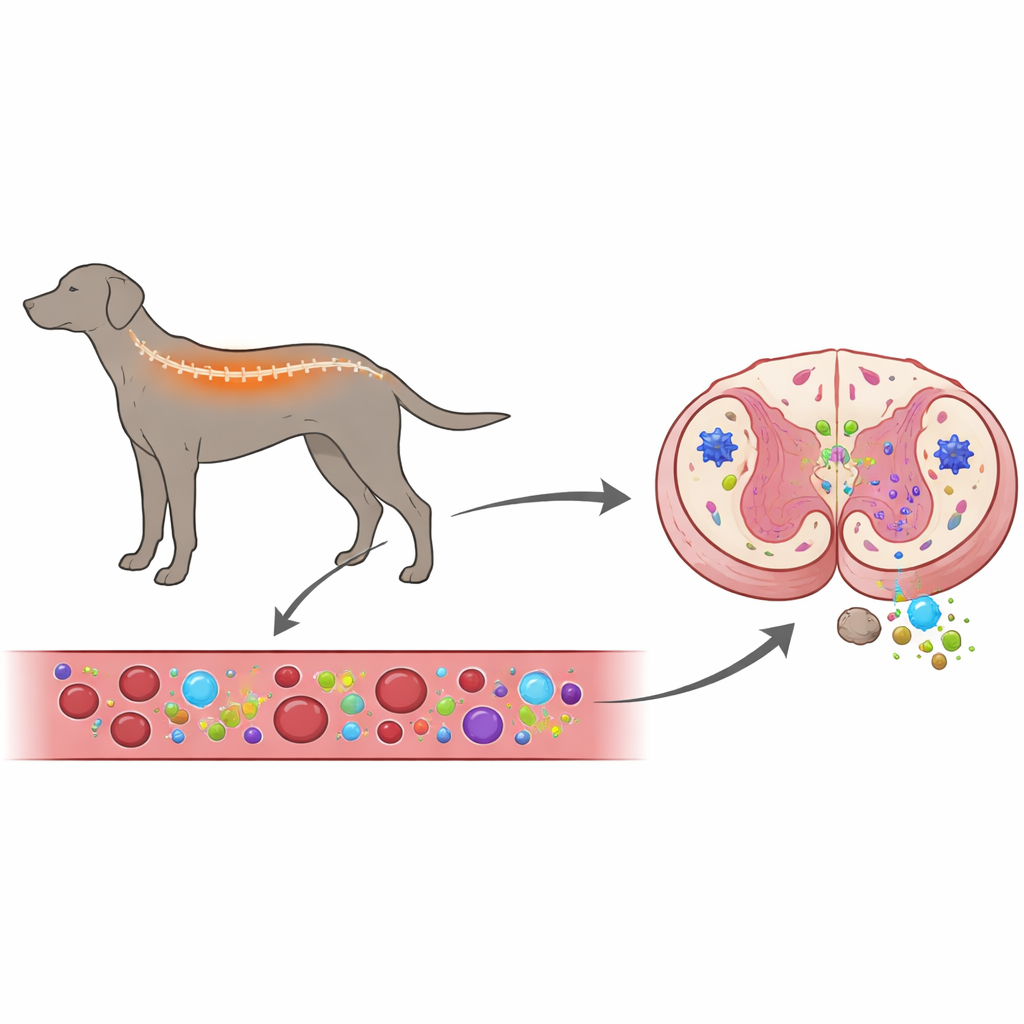
Badanie krwi i rdzenia jednocześnie
Naukowcy postanowili odpowiedzieć na kluczowe pytanie: czy układ odpornościowy napędza tę chorobę u psów, czy raczej reaguje na już toczące się uszkodzenie nerwów? Aby to sprawdzić, zbadali zarówno krew, jak i rdzenie kręgowe psów z zwyrodnieniową mielopatią i porównali je ze zdrowymi psami oraz z psami cierpiącymi na inny problem kręgosłupa — przepuklinę międzykręgową, która uciska rdzeń z zewnątrz. Mierzyli aktywność genów związanych z zapaleniem w komórkach krwi i tkance rdzenia oraz używali znakowanych przeciwciał do zobrazowania, jakie komórki odpornościowe i podporowe występują w rdzeniu i jak są aktywne.
Sygnały alarmowe układu odpornościowego we krwi
We krwi chorych psów zespół odkrył oznaki, że niektóre białe krwinki znalazły się w stanie „czujności”. Były bardziej aktywne geny powiązane z molekularnym systemem alarmowym zwanym inflamasomem, który pomaga wytwarzać mediatory zapalne. Jednocześnie zwiększona była aktywność genu kodującego cząsteczkę hamującą odpowiedź immunologiczną, która zwykle łagodzi zapalenie, co sugeruje, że organizm próbował utrzymać alarm pod kontrolą. Standardowe badania krwi wyglądały jednak normalnie: liczba białych krwinek i powszechny marker zapalenia — białko C-reaktywne — mieściły się w typowych granicach. Ten wzorzec wskazuje na subtelną, ściśle regulowaną aktywację układu odpornościowego, a nie na pełnoskalowy, ogólnoustrojowy napływ zapalny.
Kto wchodzi do rdzenia kręgowego, a kto zostaje na zewnątrz
Następną kwestią było, czy aktywowane komórki krwi rzeczywiście napływają do rdzenia kręgowego, jak to bywa w niektórych modelach mysich ALS. Przy użyciu markerów komórkowych, które rozróżniają rezydentne komórki odpornościowe mózgu od przybyszów z krwi, naukowcy zauważyli zaledwie garść prawdopodobnych imigrantów w całym przekroju badanego rdzenia. Innymi słowy, znaleziono dowody na to, że niektóre komórki pochodzenia krwiowego wniknęły do tkanki nerwowej, ale w bardzo niewielkiej liczbie. Jednocześnie stwierdzono zwiększoną produkcję sygnału chemicznego w rdzeniu, który zwykle przyciąga takie komórki z krwiobiegu, co wskazuje, że sama tkanka wzywała pomoc, nawet jeśli odpowiedzi przybyło niewiele.
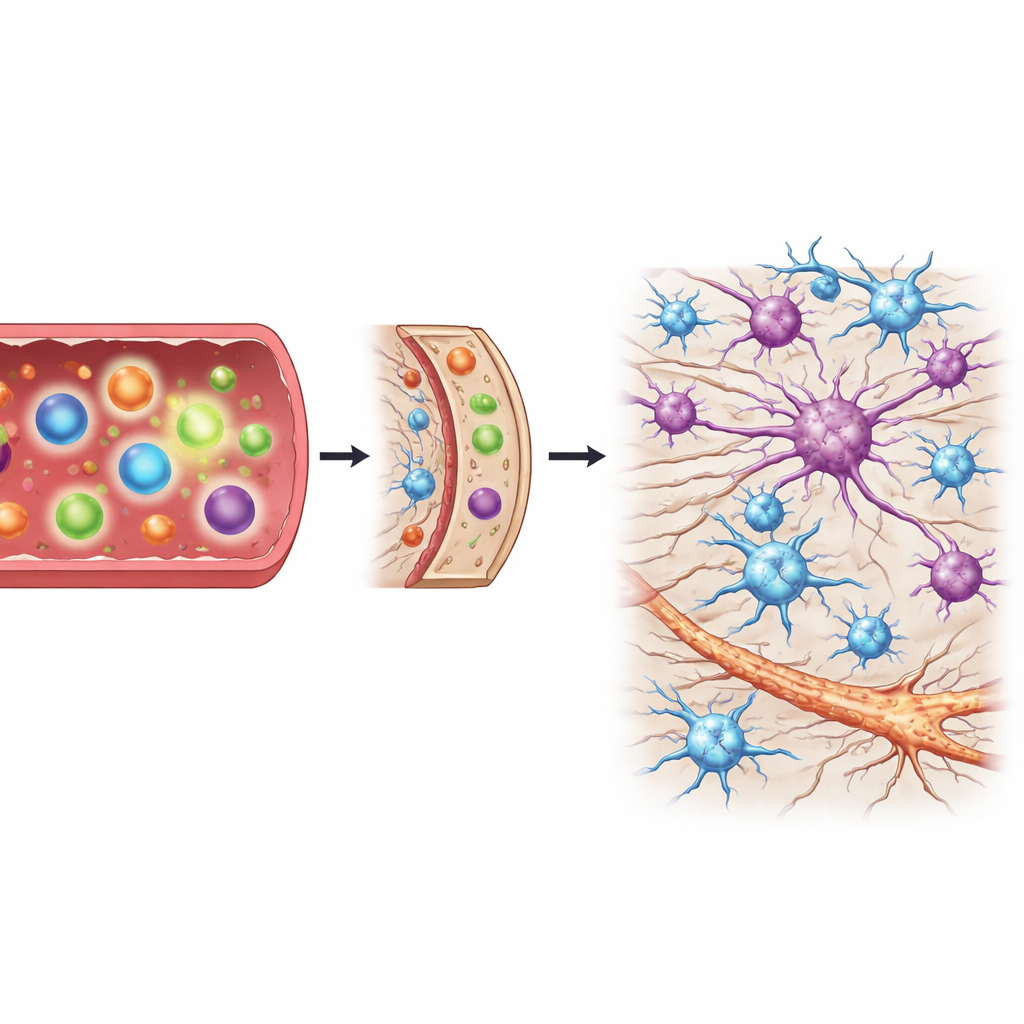
Komórki podporowe reagują w miarę nasilania się uszkodzeń
Rdzeń kręgowy zawiera nie tylko włókna nerwowe, ale także komórki podporowe zwane astrocytami i mikroglejem, które w zależności od stanu mogą chronić lub szkodzić neuronom. Grupując próbki rdzenia zgodnie z nasileniem uszkodzeń — od braku zmian, przez łagodne i umiarkowane, aż po ciężkie — zespół mógł śledzić, jak te komórki podporowe zmieniają się w czasie. W miarę postępu degeneracji gwałtownie wzrastała aktywność genów oznaczających zarówno szkodliwe, jak i ochronne formy astrocytów, a także zwiększała się aktywność chemokiny przyciągającej komórki odpornościowe. Natomiast markery aktywacji mikrogleju nie wykazywały silnych, wczesnych wzrostów, gdy uszkodzenia były jeszcze łagodne. Taka kolejność zdarzeń sugeruje, że duża fala aktywacji astrocytów i sygnalizacji immunologicznej pojawia się po tym, jak uszkodzenie nerwów już się zadomowi, a nie na jego samym początku.
Co to oznacza dla psów i ludzi
Podsumowując, wyniki układają się w obraz, w którym zwyrodnieniowa mielopatia wiąże się ze spokojną, ale złożoną zmianą immunologiczną: komórki krwi są przygotowane do działania, rdzeń kręgowy wysyła sygnały alarmowe, a lokalne komórki podporowe silnie reagują w miarę narastania uszkodzeń. Jednocześnie faktyczna inwazja komórek odpornościowych z krwi do rdzenia pozostaje ograniczona, a dramatyczne zmiany zapalne ujawniają się głównie w późniejszych stadiach. Dla opiekunów psów oznacza to, że w momencie pojawienia się widocznych objawów choroby zmiany immunologiczne są bardziej odpowiedzią na utratę neuronów niż jej pierwotną przyczyną. Dla medycyny ludzkiej naturalnie występujące przypadki u psów sugerują, że tłumienie zapalenia może nadal przynosić korzyść, lecz terapie skoncentrowane wyłącznie na blokowaniu napływu komórek odpornościowych do układu nerwowego raczej nie zatrzymają choroby u źródła. Zamiast tego leczenie może wymagać ukierunkowania na pierwotną wrażliwość neuronów przy jednoczesnym ostrożnym modulowaniu, a nie prostym wyłączaniu, odpowiedzi immunologicznej organizmu.
Cytowanie: Yokota, S., Kobatake, Y., Yoshida, K. et al. Analysis of immune-related alterations in blood and spinal cord of canine degenerative myelopathy, a spontaneous model of amyotrophic lateral sclerosis. Sci Rep 16, 13494 (2026). https://doi.org/10.1038/s41598-026-43838-5
Słowa kluczowe: zwyrodnieniowa mielopatia, stwardnienie zanikowe boczne, ne Zapalenie układu nerwowego, model psów, odpowiedź immunologiczna