Clear Sky Science · zh
外泌体介导递送miRNA-1290抑制剂增强前列腺癌中JNK依赖的组织驻留记忆T细胞免疫
为什么这项研究重要
对许多男性而言,前列腺癌是一种缓慢发展的威胁,但一旦对常规治疗失去反应,就可能迅速变成致命疾病。本研究探索了一种新的方法,利用细胞释放的微小天然递送囊泡将遗传“关闭开关”直接运送到肿瘤中,从而重新唤醒机体自身的免疫系统。该研究指向这样一种未来:前列腺癌的控制不仅依赖直接作用于肿瘤的药物,还可以通过有针对性地重新武装驻留于肿瘤内部的免疫细胞来实现。
一个小的遗传开关却有大影响
研究的核心是一段称为miRNA-1290的短小遗传物质。此类微小RNA可同时微调多种基因的表达,既能促进也能抑制癌症。早期工作将高水平miRNA-1290与侵袭性肿瘤联系起来,但其在前列腺癌中的作用及作为治疗靶点的价值尚不明确。作者首先证实miRNA-1290在小鼠前列腺肿瘤中确实升高。随后他们设计了一种匹配的“抑制剂”,可与miRNA-1290结合并阻断其功能,期望通过关闭它来减缓肿瘤生长并改变肿瘤内部免疫细胞的行为。
微小快递:外泌体作为递送载体
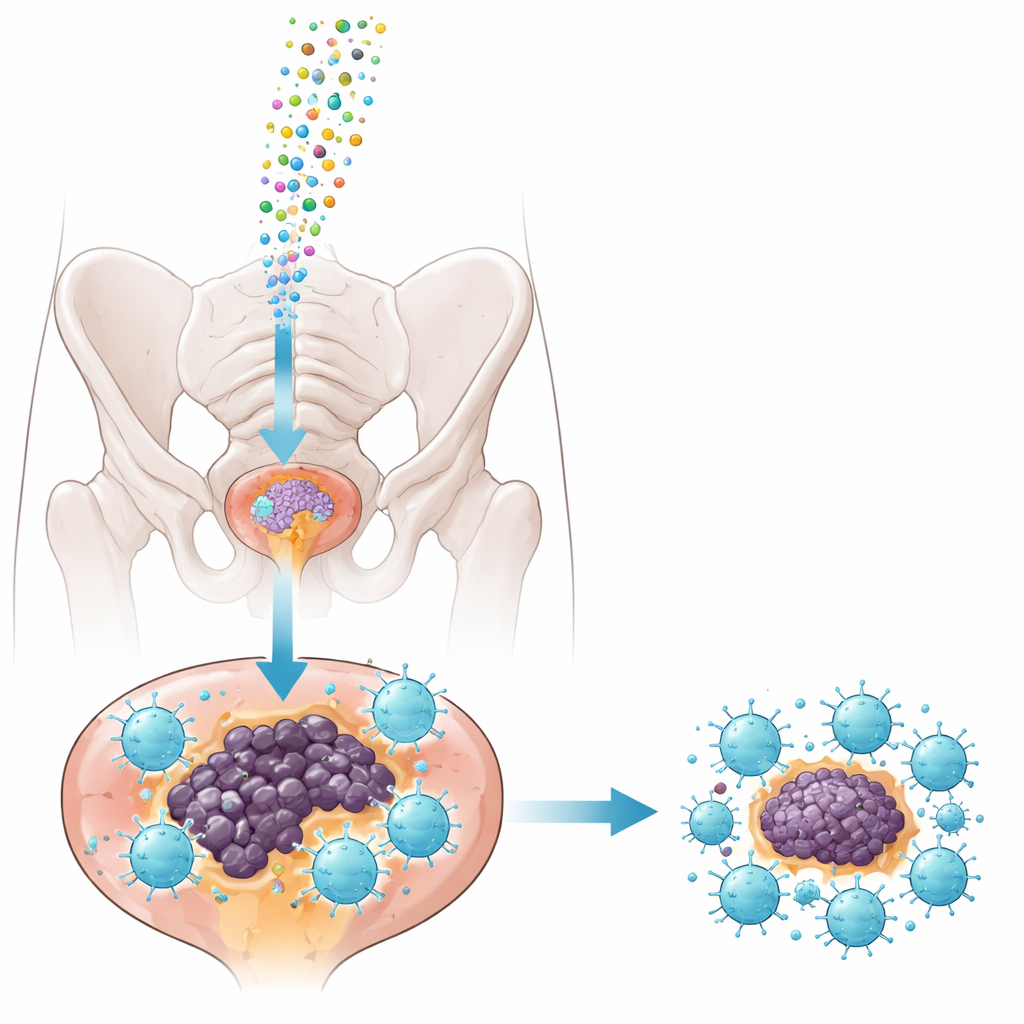
为将抑制剂安全输送至肿瘤,研究团队转向外泌体——细胞自然释放的纳米级囊泡,可携带RNA货物。他们从小鼠前列腺癌细胞系中提取外泌体,仔细纯化,并将其装载miRNA-1290抑制剂或无害的对照序列。检测显示,外泌体尺寸均一,保留了常见表面标志,且在直接注入成熟的小鼠前列腺肿瘤(TRAMP小鼠模型)后可被肿瘤组织有效摄取。重要的是,在所用剂量下,治疗并未扰动健康动物的肝肾功能或体重,提示该方法相对安全。
肿瘤增速放慢,本地免疫更强
接受装载miRNA-1290抑制剂外泌体治疗的肿瘤负荷小鼠,其肿瘤生长变慢,体重稳定或改善,生存期也优于接受空载或对照外泌体的对照组。抑制剂显著降低了肿瘤内miRNA-1290的水平,但在血液或主要器官中未见下降,表明作用高度局部化。为揭示肿瘤内部变化,研究者对数千个单个免疫细胞进行了单细胞RNA测序,并用流式细胞术验证结果。他们发现总体T细胞、杀伤性CD8 T细胞特别是被称为组织驻留记忆T细胞(Trm)的一类显著增加。Trm细胞长期驻留于组织并能迅速响应危险信号,这些细胞的基因表达模式富集了炎症和适应性免疫通路,提示抗肿瘤反应更为积极。
一种信号通路如何驱动记忆T细胞
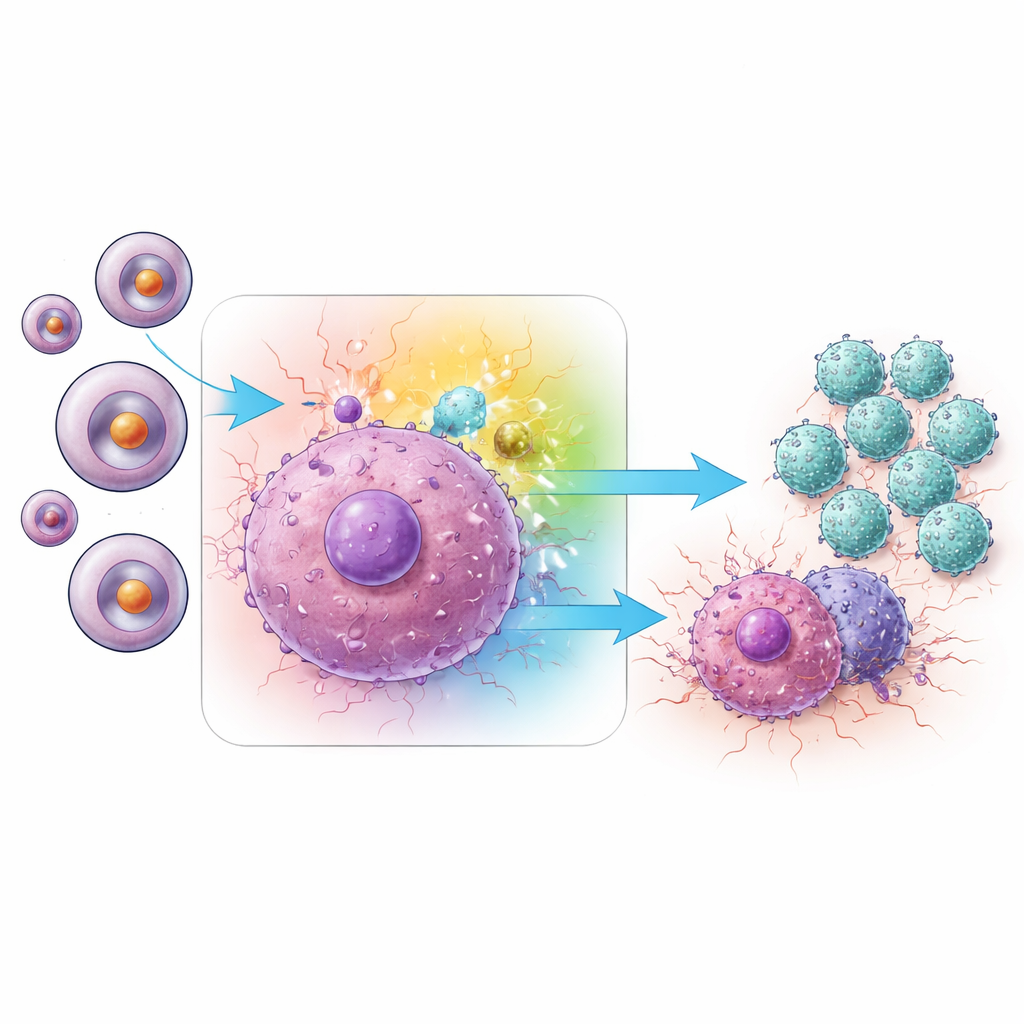
进一步研究中,团队探寻了哪些Trm细胞内的信号通路负责这种增强活性。分析指向了MAPK通路,尤其是名为JNK的分支。在接受miRNA-1290抑制剂处理的肿瘤中,Trm细胞显示出更高水平的活化(磷酸化)JNK。与此同时,肿瘤中含有更多促炎性信使蛋白,如IFN-γ和TNF-α,这些是CD8 T细胞杀伤癌细胞的典型工具。当研究者选择性阻断不同的MAPK分支时,发现抑制JNK——而非相关的ERK或p38——会大幅减少这些关键细胞因子的产生。用小干扰RNA沉默Trm细胞中的JNK亦产生相同的抑制效果,确立了JNK活性与miRNA-1290抑制所触发的增强免疫攻击之间的直接联系。
这对未来治疗可能意味着什么
综合来看,将miRNA-1290抑制剂装入外泌体并注入前列腺肿瘤,既能减缓癌症生长,又能唤醒以组织驻留记忆T细胞及其JNK信号为中心的强大且持久的局部免疫反应。尽管这些实验在小鼠中进行并采用了直接肿瘤注射——这对所有病人未必可行——但该工作提供了明确的原理验证。研究表明miRNA-1290既是前列腺癌的推动因子,也是重塑肿瘤免疫环境的杠杆,并暗示基于外泌体的RNA药物可能成为一类新疗法,帮助免疫系统控制前列腺癌。
引用: Liang, B., Zou, S. Exosome-mediated delivery of miRNA-1290 inhibitor enhances JNK-dependent tissue-resident memory T cell immunity in prostate cancer. Sci Rep 16, 13472 (2026). https://doi.org/10.1038/s41598-026-43719-x
关键词: 前列腺癌, microRNA治疗, 外泌体, 肿瘤免疫反应, 组织驻留记忆T细胞