Clear Sky Science · sv
Exosommedierad leverans av miRNA‑1290‑hämmare förstärker JNK‑beroende vävnadsresident minnes‑T‑cellsimmunitet vid prostatacancer
Varför denna forskning är viktig
För många män är prostatacancer ett långsamt växande hot som plötsligt kan bli livshotande när den slutar svara på standardbehandlingar. Denna studie undersöker ett nytt sätt att få kroppens eget immunsystem att åter rikta sig mot sjukdomen, genom att använda cellernas egna små leveranspaket för att föra en genetisk "avstängningsknapp" direkt in i tumörer. Arbetet pekar mot en framtid där prostatacancer kanske kan kontrolleras inte bara med läkemedel som angriper tumörcellerna, utan också genom att omsorgsfullt ombeväpna de immunceller som lever inuti tumören.
En liten genetisk brytare med stor effekt
I studiens centrum står en kort genetisk bit kallad miRNA‑1290. Sådana mikroRNA fungerar som finjusterare av många gener samtidigt och kan antingen främja eller hämma cancer. Tidigare studier hade kopplat höga nivåer av miRNA‑1290 till aggressiva tumörer, men dess roll i prostatacancer och dess värde som behandlingsmål var fortfarande oklara. Författarna bekräftade först att miRNA‑1290 faktiskt är förhöjt i museprostatatumörer. De designade sedan en matchande "hämmare" som binder till miRNA‑1290 och blockerar dess funktion, i hopp om att stänga ner den skulle bromsa tumörtillväxt och förändra hur immunceller beter sig i tumören.
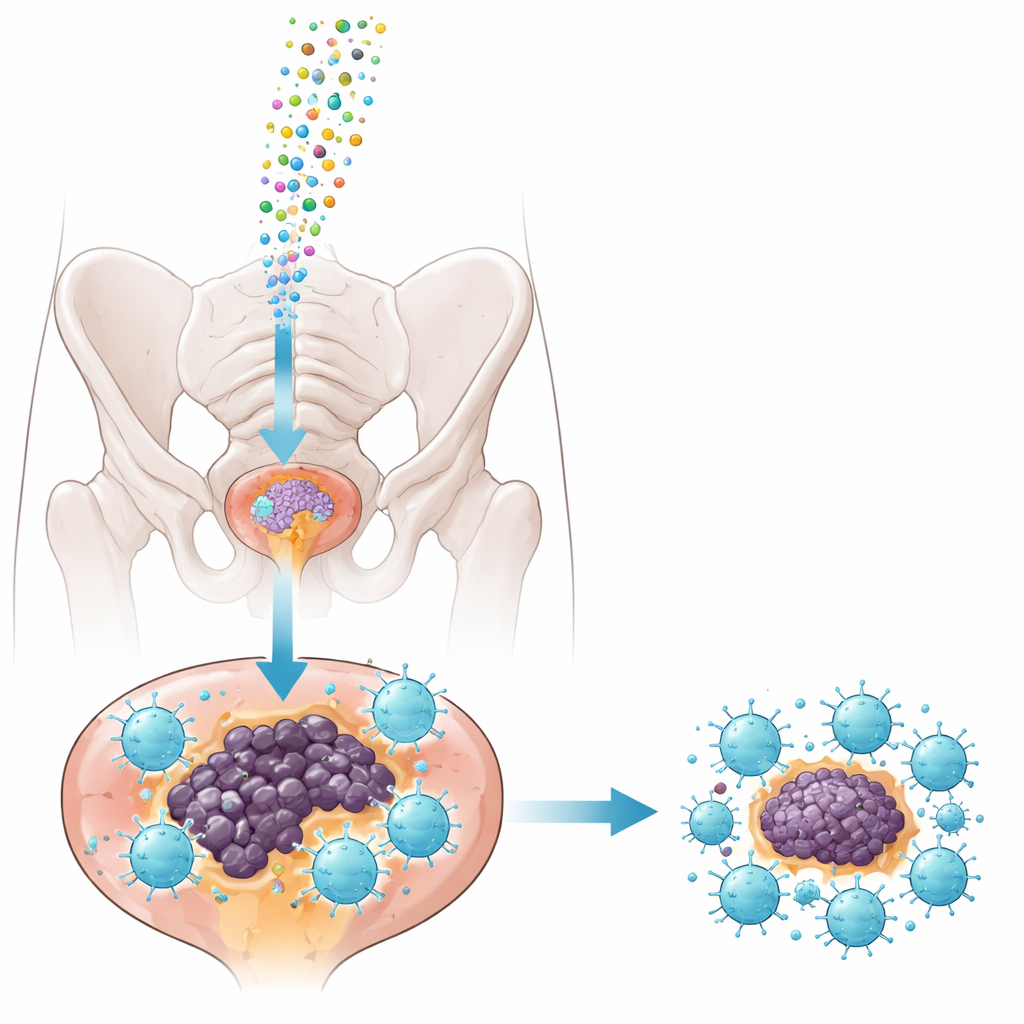
Små kurirer: exosomer som leveransfordon
För att få hämmaren säkert in i tumörerna vände teamet sig till exosomer—nanoskala bubblor som naturligt släpps ut av celler och kan bära RNA‑last. De skördade exosomer från en museprostatacancercellinje, renade dem noggrant och lastade dem med antingen miRNA‑1290‑hämmaren eller en ofarlig kontrollsekvens. Tester visade att exosomerna var enhetliga i storlek, behöll sina vanliga ytmarkörer och togs lätt upp av tumörvävnad när de injicerades direkt i prostatatumörer i en väl etablerad musemodell (TRAMP‑möss). Viktigt är att behandlingen inte störde lever‑ eller njurfunktion eller kroppsvikt hos friska djur, vilket tyder på att tillvägagångssättet är relativt säkert vid de använda doserna.
Trögare tumörer och starkare lokal immunitet
När tumörbärande möss fick exosomer som bar miRNA‑1290‑hämmaren växte deras cancer långsammare, kroppsvikten stabiliserades eller förbättrades och de levde längre än kontrollgrupper som fick tomma eller kontroll‑lastade exosomer. Hämmaren minskade kraftigt miRNA‑1290‑nivåerna i själva tumören men inte i blod eller viktiga organ, vilket visar att effekten var starkt lokaliserad. För att förstå vad som skedde inne i tumörerna profilerade forskarna tusentals enskilda immunceller med single‑cell RNA‑sekvensering och bekräftade fynden med flödescytometri. De såg en markant ökning av totalt antal T‑celler, av cytotoxiska CD8‑T‑celler och särskilt av en specialiserad undergrupp kallad vävnadsresidenta minnes‑T‑celler (Trm), som bosätter sig långsiktigt i vävnader och kan svara snabbt på hot. Genaktivitetsmönster i dessa celler visade berikning av inflammatoriska och adaptiva immunvägar, förenligt med ett mer aggressivt antitumörsvar.
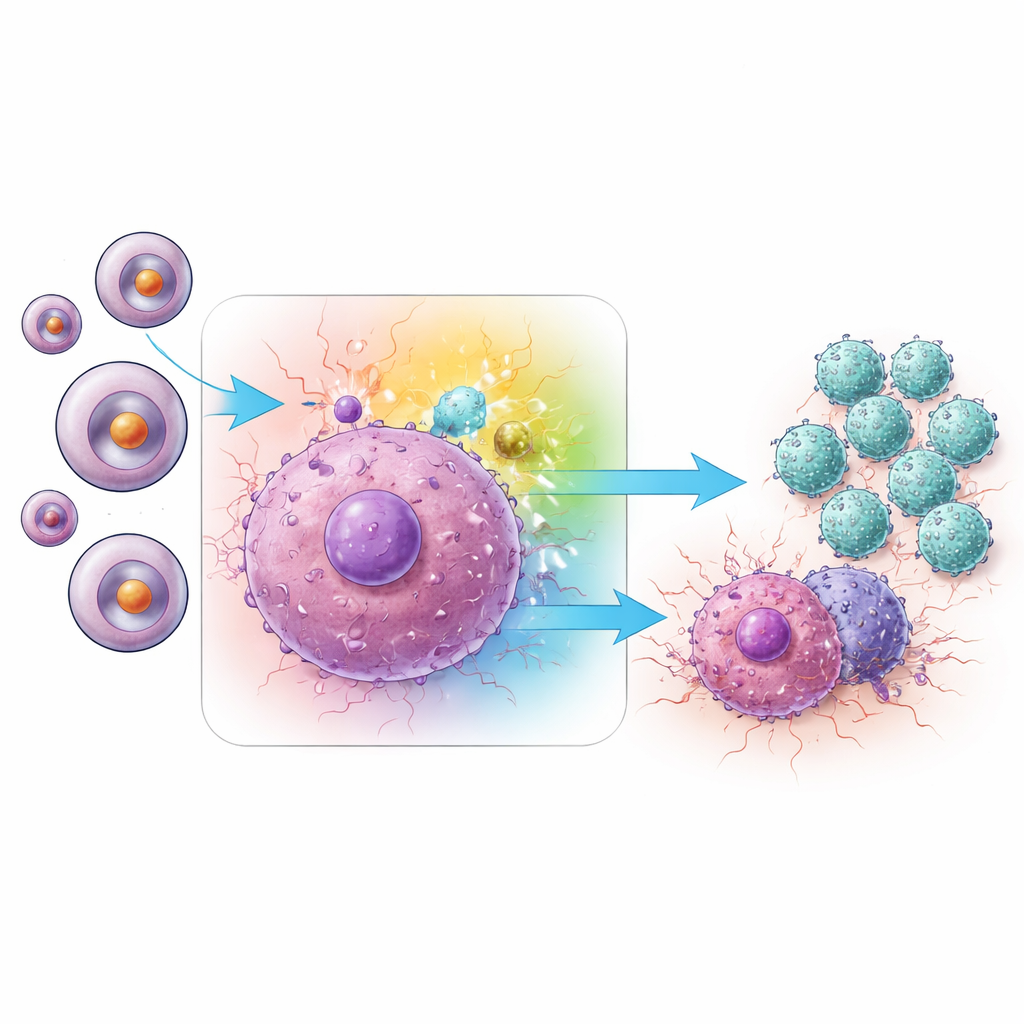
Hur en signalväg driver minnes‑T‑celler
För att gå djupare frågade teamet vilka interna signalvägar i Trm‑celler som stod för den ökade aktiviteten. Deras analyser pekade på MAPK‑nätverket, och särskilt på en gren känd som JNK. I tumörer behandlade med miRNA‑1290‑hämmaren visade Trm‑celler högre nivåer av aktiverad (fosforylerad) JNK jämfört med kontroller. Samtidigt innehöll tumörerna mer av flera proinflammatoriska budbärarproteiner, inklusive IFN‑γ och TNF‑α, vilka är klassiska vapen som CD8‑T‑celler använder för att döda cancerceller. När forskarna selektivt blockerade olika MAPK‑grenar fann de att nedstängning av JNK—men inte två närbesläktade grenar, ERK eller p38—kraftigt minskade produktionen av dessa nyckelcytokiner. Att tysta JNK med små interfererande RNA i Trm‑celler gav samma dämpande effekt, vilket tydligt länkar JNK‑aktivitet till det förstärkta immunsvaret som triggas av miRNA‑1290‑inhibering.
Vad detta kan innebära för framtida vård
Tillsammans visar resultaten att paketering av en miRNA‑1290‑hämmare i exosomer och injektion i prostatatumörer kan bromsa tumörtillväxt samtidigt som det väcker ett kraftfullt, långvarigt lokalt immunsvar centrerat på vävnadsresidenta minnes‑T‑celler och deras JNK‑signalering. Även om experimenten utfördes i möss och med direkta tumörinjektioner—vilket kanske inte är praktiskt för alla patienter—ger arbetet ett tydligt proof of principle. Det tyder på att miRNA‑1290 både driver prostatacancer och kan användas för att omforma tumörens immummiljö, och att exosombaserade RNA‑läkemedel skulle kunna bli en ny klass terapier som hjälper immunsystemet att hålla prostatacancer i schack.
Citering: Liang, B., Zou, S. Exosome-mediated delivery of miRNA-1290 inhibitor enhances JNK-dependent tissue-resident memory T cell immunity in prostate cancer. Sci Rep 16, 13472 (2026). https://doi.org/10.1038/s41598-026-43719-x
Nyckelord: prostatacancer, microRNA‑terapi, exosomer, tumörens immunsvar, vävnadsresidenta minnes‑T‑celler