Clear Sky Science · it
Consegna mediata da esosomi di un inibitore di miRNA‑1290 potenzia l’immunità delle cellule T residenti tissutali dipendente da JNK nel cancro della prostata
Perché questa ricerca è importante
Per molti uomini il cancro della prostata è una minaccia che progredisce lentamente ma che può diventare improvvisamente letale quando smette di rispondere ai trattamenti standard. Questo studio esplora un nuovo modo per riportare il sistema immunitario dell’organismo contro la malattia, impiegando minuscoli pacchetti naturali rilasciati dalle cellule per trasportare direttamente nei tumori un “interruttore” genetico. Il lavoro indica un futuro in cui il cancro della prostata potrebbe essere controllato non solo da farmaci che agiscono sul tumore, ma anche rinnovando con precisione le difese immunitarie che risiedono al suo interno.
Un piccolo interruttore genetico dall’impatto grande
Al centro dello studio c’è un breve frammento di materiale genetico chiamato miRNA‑1290. I microRNA agiscono come regolatori di precisione di molti geni contemporaneamente e possono promuovere o inibire il cancro. Studi precedenti avevano collegato livelli elevati di miRNA‑1290 a tumori aggressivi, ma il suo ruolo nel cancro prostatico e il suo valore come bersaglio terapeutico restavano incerti. Gli autori hanno prima confermato che miRNA‑1290 è effettivamente aumentato nei tumori prostatici murini. Hanno poi progettato un “inibitore” complementare che si lega a miRNA‑1290 e ne blocca l’azione, con l’ipotesi che spegnerlo rallentasse la crescita tumorale e modificasse il comportamento delle cellule immunitarie all’interno del cancro.
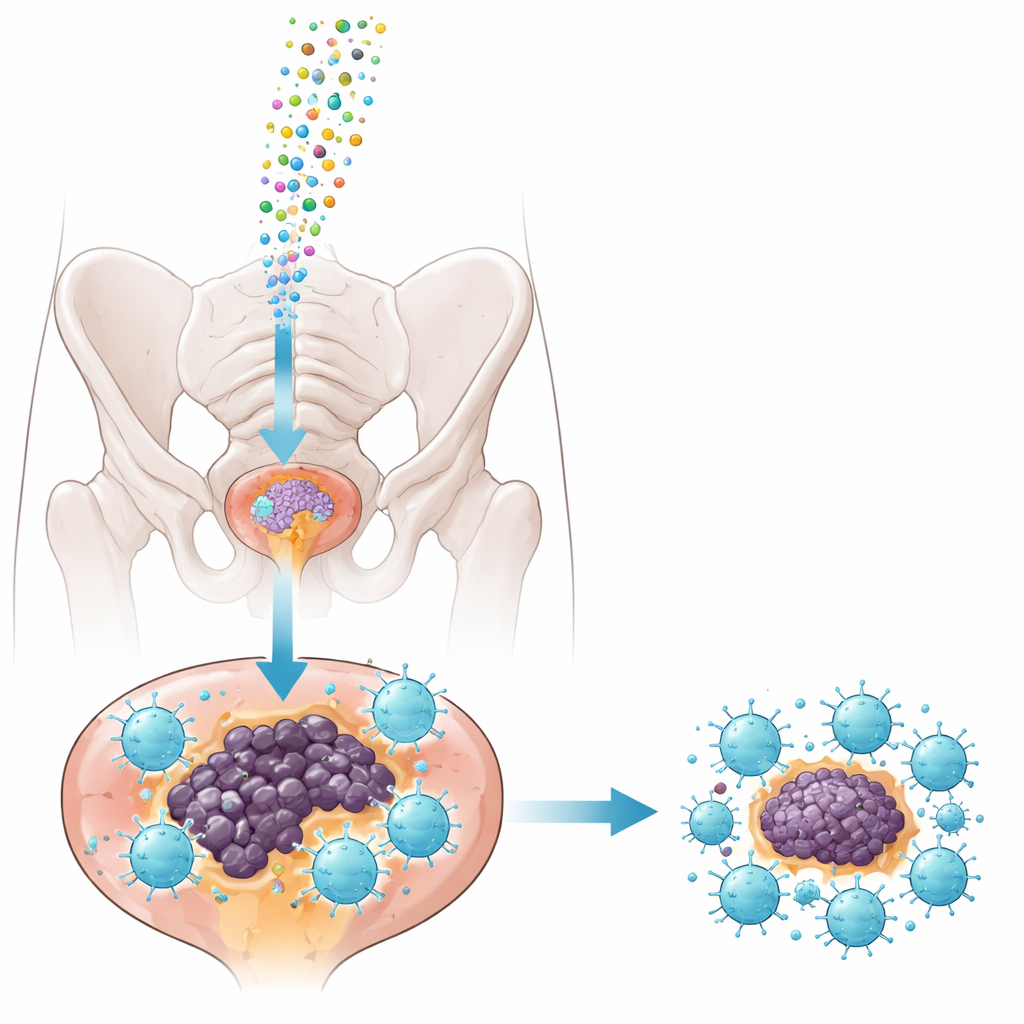
Piccoli corrieri: gli esosomi come veicoli di consegna
Per veicolare in sicurezza l’inibitore nei tumori, il gruppo si è rivolto agli esosomi—bolle nanoscalari rilasciate naturalmente dalle cellule che possono trasportare RNA. Hanno isolato esosomi da una linea cellulare di cancro prostatico murino, li hanno purificati con cura e caricati con l’inibitore di miRNA‑1290 o con una sequenza di controllo innocua. I test hanno mostrato che gli esosomi avevano dimensioni uniformi, mantenevano i normali marcatori di superficie e venivano prontamente assorbiti dal tessuto tumorale quando iniettati direttamente nei tumori prostatici in un modello murino consolidato (topi TRAMP). È importante che il trattamento non abbia alterato la funzione epatica o renale né il peso corporeo negli animali sani, suggerendo che l’approccio è relativamente sicuro alle dosi utilizzate.
Tumori più lenti e immunità locale più forte
Quando i topi portatori di tumore hanno ricevuto esosomi contenenti l’inibitore di miRNA‑1290, i loro tumori sono cresciuti più lentamente, il peso corporeo si è stabilizzato o è migliorato e hanno vissuto più a lungo rispetto agli animali di controllo che avevano ricevuto esosomi vuoti o caricati con controllo. L’inibitore ha ridotto drasticamente i livelli di miRNA‑1290 nel tumore stesso ma non nel sangue o negli organi principali, indicando che l’effetto era altamente localizzato. Per capire cosa stesse avvenendo all’interno dei tumori, i ricercatori hanno profilato migliaia di singole cellule immunitarie con RNA-seq a cellula singola e hanno confermato i risultati con citometria a flusso. Hanno osservato un netto aumento delle cellule T complessive, delle cellule T CD8 citotossiche e in particolare di una sottopopolazione speciale chiamata cellule T memoria residenti tissutali (Trm), che prendono residenza a lungo termine nei tessuti e possono rispondere rapidamente alle minacce. I pattern di attività genica in queste cellule mostravano un’arricchimento di vie infiammatorie e di immunità adattativa, coerente con una risposta anti-tumorale più vigorosa.
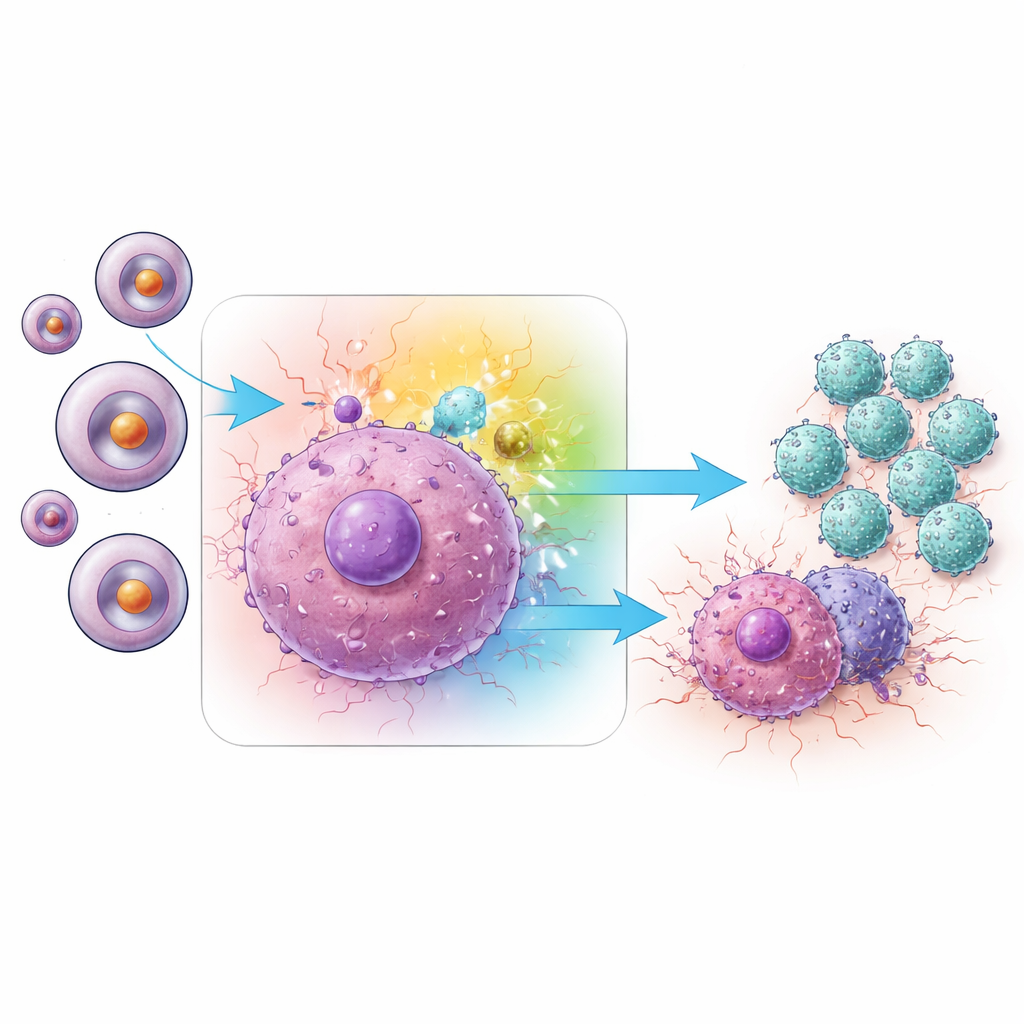
Come una via di segnalazione alimenta le cellule T memoria
Approfondendo, il team ha indagato quali vie di segnalazione interne nelle cellule Trm fossero responsabili di questa maggiore attività. Le analisi hanno indicato la rete MAPK, e in particolare un ramo noto come JNK. Nei tumori trattati con l’inibitore di miRNA‑1290, le cellule Trm mostravano livelli più alti di JNK attivato (fosforilato) rispetto ai controlli. Allo stesso tempo, i tumori contenevano maggiori quantità di diverse proteine messaggere pro‑infiammatorie, tra cui IFN‑γ e TNF‑α, armi classiche usate dalle cellule T CD8 per uccidere le cellule tumorali. Quando i ricercatori hanno bloccato selettivamente diversi rami della MAPK, hanno scoperto che l’inibizione di JNK—ma non di due rami correlati, ERK o p38—riduceva notevolmente la produzione di queste citochine chiave. L’attenuazione di JNK con RNA interferente nelle cellule Trm ha prodotto lo stesso effetto di smorzamento, collegando saldamente l’attività di JNK all’attacco immunitario potenziato indotto dall’inibizione di miRNA‑1290.
Cosa potrebbe significare per le cure future
Nel complesso, i risultati mostrano che incapsulare un inibitore di miRNA‑1290 in esosomi e iniettarlo nei tumori prostatici può rallentare la crescita tumorale risvegliando una risposta immunitaria locale potente e duratura incentrata sulle cellule T memoria residenti tissutali e sulla loro segnalazione JNK. Sebbene gli esperimenti siano stati condotti nei topi e abbiano impiegato iniezioni dirette nel tumore—una procedura che potrebbe non essere pratica per tutti i pazienti—il lavoro fornisce una chiara prova di principio. Suggerisce che miRNA‑1290 è sia un motore del cancro della prostata sia una leva per rimodellare l’ambiente immunitario tumorale, e che i farmaci a base di RNA veicolati da esosomi potrebbero diventare una nuova classe terapeutica per aiutare il sistema immunitario a tenere sotto controllo il cancro prostatico.
Citazione: Liang, B., Zou, S. Exosome-mediated delivery of miRNA-1290 inhibitor enhances JNK-dependent tissue-resident memory T cell immunity in prostate cancer. Sci Rep 16, 13472 (2026). https://doi.org/10.1038/s41598-026-43719-x
Parole chiave: cancro della prostata, terapia con microRNA, esosomi, risposta immunitaria tumorale, cellule T memoria residenti tissutali