Clear Sky Science · ru
Доставка ингибитора miRNA-1290 с помощью экзосом усиливает JNK-зависимую иммунную ответную функцию тканево-резидентных Т-клеток при раке предстательной железы
Почему это исследование важно
Для многих мужчин рак предстательной железы развивается медленно, но может внезапно стать смертельным, когда перестаёт отвечать на стандартные методы лечения. В этом исследовании рассматривается новый способ заставить собственную иммунную систему снова атаковать болезнь, используя крошечные природные «пакеты доставки» от клеток для переноса генетического «выключателя» непосредственно в опухоль. Работа указывает на будущее, в котором контроль над раком предстательной железы будет осуществляться не только препаратами, направленными на саму опухоль, но и через целенаправленную перебалансировку иммунных клеток, обитающих в ней.
Небольшой генетический переключатель с большим эффектом
В центре исследования — короткий фрагмент генетического материала, называемый miRNA-1290. Такие микроРНК действуют как тонкие регуляторы множества генов одновременно и могут либо способствовать, либо сдерживать развитие рака. Ранее повышенные уровни miRNA-1290 связывали с агрессивными опухолями, но её роль при раке предстательной железы и ценность как терапевтической мишени оставались неясными. Авторы сначала подтвердили, что miRNA-1290 действительно повышена в опухолях предстательной железы у мышей. Затем они разработали соответствующий «ингибитор», который связывается с miRNA-1290 и блокирует её активность, в надежде, что её подавление замедлит рост опухоли и изменит поведение иммунных клеток в опухолевой среде.
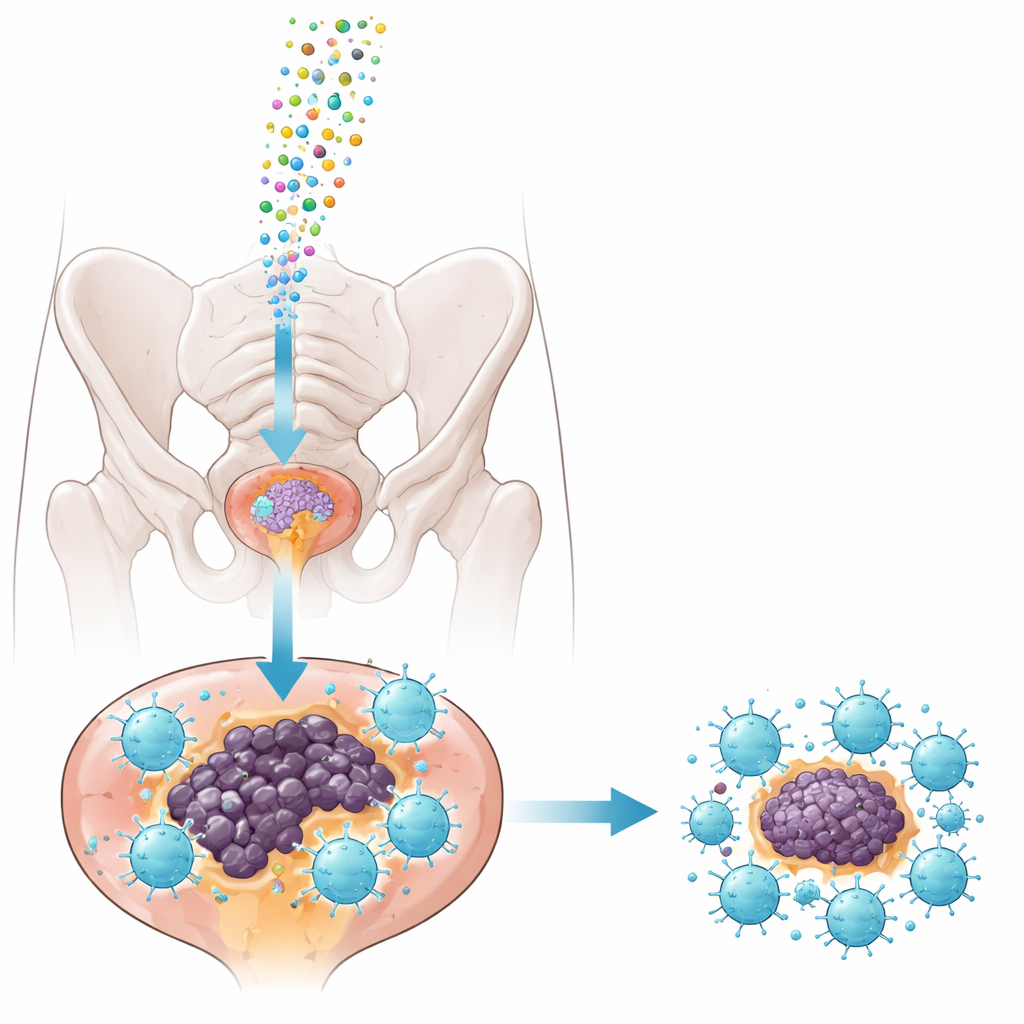
Крошечные курьеры: экзосомы как носители
Чтобы безопасно доставить ингибитор в опухоли, команда обратилась к экзосомам — наноскопическим пузырькам, естественно выделяемым клетками, которые могут переносить РНК-груз. Они выделили экзосомы из клеточной линии мышиного рака предстательной железы, тщательно их очистили и загрузили либо ингибитором miRNA-1290, либо безвредной контрольной последовательностью. Испытания показали, что экзосомы были однородны по размеру, сохраняли характерные поверхностные маркеры и хорошо захватывались тканью опухоли при прямой инъекции в предстательную железу в хорошо изученной мышиной модели (TRAMP). Важно, что лечение не нарушало функции печени и почек и не вызывало потери массы тела у здоровых животных, что указывает на относительную безопасность подхода при использованных дозах.
Замедление роста опухоли и усиление локального иммунитета
Когда мышам с опухолями вводили экзосомы, несущие ингибитор miRNA-1290, их опухоли росли медленнее, масса тела стабилизировалась или улучшалась, а продолжительность жизни была выше по сравнению с контрольными животными, получавшими пустые или контрольные экзосомы. Ингибитор резко снижал уровень miRNA-1290 в самой опухоли, но не в крови или крупных органах, что указывает на высокую локализацию эффекта. Чтобы выяснить, что происходило внутри опухолей, исследователи профилировали тысячи отдельных иммунных клеток с помощью одноклеточного РНК-секвенирования и подтвердили результаты проточной цитометрией. Они обнаружили заметное увеличение общего числа Т-клеток, цитотоксических CD8 Т-клеток и особенно специального подтипа — тканево-резидентных Т-клеток памяти (Trm), которые постоянно обитают в тканях и могут быстро реагировать на угрозу. Шаблоны активности генов в этих клетках показали обогащение воспалительных и адаптивных иммунных путей, что согласуется с усиленным антиопухолевым ответом.
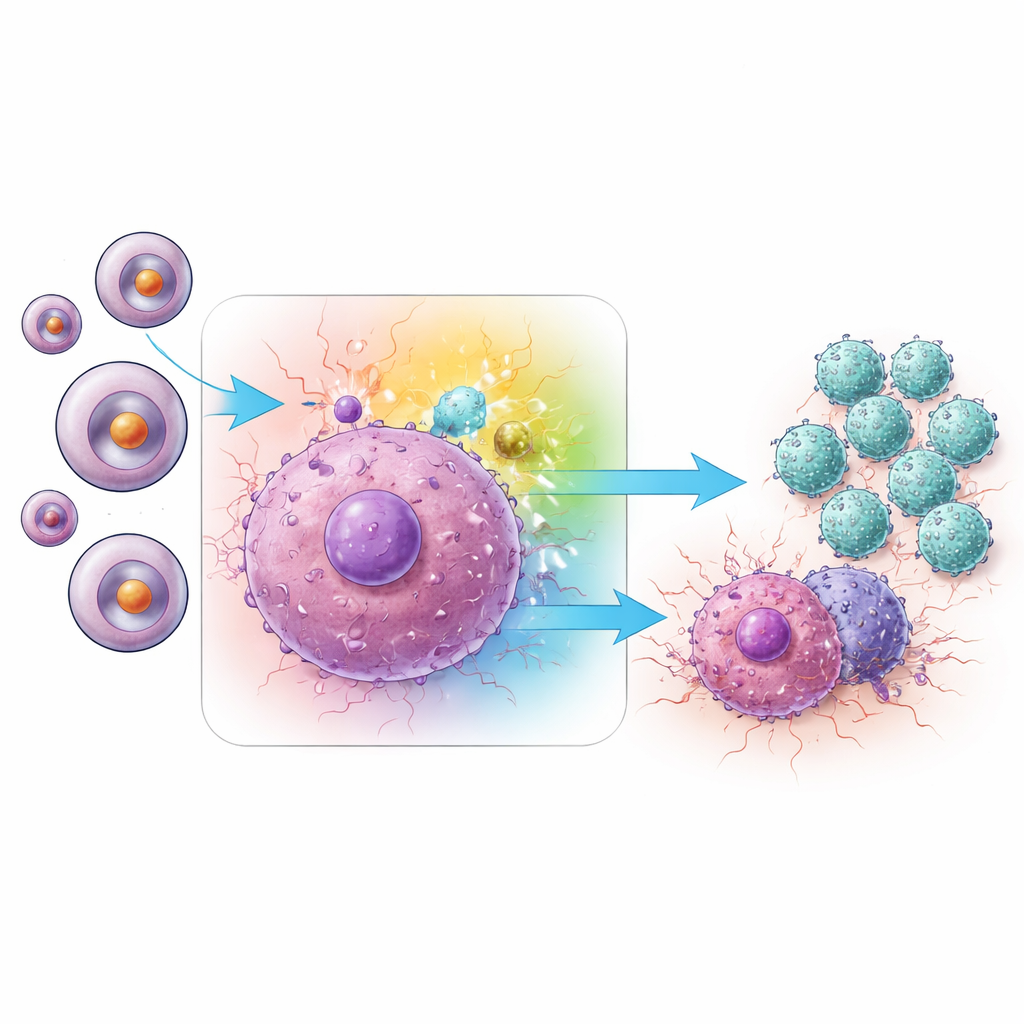
Каким образом один сигнальный путь активирует Т-клетки памяти
Углубляясь, команда изучала, какие внутриклеточные сигнальные пути в Trm ответственны за повышенную активность. Их анализ указал на сеть MAPK и особенно на её ветвь, известную как JNK. В опухолях, обработанных ингибитором miRNA-1290, Trm-клетки демонстрировали повышенные уровни активированного (фосфорилированного) JNK по сравнению с контролем. Одновременно в опухолях было больше ряда провоспалительных сигнальных белков, включая IFN-γ и TNF-α, которые являются классическими «боеприпасами» CD8 Т-клеток для уничтожения раковых клеток. При селективной блокаде разных ветвей MAPK выяснилось, что ингибирование JNK — но не двух родственных ветвей, ERK или p38 — резко снижало выработку этих ключевых цитокинов. Подавление JNK с помощью малых интерферирующих РНК в Trm-клетках давало тот же угнетающий эффект, что прочно связывает активность JNK с усиленной иммунной атакой, вызванной ингибированием miRNA-1290.
Что это может значить для будущей терапии
В сумме результаты демонстрируют, что упаковка ингибитора miRNA-1290 в экзосомы и его инъекция в опухоли предстательной железы может замедлить рост опухоли и одновременно пробудить мощный, долгосрочный локальный иммунный ответ, сфокусированный на тканево-резидентных Т-клетках памяти и их JNK-сигналинге. Хотя эксперименты проводились на мышах и включали прямые инъекции в опухоль — что может быть непрактично для всех пациентов — работа представляет собой ясное доказательство принципа. Она указывает на то, что miRNA-1290 является не только фактором, способствующим развитию рака предстательной железы, но и рычагом для перестройки иммунной среды опухоли, а также что экзосом-основанные РНК-лекарства могут стать новым классом терапий, помогающих иммунной системе сдерживать рак предстательной железы.
Цитирование: Liang, B., Zou, S. Exosome-mediated delivery of miRNA-1290 inhibitor enhances JNK-dependent tissue-resident memory T cell immunity in prostate cancer. Sci Rep 16, 13472 (2026). https://doi.org/10.1038/s41598-026-43719-x
Ключевые слова: рак предстательной железы, терапия микроРНК, экзосомы, иммунный ответ на опухоль, тканево-резидентные Т-клетки памяти