Clear Sky Science · nl
Exosoom-gemedieerde aflevering van miRNA-1290-remmer versterkt JNK-afhankelijke weefsel-resident geheugen-T-celimmuniteit bij prostaatkanker
Waarom dit onderzoek ertoe doet
Voor veel mannen is prostaatkanker een sluimerende bedreiging die plots levensbedreigend kan worden zodra de tumor niet langer op standaardbehandelingen reageert. Deze studie onderzoekt een nieuwe manier om het eigen immuunsysteem weer tegen de ziekte te keren, door gebruik te maken van kleine, natuurlijke afleverpakketjes van cellen om een genetische "uit-knop" rechtstreeks in tumoren af te leveren. Het werk wijst op een toekomst waarin prostaatkanker niet alleen door middelen die de tumor zelf raken wordt bestreden, maar ook door het gericht herbewapenen van de immuuncellen die in de tumor verblijven.
Een kleine genetische schakelaar met grote impact
Centraal in de studie staat een kort stukje genetisch materiaal genaamd miRNA-1290. Zulke microRNA’s werken als fijnregelaars van veel genen tegelijk en kunnen kanker zowel bevorderen als remmen. Eerder onderzoek koppelde hoge miRNA-1290-niveaus aan agressieve tumoren, maar de rol ervan bij prostaatkanker en de waarde als therapeutisch doel waren nog onduidelijk. De auteurs bevestigden eerst dat miRNA-1290 inderdaad verhoogd is in muizenprostaattumoren. Vervolgens maakten ze een bijpassende "remmer" die aan miRNA-1290 bindt en zijn werking blokkeert, in de hoop dat het uitschakelen ervan tumorgroei zou vertragen en het gedrag van immuuncellen in de kanker zou veranderen.
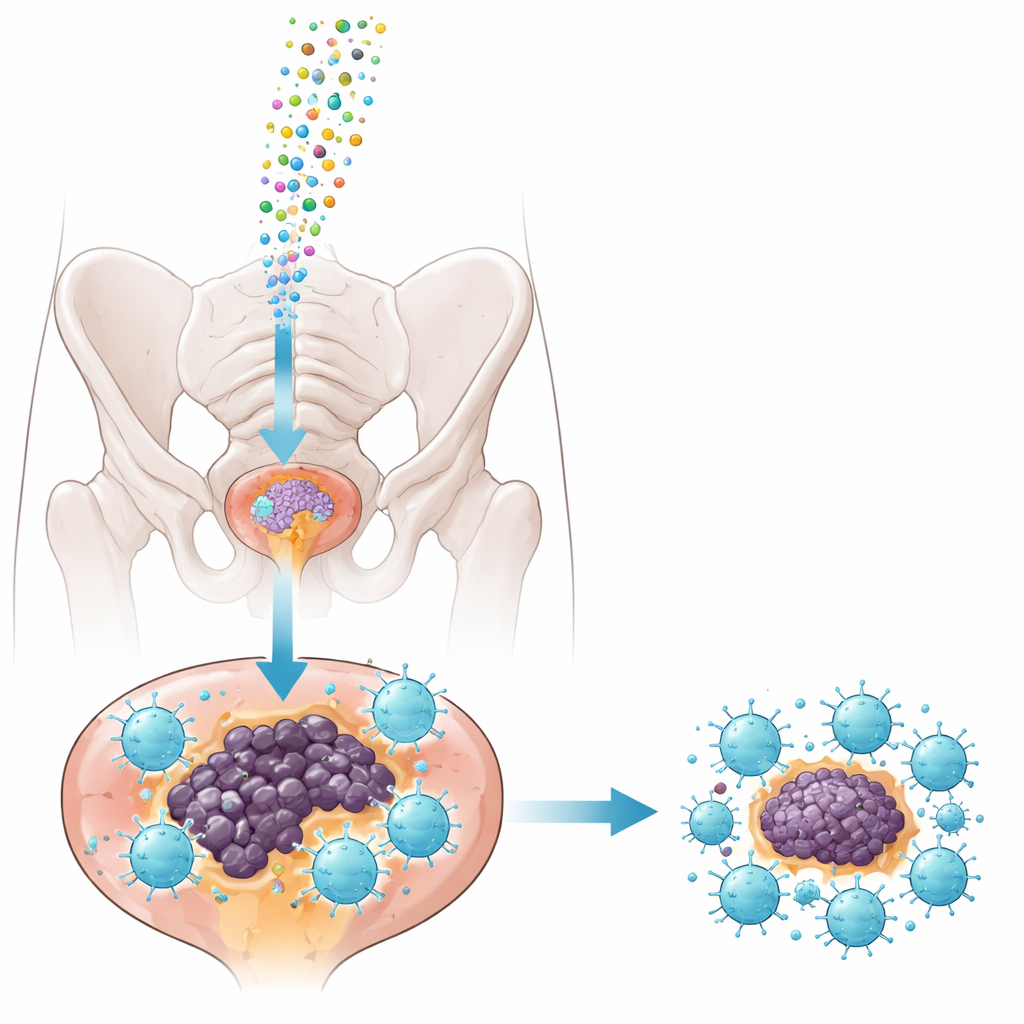
Kleine koeriers: exosomen als aflevervehikels
Om de remmer veilig in tumoren te brengen, wendde het team zich tot exosomen—nanoschaalblaasjes die cellen van nature afgeven en die RNA-lading kunnen vervoeren. Ze wonnen exosomen uit een muizenprostaatkankercellijn, zuiverden ze zorgvuldig en laadden ze met ofwel de miRNA-1290-remmer of een onschadelijke controlevodelijn. Tests toonden aan dat de exosomen uniform van grootte waren, hun gebruikelijke oppervlaktemarkers behielden en gemakkelijk door tumoren werden opgenomen wanneer ze rechtstreeks in prostaattumoren werden geïnjecteerd in een goed gevestigde muismodel (TRAMP-muizen). Belangrijk was dat de behandeling de lever- en nierfunctie of het lichaamsgewicht van gezonde dieren niet verstoorde, wat suggereert dat de benadering bij de gebruikte doseringen relatief veilig is.
Langzamere tumoren en sterkere lokale immuniteit
Toen muizen met tumoren exosomen ontvingen die de miRNA-1290-remmer droegen, groeiden hun kankers langzamer, stabiliseerde of verbeterde hun lichaamsgewicht en leefden ze langer dan controledieren die lege of controle-geladen exosomen kregen. De remmer verminderde miRNA-1290-niveaus scherp in de tumor zelf, maar niet in bloed of belangrijke organen, wat aangeeft dat het effect sterk gelokaliseerd was. Om te begrijpen wat er in de tumoren gebeurde, profiseerden de onderzoekers duizenden individuele immuuncellen met single-cell RNA-sequencing en bevestigden de bevindingen met flowcytometrie. Ze vonden een opvallende toename van totale T-cellen, van dodelijke CD8-T-cellen en vooral van een speciale subset genaamd weefsel-residente geheugen-T-cellen (Trm), die langdurig in weefsels verblijven en snel op gevaar kunnen reageren. De genactiviteitsprofielen in deze cellen toonden verrijking van inflammatoire en adaptieve immuunroutes, wat overeenkomt met een krachtiger antitumorrespons.
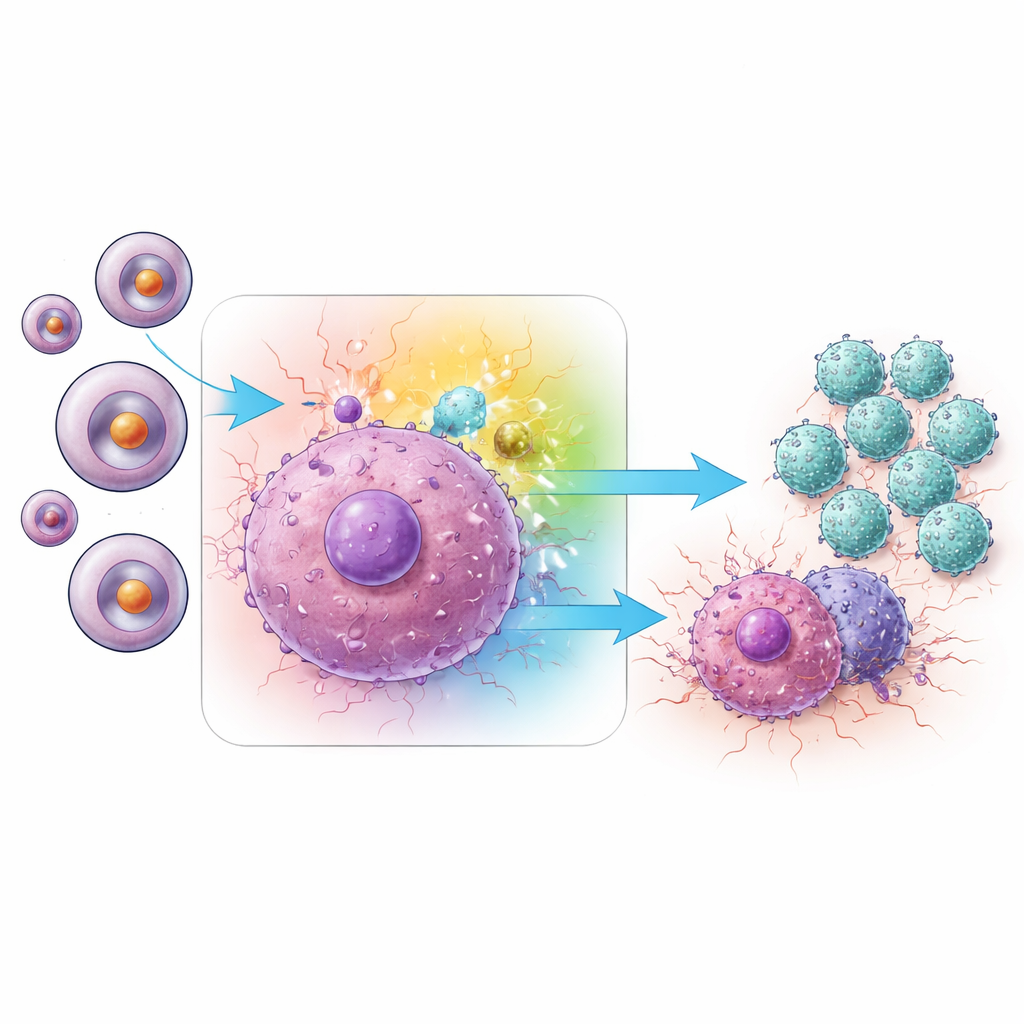
Hoe één signaalroute geheugen-T-cellen aandrijft
Dieper gravend vroegen de onderzoekers welke interne signaalroutes in Trm-cellen verantwoordelijk waren voor deze verhoogde activiteit. Hun analyses wezen op het MAPK-netwerk, en met name op een tak die bekendstaat als JNK. In tumoren behandeld met de miRNA-1290-remmer vertoonden Trm-cellen hogere niveaus van geactiveerd (gefosforyleerd) JNK vergeleken met controles. Tegelijkertijd bevatten de tumoren meer van verschillende pro-inflammatoire boodschapperproteïnen, waaronder IFN-γ en TNF-α, klassieke wapens die door CD8-T-cellen worden gebruikt om kankercellen te doden. Wanneer de onderzoekers selectief verschillende MAPK-takken blokkeerden, bleek dat het uitschakelen van JNK—maar niet twee verwante takken, ERK of p38—de productie van deze sleutelcytokines sterk verminderde. Het stilleggen van JNK met small interfering RNA in Trm-cellen had hetzelfde dempende effect, wat JNK-activiteit stevig koppelt aan de versterkte immuunaanval die door miRNA-1290-remming wordt opgewekt.
Wat dit kan betekenen voor toekomstige zorg
Gezamenlijk tonen de resultaten aan dat het verpakken van een miRNA-1290-remmer in exosomen en het injecteren daarvan in prostaattumoren de tumorgroei kan vertragen terwijl het een krachtige, langdurige lokale immuunrespons activeert die gecentreerd is rond weefsel-residente geheugen-T-cellen en hun JNK-signaleringspad. Hoewel de experimenten in muizen werden uitgevoerd en directe tumorinjecties gebruikten—wat niet voor alle patiënten praktisch zal zijn—biedt het werk een duidelijke proof of principle. Het suggereert dat miRNA-1290 zowel een aandrijver van prostaatkanker is als een hefboom om de immuunomgeving van de tumor te hervormen, en dat exosoom-gebaseerde RNA-geneesmiddelen mogelijk een nieuwe klasse therapieën kunnen worden die het immuunsysteem helpen prostaatkanker onder controle te houden.
Bronvermelding: Liang, B., Zou, S. Exosome-mediated delivery of miRNA-1290 inhibitor enhances JNK-dependent tissue-resident memory T cell immunity in prostate cancer. Sci Rep 16, 13472 (2026). https://doi.org/10.1038/s41598-026-43719-x
Trefwoorden: prostaatkanker, microRNA-therapie, exosomen, tumorimmuunrespons, weefsel-residente geheugen-T-cellen