Clear Sky Science · de
Exosomvermittelte Verabreichung eines miRNA-1290-Inhibitors verstärkt JNK‑abhängige Gewebe‑residenten Memory‑T‑Zell‑Immunität beim Prostatakarzinom
Warum diese Forschung wichtig ist
Für viele Männer ist Prostatakrebs eine schleichende Bedrohung, die plötzlich lebensbedrohlich werden kann, wenn sie nicht mehr auf Standardtherapien anspricht. Diese Studie untersucht einen neuen Weg, das körpereigene Immunsystem wieder gegen die Erkrankung zu richten, indem winzige, natürliche Transportpakete aus Zellen verwendet werden, um einen genetischen „Ausschalter“ direkt in Tumore zu bringen. Die Arbeit deutet auf eine Zukunft hin, in der Prostatakrebs nicht nur durch Medikamente, die direkt den Tumor treffen, kontrolliert werden könnte, sondern auch durch ein gezieltes Wiederbewaffnen der Immunzellen, die im Tumor leben.
Ein kleiner genetischer Schalter mit großer Wirkung
Im Zentrum der Studie steht ein kurzes genetisches Fragment namens miRNA‑1290. Solche MicroRNAs wirken als Feinabstimmer vieler Gene gleichzeitig und können Krebs entweder fördern oder hemmen. Frühere Arbeiten hatten hohe miRNA‑1290‑Spiegel mit aggressiven Tumoren in Verbindung gebracht, doch ihre Rolle beim Prostatakrebs und ihr Potenzial als Therapieziel waren noch unklar. Die Autoren bestätigten zunächst, dass miRNA‑1290 in Mausprostatatumoren tatsächlich erhöht ist. Anschließend entwickelten sie einen passenden „Inhibitor“, der an miRNA‑1290 bindet und ihre Wirkung blockiert, in der Hoffnung, dass deren Abschaltung das Tumorwachstum verlangsamt und das Verhalten der Immunzellen im Tumor verändert.
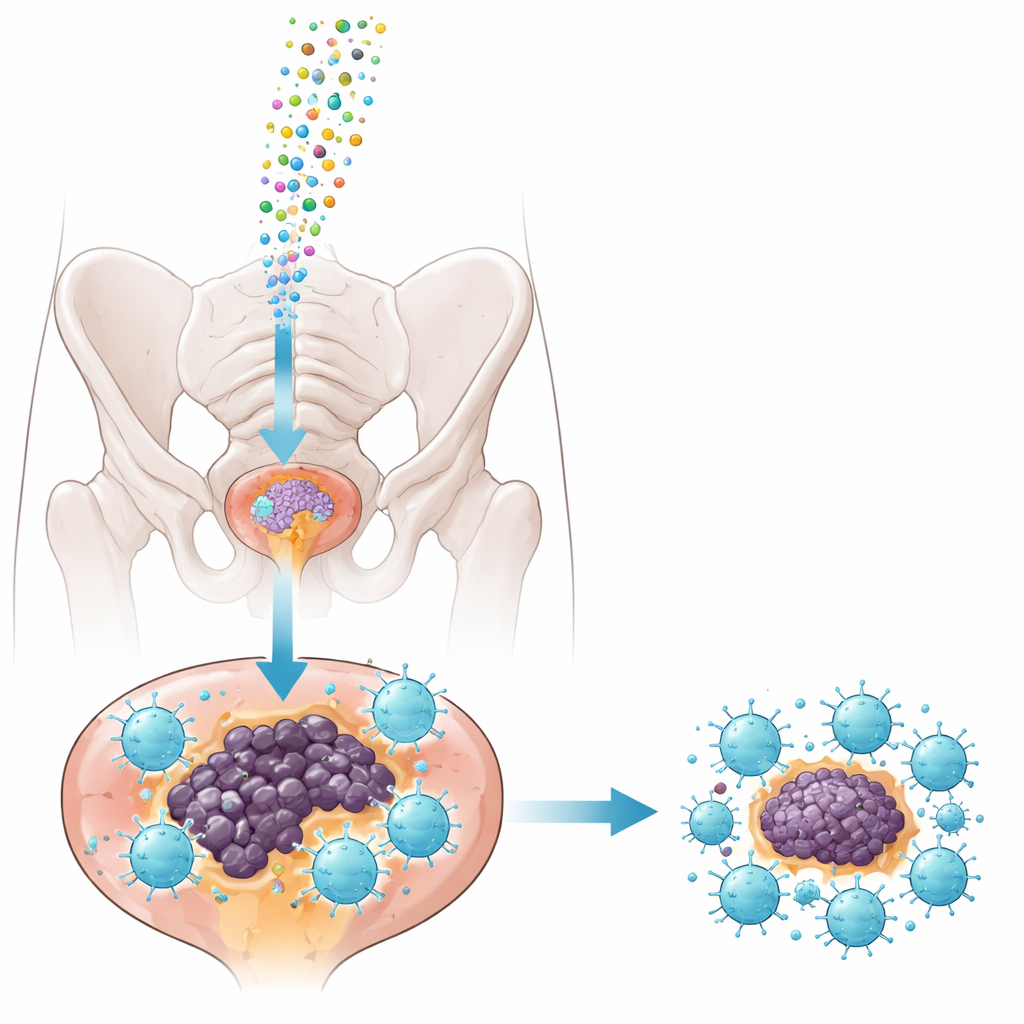
Winzige Kuriere: Exosomen als Transportvehikel
Um den Inhibitor sicher in Tumore zu bringen, griff das Team auf Exosomen zurück — nanoskalige Bläschen, die Zellen natürlicherweise freisetzen und RNA‑Fracht transportieren können. Sie gewannen Exosomen aus einer Maus‑Prostatakrebszelllinie, reinigten sie sorgfältig und beluden sie entweder mit dem miRNA‑1290‑Inhibitor oder mit einer harmlosen Kontrollsequenz. Tests zeigten, dass die Exosomen in der Größe einheitlich waren, ihre üblichen Oberflächenmarker behielten und bei direkter Injektion in die Prostatatumore eines etablierten Mausmodells (TRAMP‑Mäuse) gut vom Tumorgewebe aufgenommen wurden. Wichtig ist, dass die Behandlung die Leber‑ und Nierenfunktion sowie das Körpergewicht gesunder Tiere nicht störte, was darauf hindeutet, dass der Ansatz in den verwendeten Dosen relativ sicher ist.
Langsamere Tumore und stärkere lokale Immunität
Als tumortragende Mäuse Exosomen mit dem miRNA‑1290‑Inhibitor erhielten, wuchsen ihre Tumore langsamer, ihr Körpergewicht stabilisierte sich oder verbesserte sich, und sie lebten länger als Kontrolltiere, die leere oder kontrollbeladene Exosomen bekamen. Der Inhibitor senkte die miRNA‑1290‑Spiegel im Tumor selbst deutlich, nicht jedoch im Blut oder in wichtigen Organen, was auf einen stark lokalisierten Effekt hindeutet. Um zu verstehen, was sich im Tumor abspielte, analysierten die Forscher tausende einzelner Immunzellen mittels Einzelzellanalyse der RNA und bestätigten die Ergebnisse mit Durchflusszytometrie. Sie fanden einen markanten Anstieg insgesamt an T‑Zellen, an zytotoxischen CD8‑T‑Zellen und besonders an einer speziellen Untergruppe, den gewebe‑residenten Memory‑T‑Zellen (Trm), die langfristig in Geweben verbleiben und schnell auf Gefahren reagieren können. Genexpressionsmuster in diesen Zellen zeigten eine Anreicherung entzündlicher und adaptiver Immunwege, was zu einer stärkeren antitumoralen Reaktion passt.
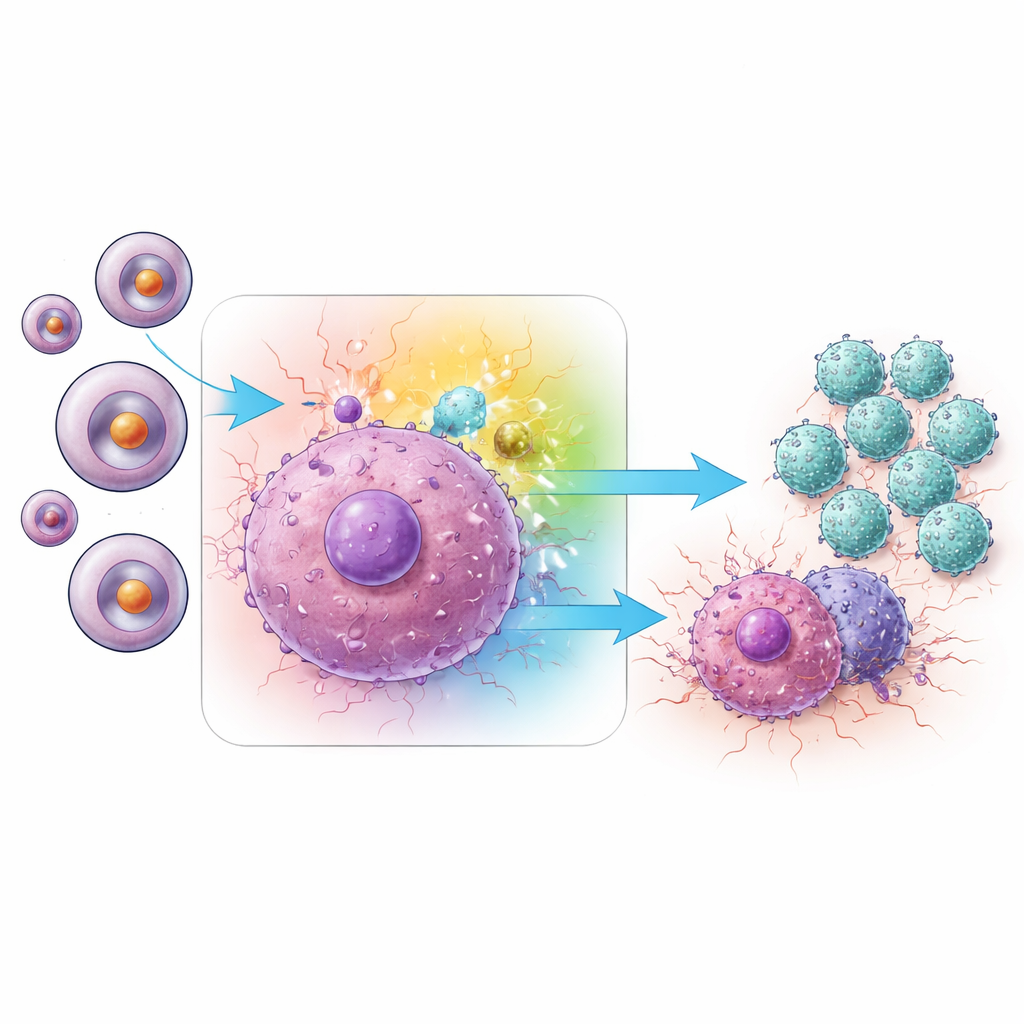
Wie ein Signalweg Memory‑T‑Zellen antreibt
Ein Blick ins Detail zeigte, welche internen Signalwege in Trm‑Zellen für diese erhöhte Aktivität verantwortlich sind. Ihre Analysen wiesen auf das MAPK‑Netzwerk hin, insbesondere auf einen Zweig, der als JNK bekannt ist. In Tumoren, die mit dem miRNA‑1290‑Inhibitor behandelt wurden, zeigten Trm‑Zellen höhere Werte an aktiviertem (phosphoryliertem) JNK im Vergleich zu Kontrollen. Gleichzeitig enthielten die Tumore mehrerer proinflammatorischer Botenproteine, darunter IFN‑γ und TNF‑α, klassische Waffen der CD8‑T‑Zellen gegen Krebszellen. Als die Forscher verschiedene MAPK‑Zweige selektiv blockierten, stellten sie fest, dass die Hemmung von JNK — nicht jedoch der verwandten Zweige ERK oder p38 — die Produktion dieser Schlüsselzytokine stark reduzierte. Das Stilllegen von JNK mit kleinen interferierenden RNAs in Trm‑Zellen hatte denselben dämpfenden Effekt und verband so die JNK‑Aktivität eindeutig mit dem durch miRNA‑1290‑Hemmung ausgelösten verstärkten Immunangriff.
Was das für die zukünftige Versorgung bedeuten könnte
Insgesamt zeigen die Ergebnisse, dass das Verpacken eines miRNA‑1290‑Inhibitors in Exosomen und dessen Injektion in Prostatatumore das Tumorwachstum verlangsamen und gleichzeitig eine starke, langanhaltende lokale Immunantwort auslösen kann, die auf geweberesidente Memory‑T‑Zellen und deren JNK‑Signalgebung zentriert ist. Obwohl die Experimente an Mäusen durchgeführt und direkte Tumorinjektionen verwendet wurden — was nicht für alle Patienten praktikabel sein dürfte — liefert die Arbeit einen klaren Proof of Principle. Sie legt nahe, dass miRNA‑1290 sowohl ein Treiber des Prostatakarzinoms als auch ein Hebel zur Umgestaltung des tumorenvironment ist und dass exosombasierte RNA‑Medikamente zu einer neuen Klasse von Therapien werden könnten, die dem Immunsystem helfen, Prostatakrebs in Schach zu halten.
Zitation: Liang, B., Zou, S. Exosome-mediated delivery of miRNA-1290 inhibitor enhances JNK-dependent tissue-resident memory T cell immunity in prostate cancer. Sci Rep 16, 13472 (2026). https://doi.org/10.1038/s41598-026-43719-x
Schlüsselwörter: Prostatakrebs, MicroRNA‑Therapie, Exosomen, tumorale Immunantwort, gewebe‑residente Memory‑T‑Zellen