Clear Sky Science · pl
Dostarczanie inhibitora miRNA-1290 za pośrednictwem egzosomów wzmacnia odporność komórek T rezydujących w tkance zależną od JNK w raku prostaty
Dlaczego te badania są istotne
Dla wielu mężczyzn rak prostaty to powolne zagrożenie, które może nagle stać się śmiertelne, gdy przestanie reagować na standardowe leczenie. W badaniu tym analizowano nowy sposób skierowania układu odpornościowego przeciwko chorobie, wykorzystując drobne, naturalne „paczki” komórkowe do dostarczenia genetycznego „wyłącznika” bezpośrednio do guzów. Praca wskazuje na przyszłość, w której raka prostaty można by kontrolować nie tylko za pomocą leków atakujących sam guz, ale także przez precyzyjne przezbrajanie komórek odpornościowych zasiedlających nowotwór.
Mały przełącznik genetyczny o dużym znaczeniu
W centrum badania znajduje się krótki fragment materiału genetycznego zwany miRNA‑1290. Takie mikroRNA działają jako drobne regulatory wielu genów naraz i mogą wspierać lub hamować rozwój nowotworu. Wcześniejsze prace wiązały wysokie poziomy miRNA‑1290 z agresywnymi guzami, lecz jego rola w raku prostaty i wartość jako celu terapeutycznego pozostawały niejasne. Autorzy najpierw potwierdzili, że miRNA‑1290 rzeczywiście jest podwyższone w guzach prostaty u myszy. Zaprojektowali następnie dopasowany „inhibitor”, który wiąże się z miRNA‑1290 i blokuje jego działanie, z nadzieją, że jego wyłączenie spowolni wzrost guza i zmieni zachowanie komórek odpornościowych w obrębie nowotworu.
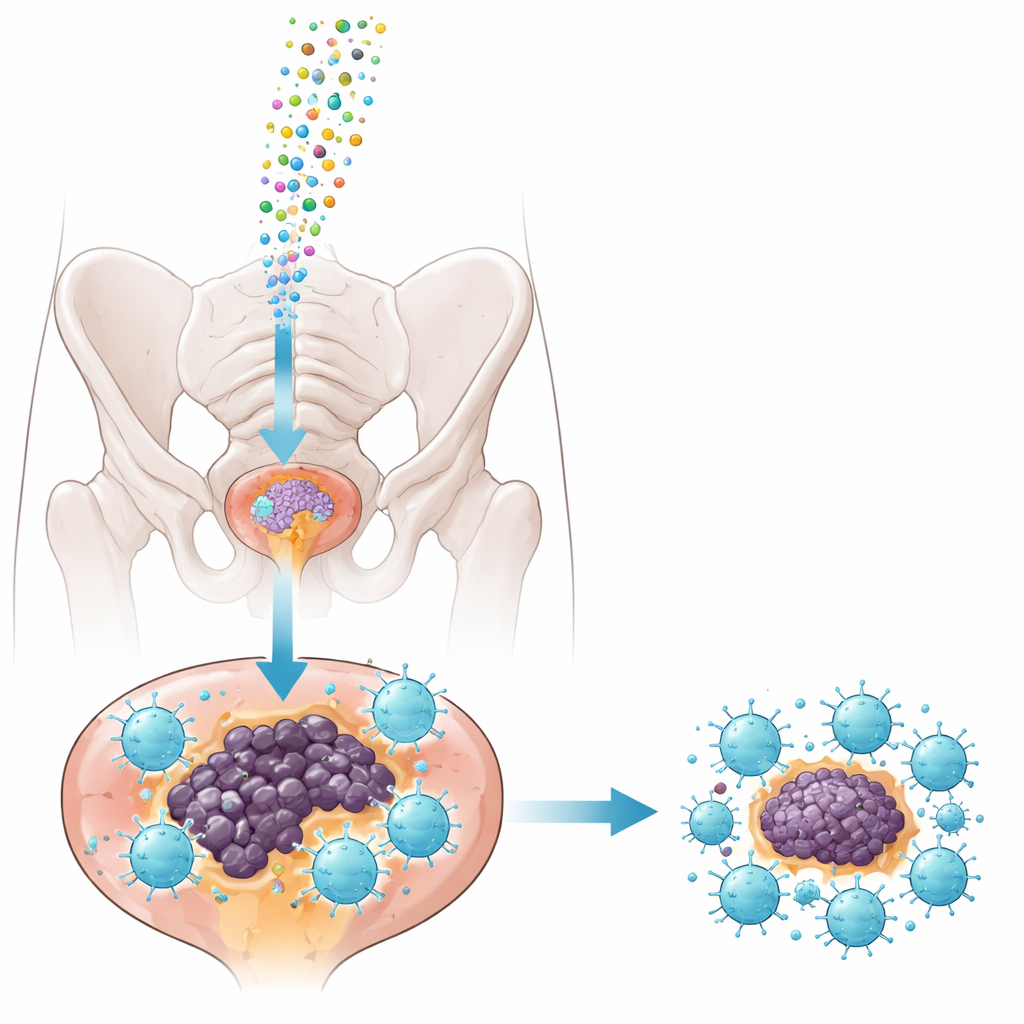
Drobni kurierzy: egzosomy jako nośniki
Aby bezpiecznie dostarczyć inhibitor do guzów, zespół sięgnął po egzosomy — nanoskaliowe pęcherzyki naturalnie uwalniane przez komórki, które mogą przenosić ładunek RNA. Pozyskali egzosomy z linii komórkowej raka prostaty myszy, starannie je oczyszczono i załadowano albo inhibitorem miRNA‑1290, albo neutralną sekwencją kontrolną. Testy wykazały, że egzosomy były jednorodne pod względem rozmiaru, zachowywały typowe markery powierzchniowe i były chętnie pobierane przez tkankę nowotworową po bezpośrednim wstrzyknięciu do guzów w dobrze opisanym modelu myszy TRAMP. Co ważne, leczenie nie zaburzało funkcji wątroby i nerek ani masy ciała zdrowych zwierząt, co sugeruje, że podejście jest stosunkowo bezpieczne przy stosowanych dawkach.
Wolniejszy wzrost guzów i silniejsza lokalna odporność
Gdy myszy z guzami otrzymywały egzosomy zawierające inhibitor miRNA‑1290, ich nowotwory rosły wolniej, masa ciała stabilizowała się lub poprawiała, a zwierzęta żyły dłużej niż kontrolne, które otrzymały puste egzosomy lub z ładunkiem kontrolnym. Inhibitor silnie obniżył poziomy miRNA‑1290 w samym guzie, ale nie w krwi ani głównych narządach, co wskazuje na wysoce zlokalizowany efekt. Aby zrozumieć zmiany wewnątrz guzów, badacze profilowali tysiące pojedynczych komórek odpornościowych za pomocą sekwencjonowania RNA pojedynczych komórek i potwierdzili wyniki cytometrią przepływową. Stwierdzili wyraźny wzrost liczby limfocytów T ogółem, cytotoksycznych limfocytów CD8 oraz szczególnie podzbioru nazywanego tkankowymi komórkami pamięci T (Trm), które osiedlają się na stałe w tkankach i mogą szybko odpowiadać na zagrożenie. Wzory aktywności genów w tych komórkach wykazywały wzbogacenie szlaków zapalnych i adaptacyjnej odpowiedzi immunologicznej, co jest zgodne z bardziej agresywną odpowiedzią przeciwko nowotworowi.
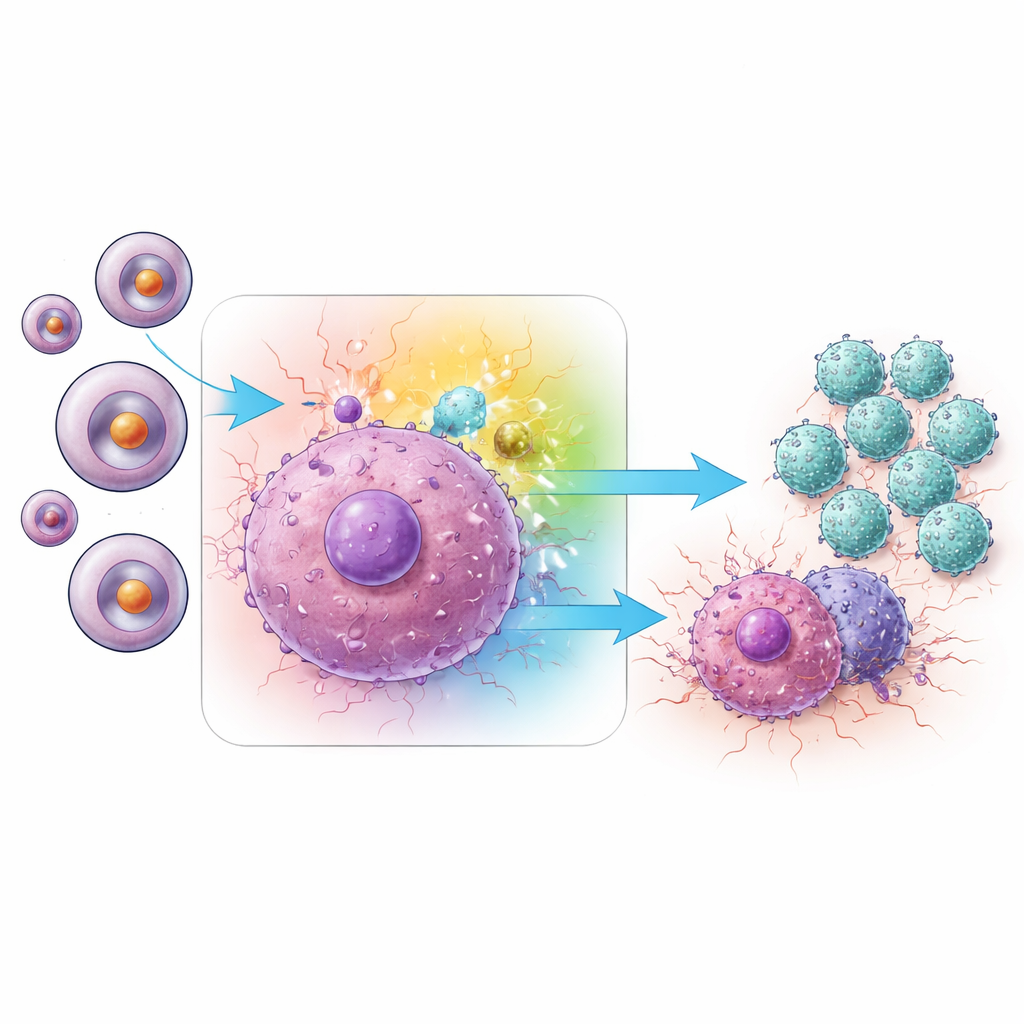
Jak jeden szlak sygnałowy napędza komórki pamięci
Zagłębiając się dalej, zespół zbadał, które wewnętrzne szlaki sygnałowe w komórkach Trm odpowiadały za tę zwiększoną aktywność. Ich analizy wskazały sieć MAPK, a w szczególności odgałęzienie znane jako JNK. W guzach leczonych inhibitorem miRNA‑1290 komórki Trm wykazywały wyższe poziomy aktywowanego (ufosforylowanego) JNK w porównaniu z kontrolami. Jednocześnie guzy zawierały więcej kilku prozapalnych białek sygnałowych, w tym IFN‑γ i TNF‑α, które są klasycznymi „bronami” używanymi przez limfocyty CD8 do zabijania komórek nowotworowych. Gdy badacze selektywnie blokowali różne odgałęzienia MAPK, stwierdzili, że wyłączenie JNK — w przeciwieństwie do dwóch powiązanych odgałęzień, ERK lub p38 — silnie zmniejszało produkcję tych kluczowych cytokin. Wyciszenie JNK za pomocą małych interferujących RNA w komórkach Trm dało ten sam efekt tłumiący, co zdecydowanie powiązało aktywność JNK z nasilonym atakiem immunologicznym wywołanym przez inhibicję miRNA‑1290.
Co to może znaczyć dla przyszłej opieki
Podsumowując, wyniki pokazują, że zapakowanie inhibitora miRNA‑1290 w egzosomy i wstrzyknięcie ich do guzów prostaty może spowolnić wzrost nowotworu, jednocześnie uruchamiając silną, długotrwałą lokalną odpowiedź immunologiczną skoncentrowaną na tkankowych komórkach pamięci T i ich sygnalizacji JNK. Choć eksperymenty przeprowadzono na myszach i użyto bezpośrednich wstrzyknięć do guza — co nie zawsze będzie praktyczne u wszystkich pacjentów — praca dostarcza jasnego dowodu koncepcji. Sugeruje, że miRNA‑1290 jest zarówno czynnikiem napędzającym raka prostaty, jak i dźwignią do przekształcenia środowiska immunologicznego guza, a terapie oparte na egzosomach przenoszące RNA mogłyby stać się nową klasą leków pomagających układowi odpornościowemu powstrzymywać raka prostaty.
Cytowanie: Liang, B., Zou, S. Exosome-mediated delivery of miRNA-1290 inhibitor enhances JNK-dependent tissue-resident memory T cell immunity in prostate cancer. Sci Rep 16, 13472 (2026). https://doi.org/10.1038/s41598-026-43719-x
Słowa kluczowe: rak prostaty, terapia mikroRNA, egzosomy, odpowiedź immunologiczna przeciwko nowotworowi, tkankowe komórki pamięci T