Clear Sky Science · zh
SHP2通过调节IRE1α/XBP1/NLRP3介导的颗粒细胞焦亡改善大鼠多囊卵巢模型的卵巢形态和类固醇生成功能
这对女性健康为何重要
多囊卵巢综合征(PCOS)影响全球数百万女性,常导致月经不规律、妊娠困难,以及糖尿病和心脏病等长期风险。然而,这种疾病的内部机制,尤其是卵巢细胞内部发生的病理过程,仍未完全清楚。本研究使用大鼠和人类卵巢细胞,探讨了一个关键细胞开关SHP2,并展示了调节该开关如何保护卵巢免受过量雄激素驱动的损伤。
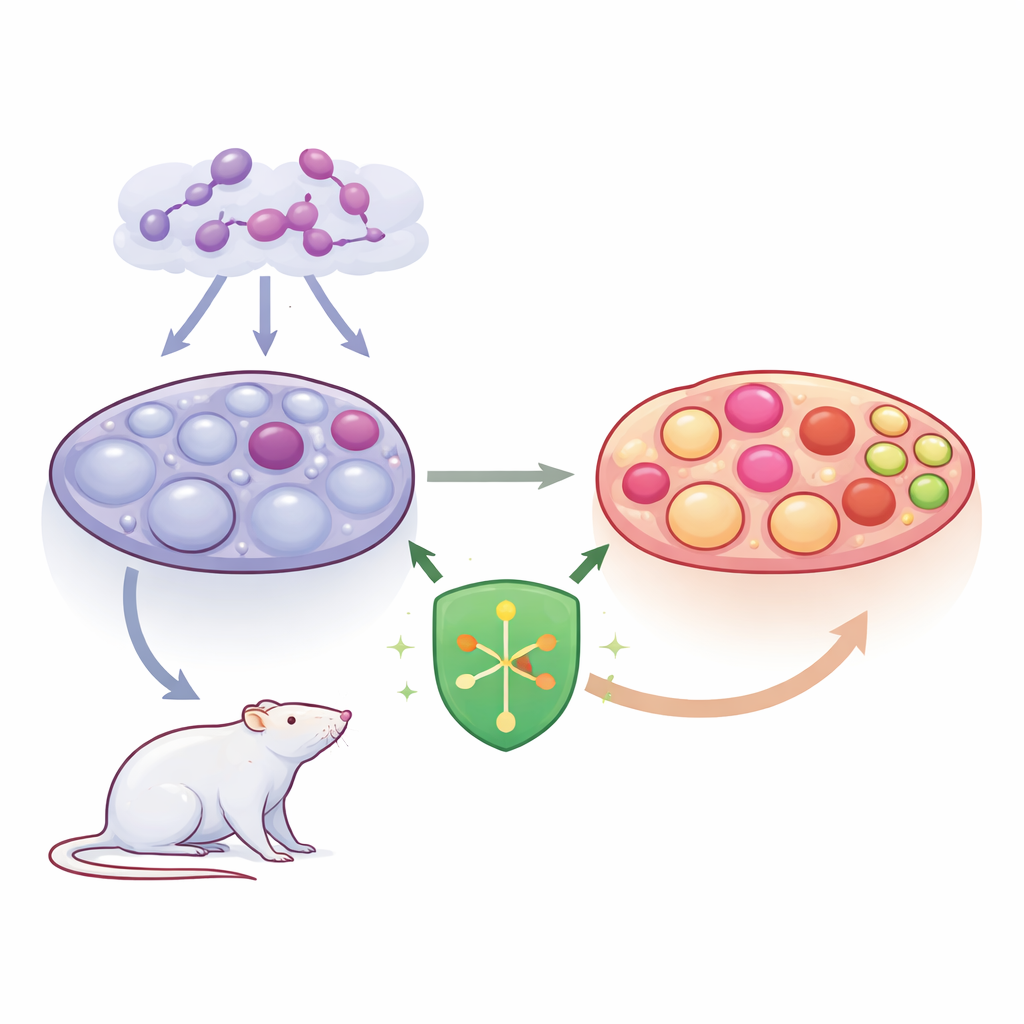
聚焦卵巢中的PCOS
PCOS的特征是激素失衡和卵巢内出现多个充满液体的囊腔(囊泡)。这些囊泡反映的是处于停滞状态、未能成熟并排卵的卵泡。研究团队关注颗粒细胞——它们包绕并滋养发育中的卵子,并参与性激素的生成。当这些细胞承受应激或以不正常的方式死亡时,卵泡会失去功能,激素水平进一步紊乱。研究者特别关心一种会使细胞破裂并加剧卵巢炎症的剧烈细胞死亡形式,称为焦亡(pyroptosis)。
一个细胞开关的保护作用
科学家们研究了SHP2,这是一种像旋钮一样调节多种细胞信号的分子,包括与生长、生存和炎症相关的通路。在通过让雄激素合成抑制剂来建立的来曲唑诱导大鼠PCOS模型中,他们用病毒载体在综合征发生前提高了SHP2的表达。与未处理的PCOS大鼠相比,SHP2过表达的动物卵巢更轻,大的囊性卵泡更少,且黄体(排卵后形成的结构)更多。它们的激素谱朝有利方向转变:雌二醇、睾酮和黄体生成素下降,促卵泡激素上升,提示更接近正常的排卵与激素生成。
细胞应激如何变得有毒
为了解颗粒细胞内发生了什么,研究团队在类人颗粒细胞模型中施加了睾酮。高水平睾酮诱导了内质网应激——细胞的蛋白质加工中心,并激活了以IRE1α和XBP1为核心的一系列信号。这又激活了一个名为NLRP3的蛋白复合体,驱动焦亡发生。细胞表现出与膜孔形成和炎性细胞死亡相关的分子标志物上调。与此同时,另一路径涉及调控因子ZEB1的活动增强,使结构蛋白PKP3减弱,并扰乱了原本让颗粒细胞受控生长与分裂的细胞周期机制。
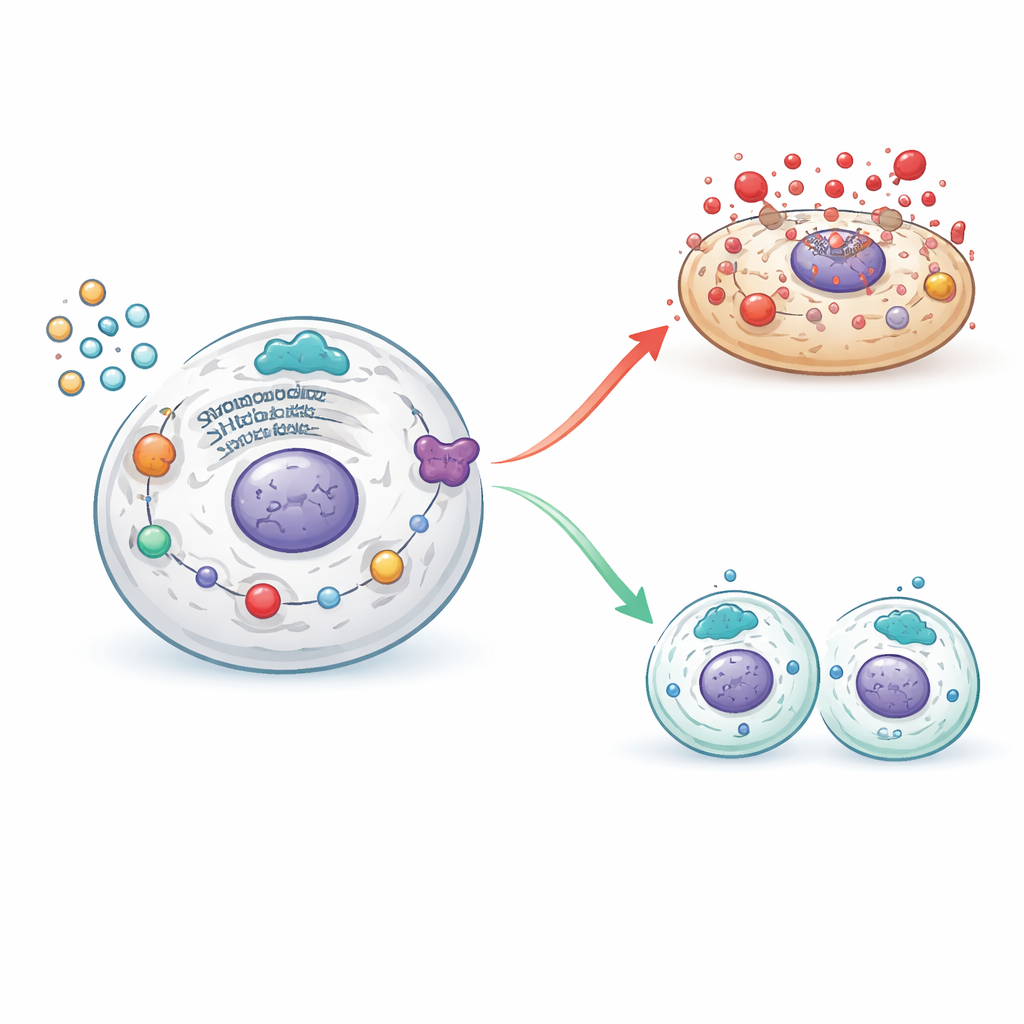
在卵巢细胞中平衡死亡与更新
当支持SHP2活性时,这些有害级联反应被抑制:细胞应激信号和焦亡机制减弱,而支持有序细胞分裂的分子恢复。阻断SHP2则产生相反效果,重新激活应激与炎症通路,再次推动颗粒细胞走向破坏性死亡并远离健康增殖。通过结合基因学工具和化学抑制剂,研究者绘制出SHP2处于损伤性炎症与组织更新之间的关键交叉点,决定颗粒细胞是以爆裂性死亡结束,还是存活以支持卵泡成熟。
这对未来治疗可能意味着什么
对非专业读者而言,核心信息是:PCOS不仅仅是一个激素问题,还是一种涉及受压且发炎的卵巢细胞的疾病。本研究将SHP2确定为一个关键开关,帮助决定颗粒细胞是以损害卵巢的自我毁灭方式死去,还是继续正常工作与分裂。在大鼠模型中,调控SHP2相关通路改善了卵巢结构和激素平衡。尽管这项工作仍处于早期的临床前阶段,但它提示未来有针对性地调整SHP2及其相关应激通路的药物,可能有望帮助恢复多囊卵巢患者的卵巢健康与生育力。
引用: Wang, D., Wang, J., Yang, B. et al. SHP2 improves ovarian morphology and steroidogenic function in a rat PCOS model by modulating IRE1α/XBP1/NLRP3-mediated granulosa cell pyroptosis. Sci Rep 16, 14376 (2026). https://doi.org/10.1038/s41598-026-43536-2
关键词: 多囊卵巢综合征, 颗粒细胞, 卵巢炎症, 细胞死亡, 激素失衡