Clear Sky Science · pt
SHP2 melhora a morfologia ovariana e a função esteroidogênica em um modelo de SOP em ratos ao modular a piroptose de células da granulosa mediada por IRE1α/XBP1/NLRP3
Por que isso importa para a saúde da mulher
A síndrome dos ovários policísticos (SOP) afeta milhões de mulheres no mundo, frequentemente causando ciclos irregulares, dificuldade para engravidar e riscos a longo prazo como diabetes e doenças cardíacas. No entanto, os mecanismos internos dessa condição, especialmente o que dá errado nas células do ovário, continuam apenas parcialmente compreendidos. Este estudo usa ratos e células ovarianas humanas para explorar um interruptor celular chave chamado SHP2 e mostra como ajustar esse interruptor pode proteger o ovário de danos induzidos por excesso de hormônios masculinos.
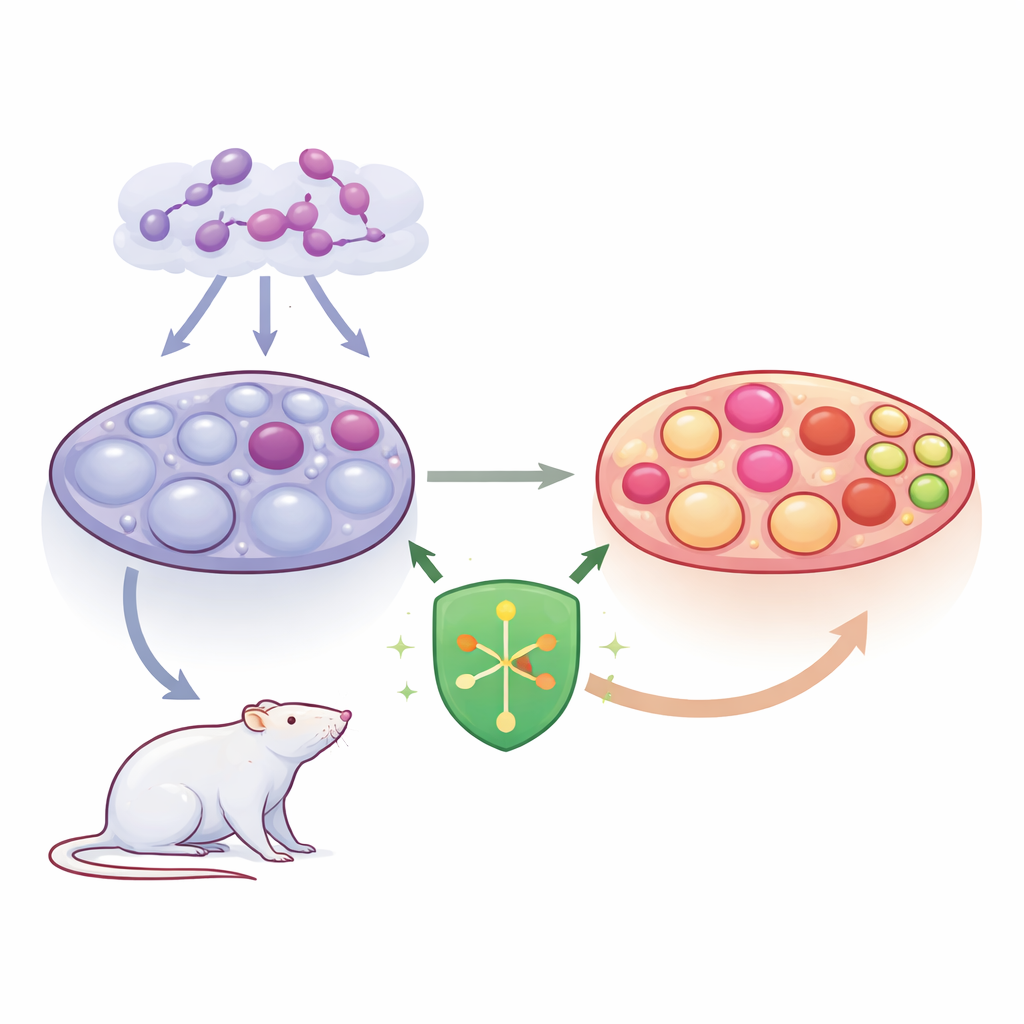
Uma visão mais próxima da SOP no ovário
A SOP é marcada por desequilíbrio hormonal e pelo aparecimento de muitos sacos cheios de líquido, ou cistos, no ovário. Esses cistos correspondem a folículos que estagnaram em vez de amadurecer e liberar um óvulo. A equipe concentrou-se nas células da granulosa, que envolvem e nutrem os óvulos em desenvolvimento e ajudam a produzir hormônios sexuais. Quando essas células são estressadas ou morrem de forma inadequada, os folículos falham e os níveis hormonais se tornam ainda mais distorcidos. Os pesquisadores deram atenção especial a uma forma inflamatória de morte celular chamada piroptose, que faz as células se romperem e alimenta a inflamação no ovário.
O papel protetor de um interruptor celular
Os cientistas investigaram o SHP2, uma molécula que funciona como um botão de controle para muitos sinais celulares, incluindo os ligados ao crescimento, sobrevivência e inflamação. Em um modelo de SOP em ratos, induzido pelo medicamento letrozol, eles usaram um vírus para aumentar os níveis de SHP2 antes do desenvolvimento da síndrome. Em comparação com ratos com SOP não tratados, aqueles com excesso de SHP2 apresentaram ovários mais leves, menos folículos císticos grandes e mais estruturas saudáveis pós-ovulação chamadas corpos lúteos. O perfil hormonal mudou em direção a uma situação favorável: estradiol, testosterona e hormônio luteinizante diminuíram, enquanto o hormônio folículo-estimulante aumentou, sugerindo uma ovulação e produção hormonal mais próximas do normal.
Como o estresse celular se torna tóxico
Para entender o que acontecia dentro das células da granulosa, a equipe recorreu a células humanas semelhantes às da granulosa expostas à testosterona. Altos níveis de testosterona desencadearam uma resposta de estresse no retículo endoplasmático, o centro de processamento de proteínas da célula, e ativaram uma cascata de sinais centrada em IRE1α e XBP1. Isso, por sua vez, ativou um complexo proteico chamado NLRP3, que impulsiona a piroptose. As células mostraram níveis mais altos de marcadores moleculares ligados à formação de poros na membrana e à morte inflamatória. Ao mesmo tempo, outra via envolvendo o regulador ZEB1 enfraqueceu uma proteína estrutural, PKP3, e perturbou as máquinas do ciclo celular que normalmente permitem que as células da granulosa cresçam e se dividam de forma controlada.
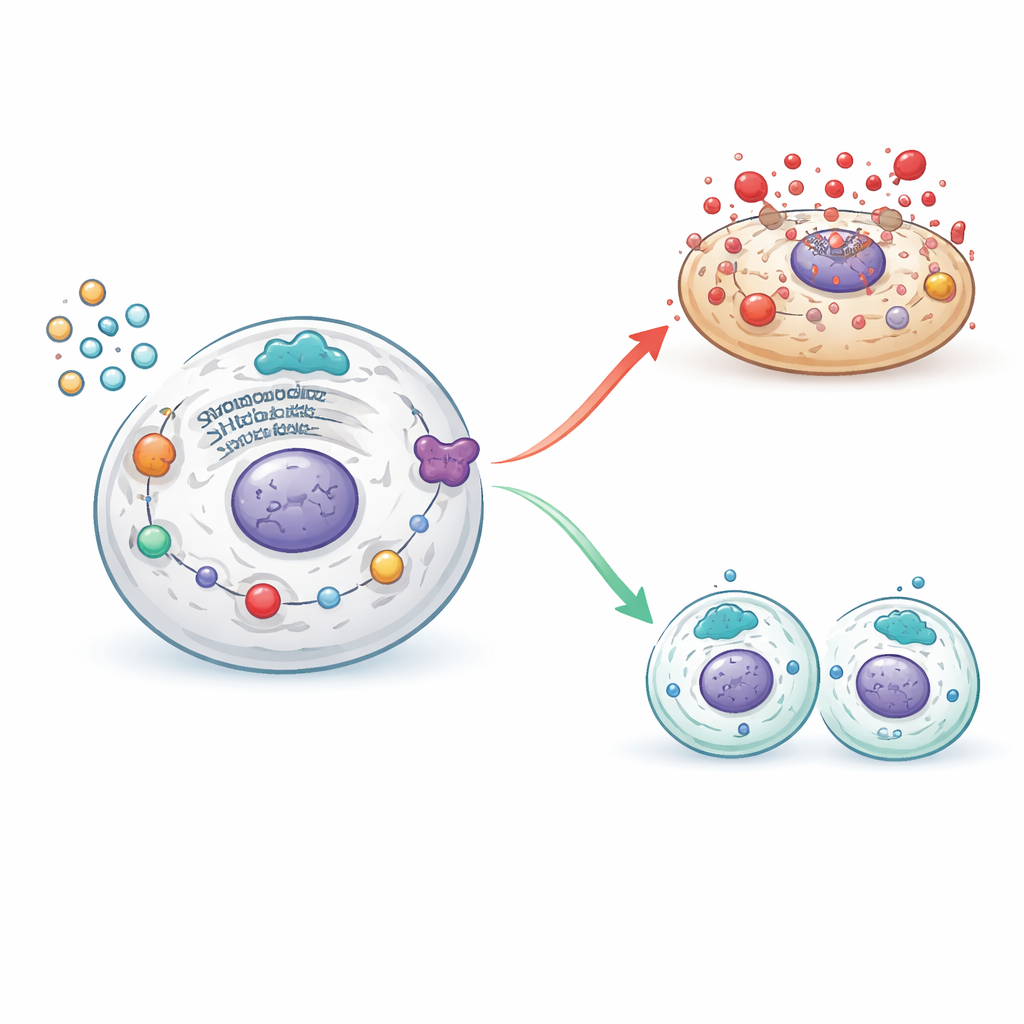
Equilibrando morte e renovação nas células ovarianas
Quando a atividade de SHP2 foi mantida, essas cascatas nocivas foram atenuadas: os sinais de estresse celular e a maquinaria da piroptose foram reduzidos, enquanto moléculas que apoiam uma divisão celular ordenada se recuperaram. Bloquear o SHP2 teve o efeito oposto, reativando vias de estresse e inflamação e novamente empurrando as células da granulosa para uma morte destrutiva em vez de uma proliferação saudável. Ao combinar ferramentas genéticas e inibidores químicos, os pesquisadores mapearam como o SHP2 se situa em um cruzamento entre inflamação danosa e renovação tecidual, determinando se as células da granulosa morrem de forma explosiva ou sobrevivem para sustentar folículos em maturação.
O que isso pode significar para tratamentos futuros
Para não especialistas, a mensagem principal é que a SOP não é apenas um problema hormonal, mas também uma doença de células ovarianas estressadas e inflamadas. Este estudo identifica o SHP2 como um interruptor central que ajuda a decidir se as células da granulosa se autodestroem de uma forma que prejudica o ovário ou continuam a funcionar e se dividir normalmente. No modelo de rato, direcionar as vias relacionadas ao SHP2 melhorou a estrutura ovariana e o equilíbrio hormonal. Embora este trabalho ainda esteja em estágio pré-clínico inicial, sugere que fármacos cuidadosamente direcionados que ajustem o SHP2 e suas vias de estresse conectadas possam, um dia, ajudar a restaurar ovários e fertilidade mais saudáveis em pessoas com SOP.
Citação: Wang, D., Wang, J., Yang, B. et al. SHP2 improves ovarian morphology and steroidogenic function in a rat PCOS model by modulating IRE1α/XBP1/NLRP3-mediated granulosa cell pyroptosis. Sci Rep 16, 14376 (2026). https://doi.org/10.1038/s41598-026-43536-2
Palavras-chave: síndrome dos ovários policísticos, células da granulosa, inflamação ovariana, morte celular, desequilíbrio hormonal