Clear Sky Science · it
SHP2 migliora la morfologia ovarica e la funzione steroidogenica in un modello di PCOS nelle ratte modulando la piroptosi delle cellule della granulosa mediata da IRE1α/XBP1/NLRP3
Perché è importante per la salute delle donne
La sindrome dell'ovaio policistico (PCOS) colpisce milioni di donne nel mondo, portando spesso cicli irregolari, difficoltà a concepire e rischi a lungo termine come diabete e malattie cardiovascolari. Tuttavia i meccanismi interni di questa condizione, in particolare ciò che va storto nelle cellule dell'ovaio, sono ancora in parte sconosciuti. Questo studio utilizza ratti e cellule ovariche umane per esplorare un interruttore cellulare chiave chiamato SHP2 e mostra come la sua modulazione possa proteggere l'ovaio dai danni indotti da un eccesso di ormoni maschili.
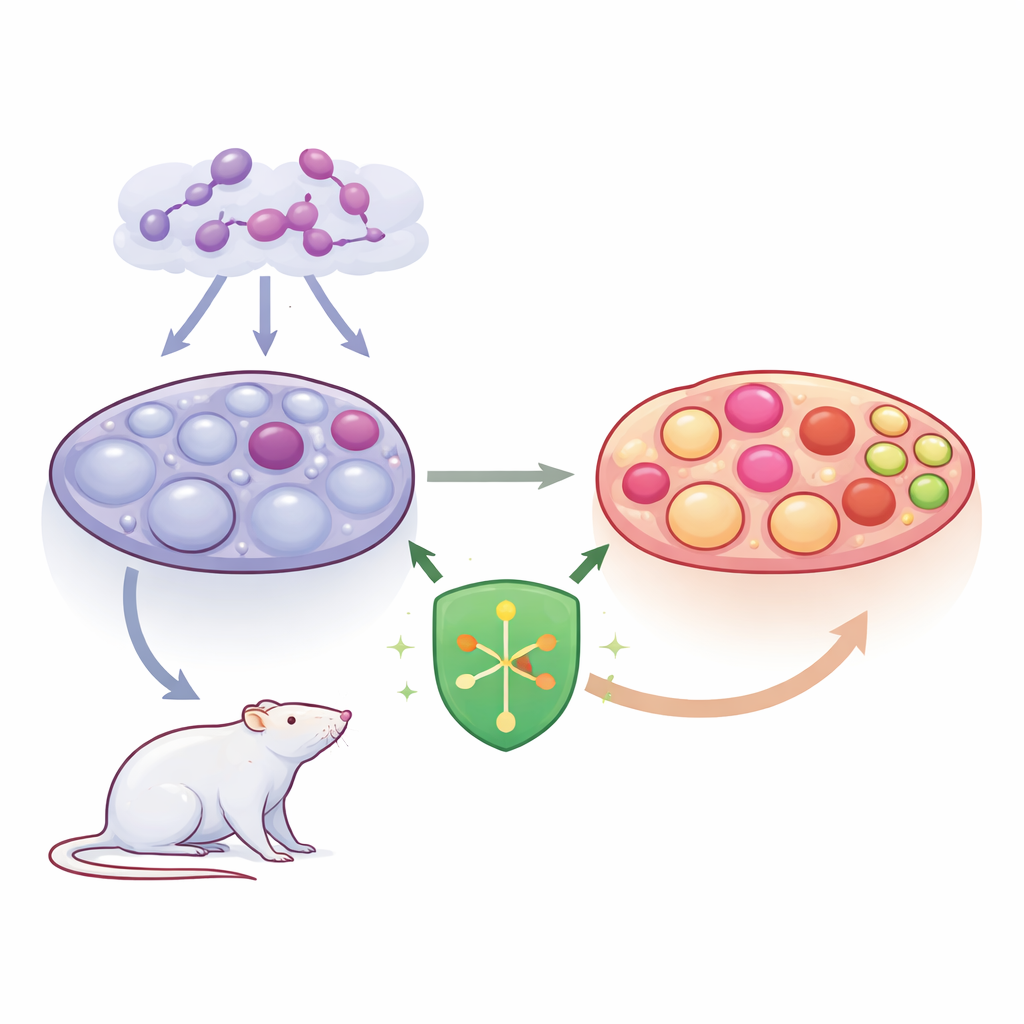
Un'analisi più approfondita della PCOS nell'ovaio
La PCOS è caratterizzata da uno squilibrio ormonale e dalla comparsa di numerose sacche piene di liquido, o cisti, nell'ovaio. Queste cisti riflettono follicoli che si sono bloccati invece di maturare e rilasciare un ovulo. Il gruppo si è concentrato sulle cellule della granulosa, che circondano e nutrono gli ovociti in sviluppo e contribuiscono alla sintesi degli ormoni sessuali. Quando queste cellule sono sotto stress o muoiono in modo anomalo, i follicoli falliscono e i livelli ormonali si alterano ulteriormente. I ricercatori hanno posto particolare attenzione a una forma infiammatoria e distruttiva di morte cellulare chiamata piroptosi, che provoca la rottura delle cellule e alimenta l'infiammazione ovarica.
Il ruolo protettivo di un interruttore cellulare
Gli scienziati hanno studiato SHP2, una molecola che funziona come una manopola di controllo per molti segnali cellulari, inclusi quelli legati alla crescita, alla sopravvivenza e all'infiammazione. In un modello di PCOS nelle ratte indotto dal farmaco letrozolo, hanno usato un virus per aumentare i livelli di SHP2 prima dell'insorgenza della sindrome. Rispetto alle ratte PCOS non trattate, quelle con livelli maggiori di SHP2 avevano ovaie più leggere, meno follicoli cistici di grandi dimensioni e un numero maggiore di strutture post-ovulatorie sane chiamate corpi lutei. Il profilo ormonale si è spostato in senso favorevole: estradiolo, testosterone e ormone luteinizzante sono diminuiti, mentre l'ormone follicolo-stimolante è aumentato, suggerendo un ripristino parziale dell'ovulazione e della produzione ormonale normale.
Come lo stress cellulare diventa tossico
Per capire cosa accadeva all'interno delle cellule della granulosa, il gruppo si è avvalso di cellule di tipo granulosa umane esposte al testosterone. L'elevato testosterone ha scatenato una risposta di stress nel reticolo endoplasmatico, il centro di lavorazione delle proteine della cellula, e ha attivato una catena di segnali centrata su IRE1α e XBP1. Questo a sua volta ha attivato un complesso proteico chiamato NLRP3, che guida la piroptosi. Le cellule hanno mostrato livelli più alti di marcatori molecolari associati alla formazione di pori nella membrana cellulare e alla morte infiammatoria. Allo stesso tempo, un'altra via che coinvolge un regolatore chiamato ZEB1 indeboliva una proteina strutturale, PKP3, e disturbava la macchina del ciclo cellulare che normalmente permette alle cellule della granulosa di crescere e dividersi in modo controllato.
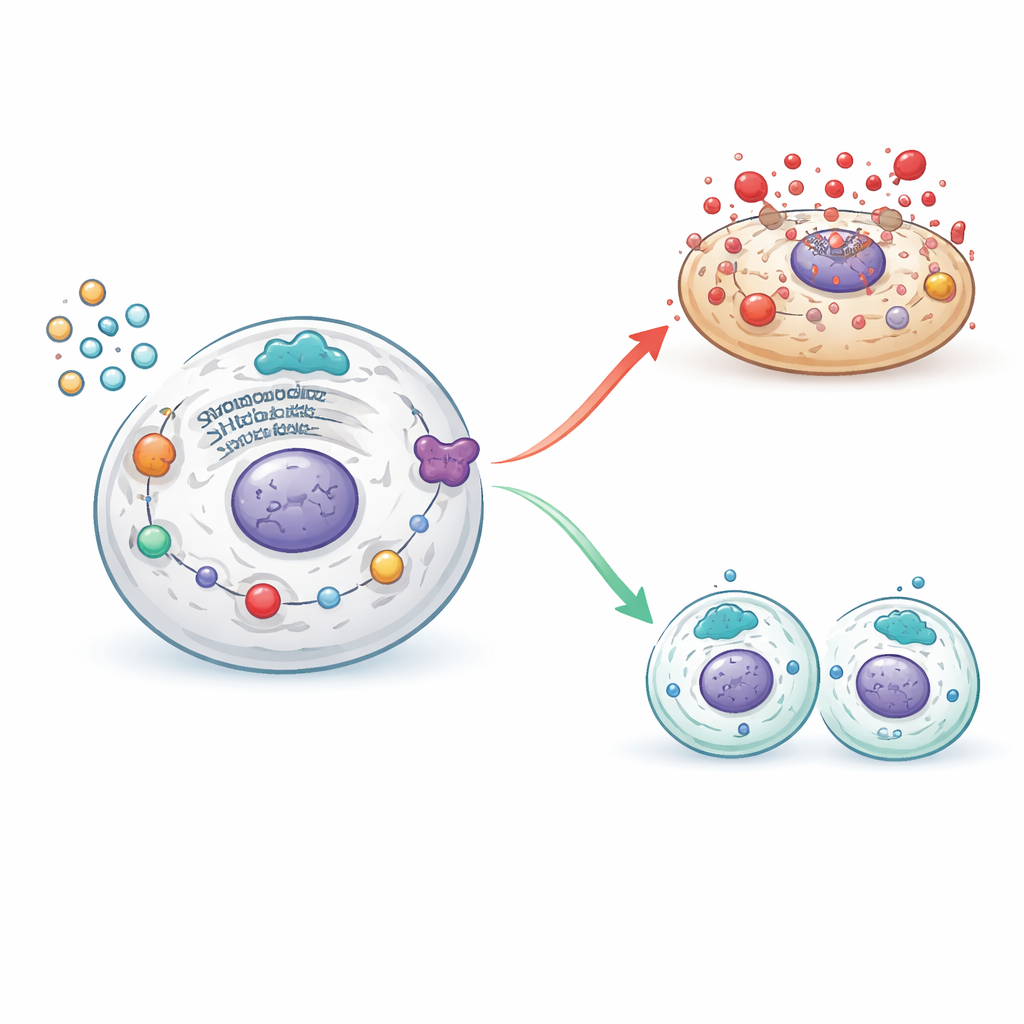
Bilanciare morte e rinnovamento nelle cellule ovariche
Quando l'attività di SHP2 è stata sostenuta, queste cascata dannose sono state attenuate: i segnali di stress cellulare e il macchinario della piroptosi sono diminuiti, mentre le molecole che supportano una divisione cellulare ordinata sono rimbalzate. Il blocco di SHP2 ha avuto l'effetto opposto, riattivando le vie di stress e infiammatorie e spingendo nuovamente le cellule della granulosa verso una morte distruttiva anziché verso una proliferazione sana. Combinando strumenti genetici e inibitori chimici, i ricercatori hanno mappato come SHP2 si trovi a un bivio tra infiammazione dannosa e rinnovamento tessutale, determinando se le cellule della granulosa muoiano in modo esplosivo o sopravvivano per sostenere i follicoli in maturazione.
Cosa potrebbe significare per terapie future
Per i non addetti ai lavori, il messaggio principale è che la PCOS non è solo un problema ormonale ma anche una patologia di cellule ovariche stressate e infiammate. Questo studio identifica SHP2 come un interruttore centrale che aiuta a decidere se le cellule della granulosa si autodistruggano in modo dannoso o continuino a funzionare e a dividersi normalmente. Nel modello di ratto, modulare le vie legate a SHP2 ha migliorato la struttura ovarica e l'equilibrio ormonale. Sebbene questo lavoro sia ancora in una fase precoce e preclinica, suggerisce che farmaci mirati e accuratamente progettati per regolare SHP2 e le vie di stress connesse potrebbero un giorno contribuire a ripristinare ovaie e fertilità più sane nelle persone con PCOS.
Citazione: Wang, D., Wang, J., Yang, B. et al. SHP2 improves ovarian morphology and steroidogenic function in a rat PCOS model by modulating IRE1α/XBP1/NLRP3-mediated granulosa cell pyroptosis. Sci Rep 16, 14376 (2026). https://doi.org/10.1038/s41598-026-43536-2
Parole chiave: sindrome dell'ovaio policistico, cellule della granulosa, infiammazione ovarica, morte cellulare, squilibrio ormonale