Clear Sky Science · de
SHP2 verbessert die Ovarmorphologie und die steroidogene Funktion in einem Rattenmodell des PCOS durch Modulation der IRE1α/XBP1/NLRP3-vermittelten Pyroptose von Granulosazellen
Warum das für die Gesundheit von Frauen wichtig ist
Das polyzystische Ovarialsyndrom (PCOS) betrifft weltweit Millionen von Frauen und führt häufig zu unregelmäßigen Menstruationen, Fruchtbarkeitsproblemen und langfristigen Risiken wie Diabetes und Herz-Kreislauf-Erkrankungen. Die genauen Abläufe, insbesondere die Störungen in den Zellen des Eierstocks, sind jedoch nur teilweise verstanden. Diese Studie nutzt Ratten und menschliche Ovarialzellen, um einen zentralen zellulären Schalter namens SHP2 zu untersuchen, und zeigt, wie die Modulation dieses Schalters den Ovar vor Schäden schützen kann, die durch überschüssige männliche Hormone ausgelöst werden.
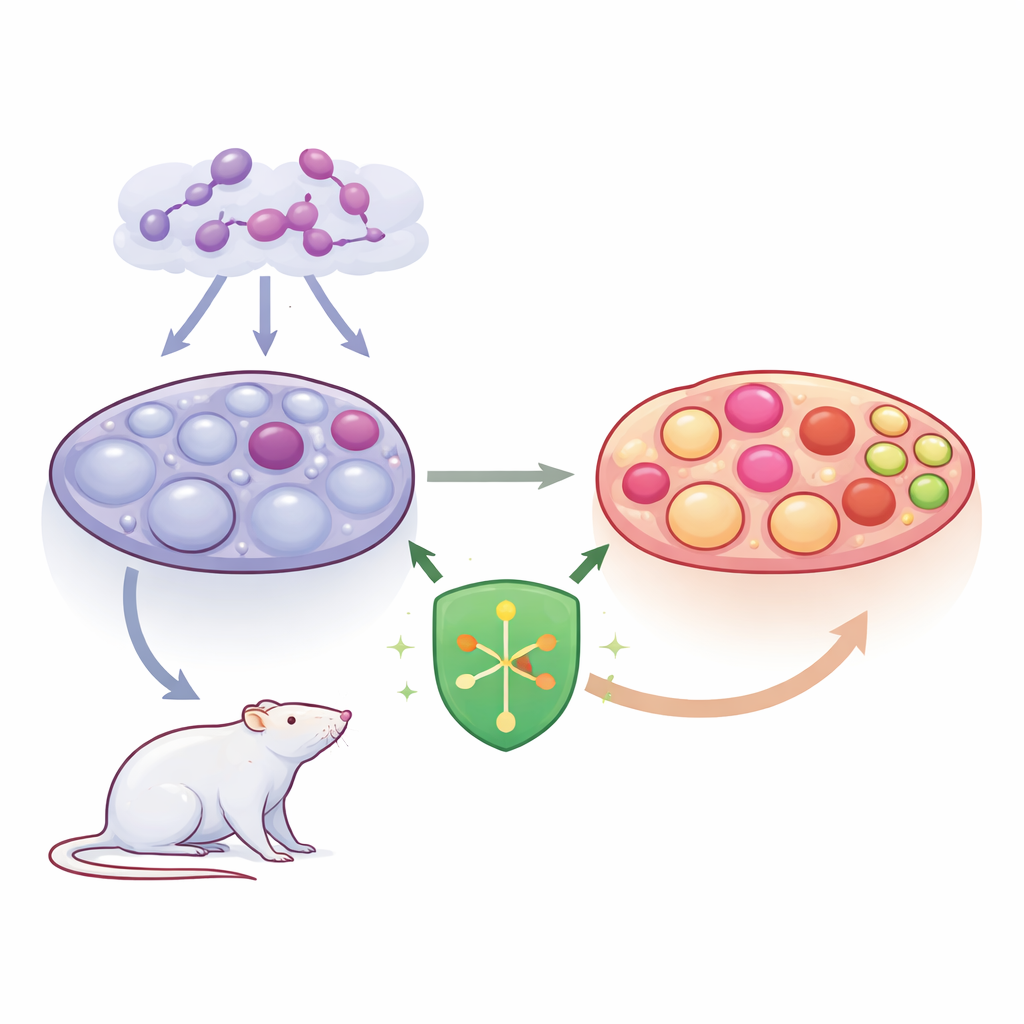
Ein genauerer Blick auf PCOS im Ovar
PCOS ist durch ein hormonelles Ungleichgewicht und das Auftreten zahlreicher flüssigkeitsgefüllter Bläschen oder Zysten im Ovar gekennzeichnet. Diese Zysten spiegeln Follikel wider, die stehen geblieben sind, statt zu reifen und ein Ei freizugeben. Das Team konzentrierte sich auf Granulosazellen, die sich um die sich entwickelnden Eizellen legen, sie ernähren und bei der Produktion von Sexualhormonen mitwirken. Wenn diese Zellen gestresst sind oder auf schädliche Weise absterben, versagen Follikel und die Hormonspiegel verschieben sich weiter. Die Forschenden interessierten sich besonders für eine feurige Form des Zelltods, die Pyroptose genannt wird, bei der Zellen aufplatzen und Entzündungen im Ovar antreiben.
Die schützende Rolle eines zellulären Schalters
Die Wissenschaftler untersuchten SHP2, ein Molekül, das wie ein Stellrad für viele Zellsignale wirkt, einschließlich solcher für Wachstum, Überleben und Entzündung. In einem Rattenmodell des PCOS, das durch Verabreichung des Wirkstoffs Letrozol erzeugt wurde, setzten sie ein Virus ein, um die SHP2-Spiegel zu erhöhen, bevor sich das Syndrom entwickelte. Im Vergleich zu unbehandelten PCOS-Ratten hatten die Tiere mit zusätzlichem SHP2 leichtere Ovarien, weniger große zystische Follikel und mehr gesunde, postovulatorische Strukturen, die sogenannten Corpora lutea. Ihr Hormonprofil verschob sich in eine günstigere Richtung: Östradiol, Testosteron und LH sanken, während das follikelstimulierende Hormon (FSH) anstieg, was auf eine normalere Ovulation und Hormonproduktion hindeutet.
Wie Zellstress toxisch wird
Um zu verstehen, was in den Granulosazellen vor sich ging, nutzte das Team menschliche granulosaähnliche Zellen, die Testosteron ausgesetzt wurden. Hohe Testosteronspiegel lösten eine Stressantwort im endoplasmatischen Retikulum, dem Proteinverarbeitungszentrum der Zelle, aus und aktivierten eine Signalkette, die IRE1α und XBP1 in den Mittelpunkt stellte. Dies wiederum aktivierte den Proteinkomplex NLRP3, der Pyroptose antreibt. Die Zellen zeigten erhöhte Spiegel molekularer Marker, die mit Porenbildung in der Zellmembran und entzündlichem Zelltod verknüpft sind. Gleichzeitig schwächte ein anderer Weg mit dem Regulator ZEB1 ein Strukturprotein, PKP3, und störte die Zellzyklusmaschinerie, die normalerweise ein kontrolliertes Wachstum und die Teilung der Granulosazellen erlaubt.
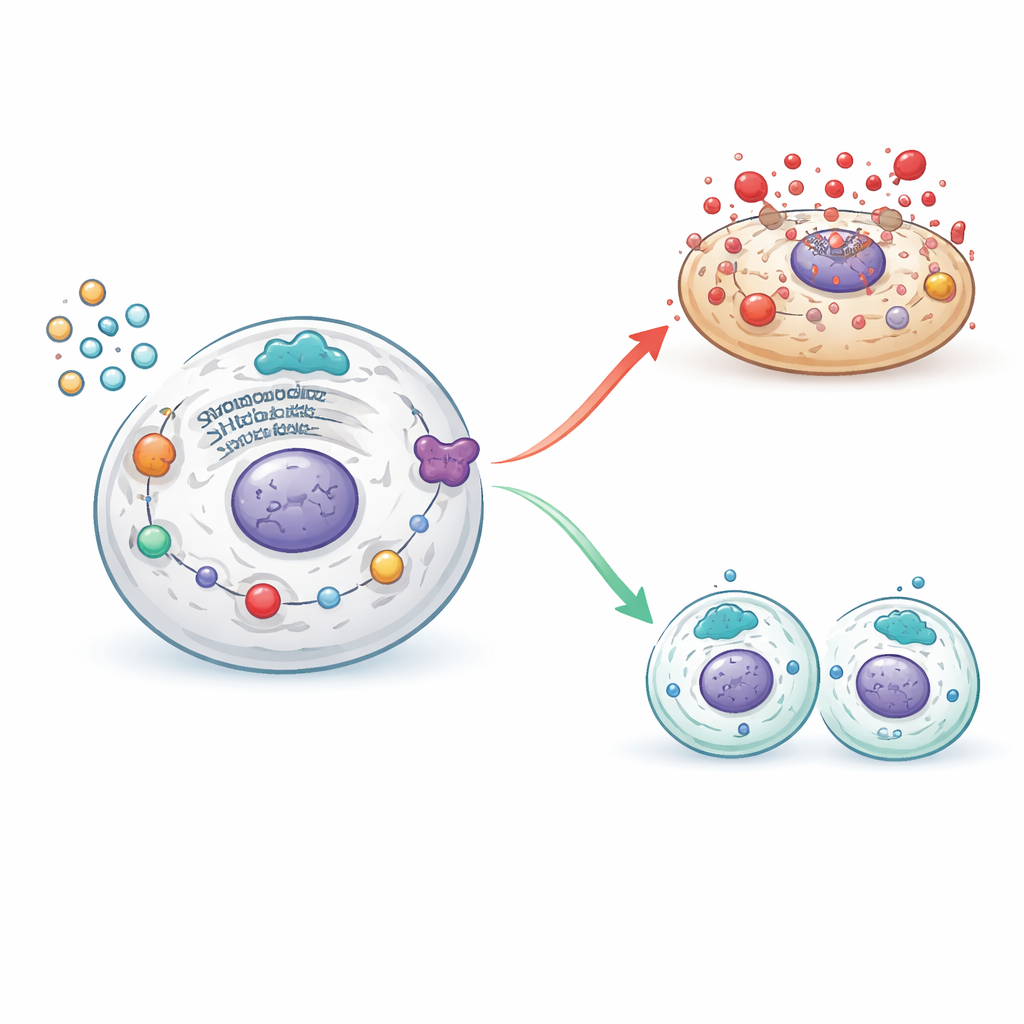
Gleichgewicht zwischen Tod und Erneuerung in Ovarzellen
Als die SHP2-Aktivität unterstützt wurde, wurden diese schädlichen Kaskaden abgeschwächt: Stresssignale der Zelle und die Pyroptose-Maschinerie verringerten sich, während Moleküle, die eine geordnete Zellteilung unterstützen, wieder zunahmen. Die Blockade von SHP2 hatte den gegenteiligen Effekt, reaktivierte Stress- und Entzündungswege und drängte die Granulosazellen erneut in einen destruktiven Tod statt in eine gesunde Proliferation. Durch die Kombination genetischer Werkzeuge und chemischer Inhibitoren kartierten die Forschenden, wie SHP2 an einer Kreuzung zwischen schädlicher Entzündung und Gewebeerneuerung sitzt und damit entscheidet, ob Granulosazellen explosionsartig sterben oder überleben, um reifende Follikel zu unterstützen.
Was das für künftige Therapien bedeuten könnte
Für Nichtfachleute ist die Kernbotschaft, dass PCOS nicht nur ein Hormonproblem ist, sondern auch eine Erkrankung gestresster und entzündeter Ovarzellen. Diese Studie identifiziert SHP2 als zentralen Schalter, der mitbestimmt, ob Granulosazellen sich auf eine Weise selbst zerstören, die das Ovar schädigt, oder ob sie weiterhin normal funktionieren und sich teilen. Im Rattenmodell verbesserte die Steuerung von SHP2-assoziierten Wegen die Ovarstruktur und das hormonelle Gleichgewicht. Obwohl diese Arbeiten noch in einem frühen, präklinischen Stadium sind, legen sie nahe, dass gezielt wirkende Medikamente, die SHP2 und seine vernetzten Stresswege anpassen, eines Tages helfen könnten, gesündere Ovarien und eine verbesserte Fruchtbarkeit bei Menschen mit PCOS wiederherzustellen.
Zitation: Wang, D., Wang, J., Yang, B. et al. SHP2 improves ovarian morphology and steroidogenic function in a rat PCOS model by modulating IRE1α/XBP1/NLRP3-mediated granulosa cell pyroptosis. Sci Rep 16, 14376 (2026). https://doi.org/10.1038/s41598-026-43536-2
Schlüsselwörter: polyzystisches Ovarialsyndrom, Granulosazellen, Ovarielle Entzündung, Zellsterben, Hormonungleichgewicht