Clear Sky Science · pl
SHP2 poprawia morfologię jajnika i funkcję steroidogenną w modelu PCOS u szczurów poprzez modulację IRE1α/XBP1/NLRP3-zależnej piroptozy komórek ziarnistych
Dlaczego to ma znaczenie dla zdrowia kobiet
Zespół policystycznych jajników (PCOS) dotyka miliony kobiet na całym świecie, często powodując nieregularne miesiączki, trudności z zajściem w ciążę oraz długoterminowe zagrożenia, takie jak cukrzyca i choroby serca. Wewnętrzne mechanizmy tej choroby, zwłaszcza to, co idzie nie tak w komórkach jajnika, są jednak wciąż tylko częściowo poznane. W badaniu wykorzystano szczury i ludzkie komórki jajnikowe, by zbadać ważny przełącznik komórkowy o nazwie SHP2 i pokazać, jak manipulacja tym przełącznikiem może chronić jajnik przed uszkodzeniami wywołanymi przez nadmiar hormonów męskich.
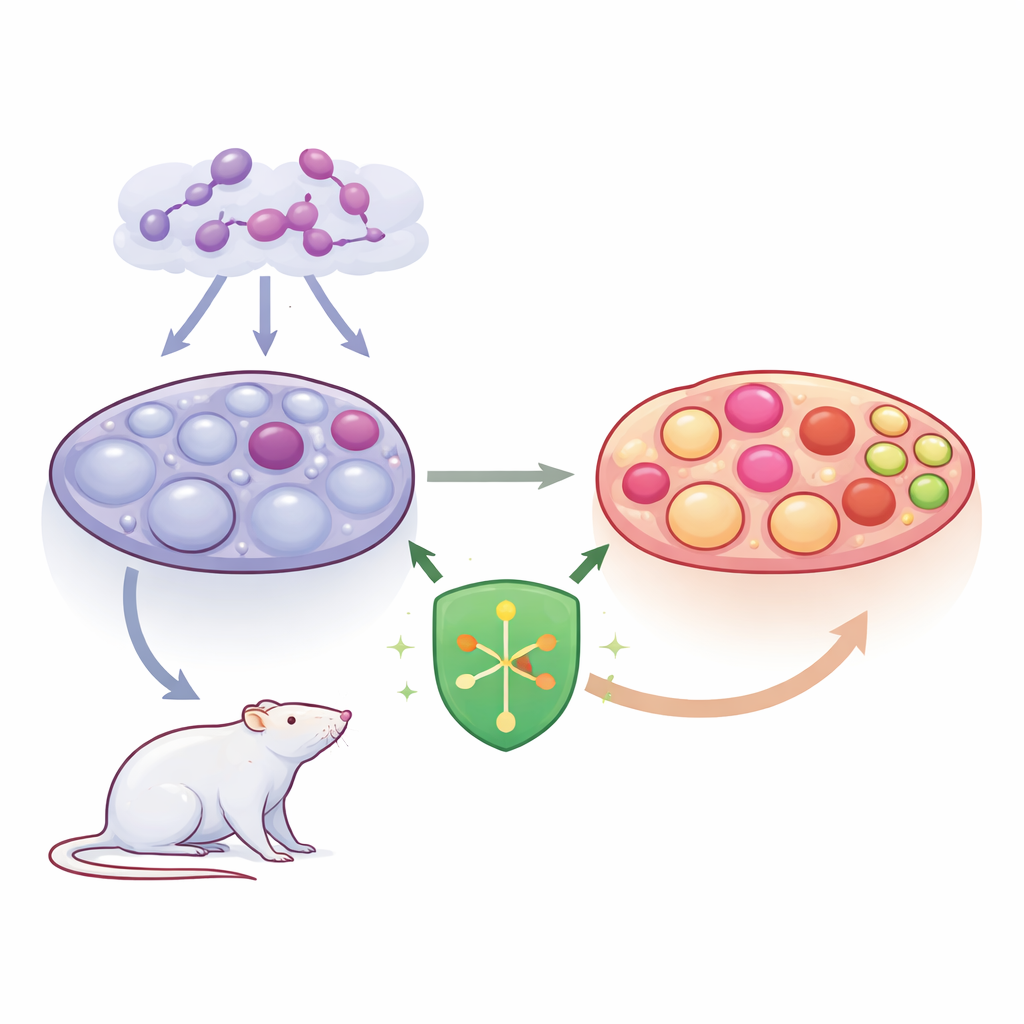
Bliższe spojrzenie na PCOS w jajniku
PCOS charakteryzuje się zaburzeniem równowagi hormonalnej i pojawieniem się licznych wypełnionych płynem torbieli w jajniku. Torbiele te odzwierciedlają pęcherzyki, które zatrzymały się w rozwoju zamiast dojrzewać i uwalniać komórkę jajową. Zespół skupił się na komórkach ziarnistych, które otaczają i odżywiają rozwijające się komórki jajowe oraz uczestniczą w produkcji hormonów płciowych. Gdy te komórki są zestresowane lub umierają w niewłaściwy sposób, pęcherzyki zawodzą, a poziomy hormonów ulegają dalszemu zaburzeniu. Badacze szczególnie interesowali się zapalną formą śmierci komórkowej zwaną piroptozą, która powoduje pękanie komórek i nasila stan zapalny w jajniku.
Ochronna rola przełącznika komórkowego
Naukowcy badali SHP2, cząsteczkę działającą jak pokrętło kontrolne dla wielu sygnałów komórkowych, w tym związanych z wzrostem, przeżyciem i stanem zapalnym. W modelu PCOS u szczurów wywołanym podawaniem letrazolu zastosowali wirusa do podwyższenia poziomu SHP2 zanim rozwinął się zespół. W porównaniu z nieleczonymi szczurami z PCOS, osobniki z dodatkowymi ilościami SHP2 miały lżejsze jajniki, mniej dużych torbielowatych pęcherzyków oraz więcej zdrowych struktur poowulacyjnych, zwanych ciałkami żółtymi. Profil hormonalny przesunął się w korzystnym kierunku: spadły stężenia estradiolu, testosteronu i hormonu luteinizującego, podczas gdy zwiększył się hormon folikulotropowy, co sugeruje bardziej normalną owulację i produkcję hormonów.
Jak stres komórkowy staje się toksyczny
Aby zrozumieć, co działo się w komórkach ziarnistych, zespół użył ludzkich komórek podobnych do ziarnistych wystawionych na działanie testosteronu. Wysokie stężenia testosteronu wywołały odpowiedź stresową retikulum endoplazmatycznego — centrum przetwarzania białek w komórce — i aktywowały kaskadę sygnałów skupioną wokół IRE1α i XBP1. To z kolei uruchomiło kompleks białkowy NLRP3, który napędza piroptozę. Komórki wykazywały wyższe poziomy molekularnych markerów związanych z tworzeniem porów w błonie komórkowej i zapalną śmiercią. Równocześnie inna ścieżka z udziałem regulatora ZEB1 osłabiała białko strukturalne PKP3 i zaburzała mechanizmy cyklu komórkowego, które normalnie pozwalają komórkom ziarnistym wzrastać i dzielić się w kontrolowany sposób.
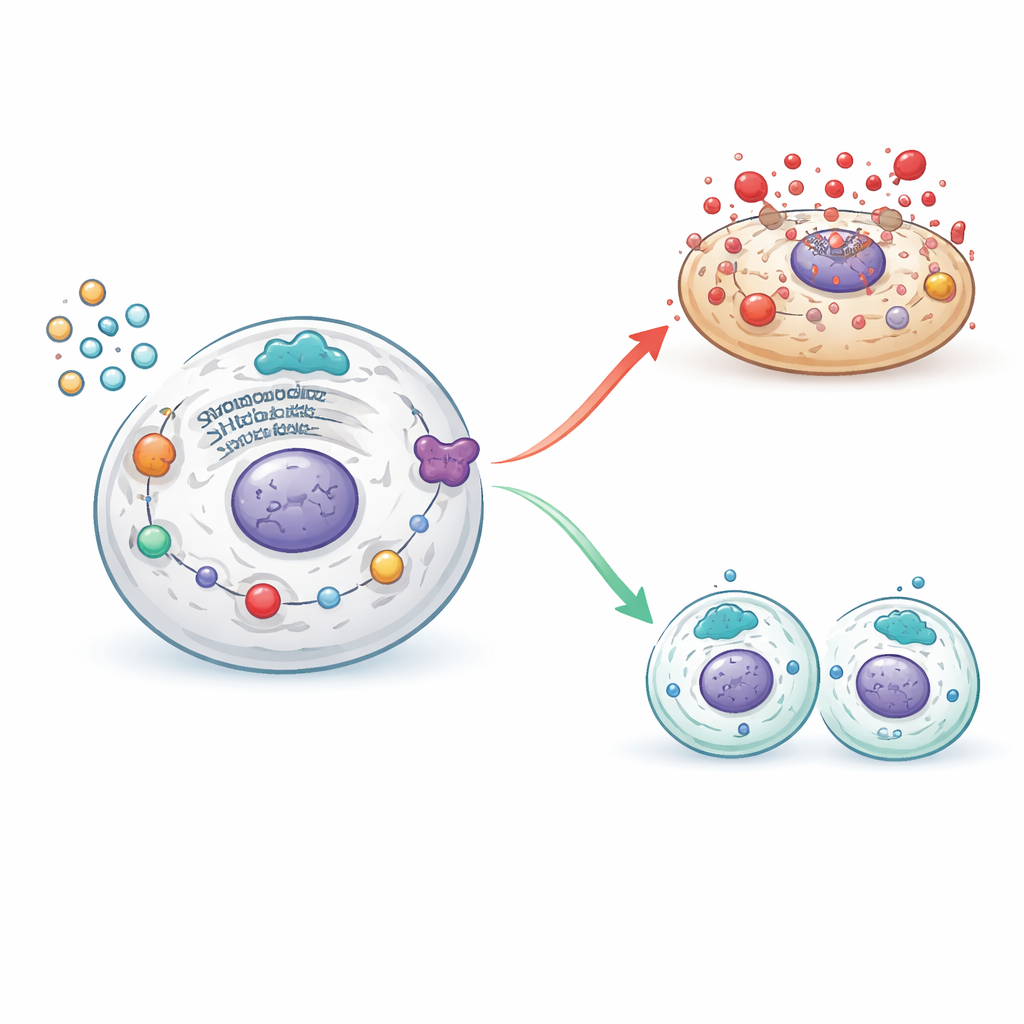
Równoważenie śmierci i odnowy w komórkach jajnika
Gdy aktywność SHP2 była wspierana, te szkodliwe kaskady zostały stłumione: sygnały stresu komórkowego i aparat piroptozy zmniejszyły się, podczas gdy molekuły wspierające uporządkowaną proliferację komórek odbudowały się. Blokada SHP2 działała odwrotnie, reaktywując szlaki stresu i zapalenia oraz ponownie skłaniając komórki ziarniste ku destrukcyjnej śmierci zamiast zdrowej proliferacji. Dzięki połączeniu narzędzi genetycznych i inhibitorów chemicznych badacze zmapowali, jak SHP2 znajduje się na skrzyżowaniu między szkodliwym zapaleniem a odnową tkanki, decydując, czy komórki ziarniste giną wybuchowo, czy przetrwają, by wspierać dojrzewające pęcherzyki.
Co to może znaczyć dla przyszłych terapii
Dla osób niebędących specjalistami kluczowy wniosek jest taki, że PCOS to nie tylko problem hormonalny, lecz także choroba wynikająca ze stresu i zapalenia komórek jajnika. To badanie identyfikuje SHP2 jako centralny przełącznik, który pomaga zdecydować, czy komórki ziarniste samozniszczą się w sposób szkodliwy dla jajnika, czy będą dalej prawidłowo funkcjonować i się dzielić. W modelu szczurzym modulacja szlaków związanych z SHP2 poprawiła strukturę jajnika i równowagę hormonalną. Choć prace te pozostają na wczesnym, przedklinicznym etapie, sugerują, że celowane leki regulujące SHP2 i powiązane ścieżki stresu mogą w przyszłości pomóc przywrócić zdrowsze jajniki i płodność u osób z PCOS.
Cytowanie: Wang, D., Wang, J., Yang, B. et al. SHP2 improves ovarian morphology and steroidogenic function in a rat PCOS model by modulating IRE1α/XBP1/NLRP3-mediated granulosa cell pyroptosis. Sci Rep 16, 14376 (2026). https://doi.org/10.1038/s41598-026-43536-2
Słowa kluczowe: zespół policystycznych jajników, komórki ziarniste, zapalenie jajnika, śmierć komórkowa, zaburzenia hormonalne