Clear Sky Science · ar
يحسّن SHP2 شكل المبيض ووظيفة توليد الهرمونات في نموذج PCOS للفئران عن طريق تعديل الذوبان الخلوي في الخلايا الحبيبية المنقوطة بواسطة IRE1α/XBP1/NLRP3
لماذا هذا مهم لصحة النساء
تؤثر متلازمة المبيض المتعدد الكيسات (PCOS) على ملايين النساء حول العالم، وغالبًا ما تتسبب في اضطراب الدورات الشهرية وصعوبة الحمل ومخاطر طويلة الأمد مثل السكري وأمراض القلب. ومع ذلك، فإن الآليات الداخلية لهذه الحالة، وبخاصة ما يخطئ داخل خلايا المبيض، لا تزال مفهومة جزئياً فقط. تستخدم هذه الدراسة الفئران وخلايا المبيض البشرية لاستكشاف مفتاح خلوي مهم يُدعى SHP2 وتُظهر كيف أن تعديل هذا المفتاح يمكن أن يحمي المبيض من التلف الناتج عن زيادة الهرمونات الذكرية.
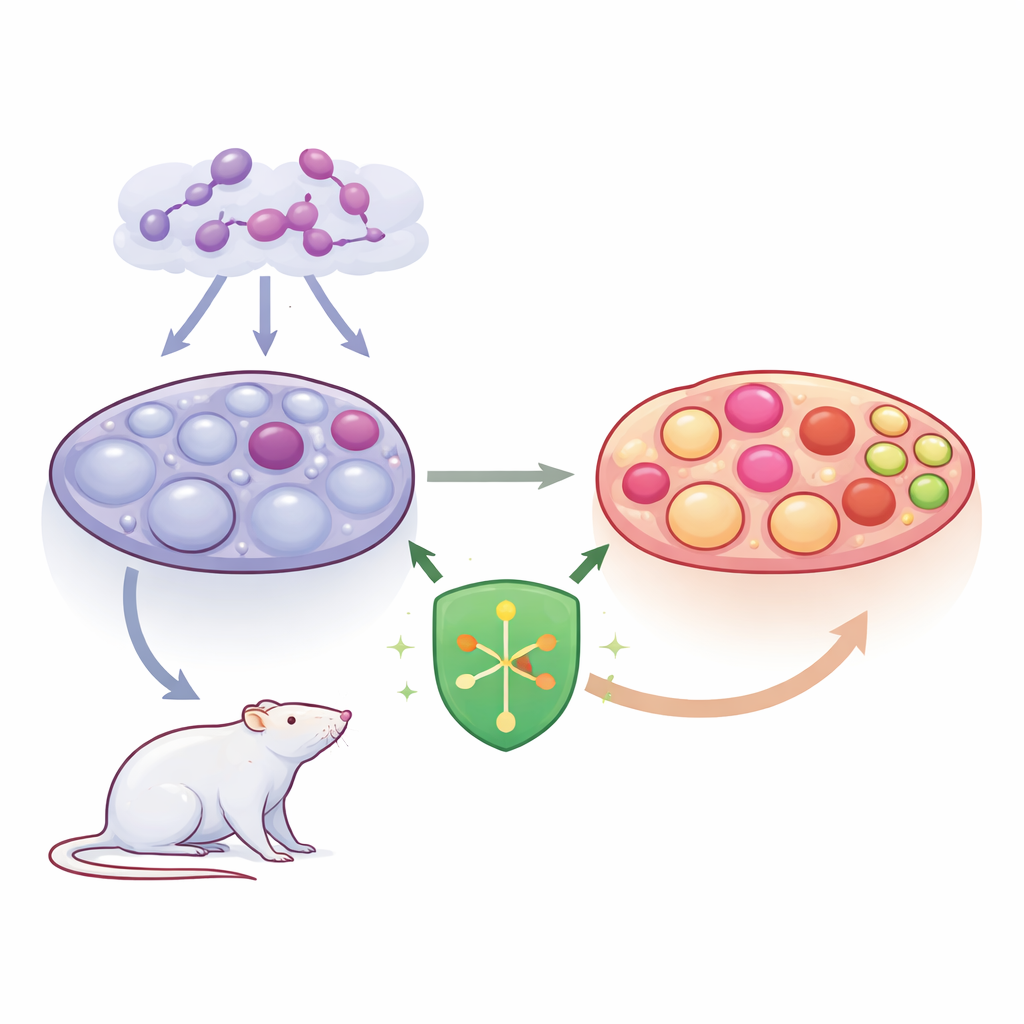
نظرة أعمق على PCOS في المبيض
تتميز متلازمة المبيض المتعدد الكيسات بخلل هرموني وظهور العديد من الأكياس المملوءة بالسائل في المبيض. تعكس هذه الأكياس بُويضات توقفت عن النضج بدلًا من الإباضة. ركز الفريق على الخلايا الحبيبية، التي تحيط بالبويضات النامية وتغذيها وتساهم في إنتاج هرمونات الجنس. عندما تتعرض هذه الخلايا للضغط أو تموت بطريقة خاطئة، تفشل الجُريبات وتزداد اضطرابات المستويات الهرمونية. كان الباحثون مهتمين بشكل خاص بنوع من موت الخلايا الالتهابي والهدّام يسمى البيروپتوز (pyroptosis)، الذي يؤدي إلى تمزق الخلايا ويغذي الالتهاب داخل المبيض.
الدور الوقائي لمفتاح خلوي
درس العلماء SHP2، وهو جزيء يعمل كمقِبض تحكم للعديد من إشارات الخلايا، بما في ذلك تلك المرتبطة بالنمو والبقاء والالتهاب. في نموذج فئران لـ PCOS تم إنشاؤه بإعطاء دواء الليتروزول، استخدموا فيروسًا لرفع مستويات SHP2 قبل تطور المتلازمة. بالمقارنة مع الفئران المصابة التي لم تُعالج، كانت الفئران ذات SHP2 الزائد ذات مبايض أخف وزنًا، وعدد أقل من الجريبات الكيسية الكبيرة، ومزيد من البُنى الصحية ما بعد الإباضة المسماة الأجسام الصفراء. تحوّلت ملفاتهم الهرمونية في اتجاه إيجابي: انخفض الإستراديول والتستوستيرون والهرمون الملوتن، بينما ارتفع هرمون المنشط للجريب، مما يوحي بإباضة وإنتاج هرموني أكثر طبيعية.
كيف يتحول ضغط الخلية إلى سم
لفهم ما كان يحدث داخل الخلايا الحبيبية، لجأ الفريق إلى خلايا تشبه الخلايا الحبيبية البشرية المعرضة للتستوستيرون. حرض التستوستيرون العالي استجابة ضغط في الشبكة الإندوبلازمية، مركز معالجة البروتين في الخلية، ونشّط سلسلة إشارات تتمحور حول IRE1α وXBP1. بدورها، نشّطت هذه السلسلة مركبًا بروتينيًا يسمى NLRP3، الذي يقود البيروپتوز. أظهرت الخلايا مستويات أعلى من العلامات الجزيئية المرتبطة بتشكيل مسامات في غشاء الخلية والموت الالتهابي. وفي الوقت نفسه، أضعفت مسارًا آخر يشمل منظمًا يدعى ZEB1 بروتينًا هيكليًا يُسمى PKP3، وعرقلت آليات دورة الخلية التي تسمح عادة للخلايا الحبيبية بالنمو والانقسام بطريقة محكومة.
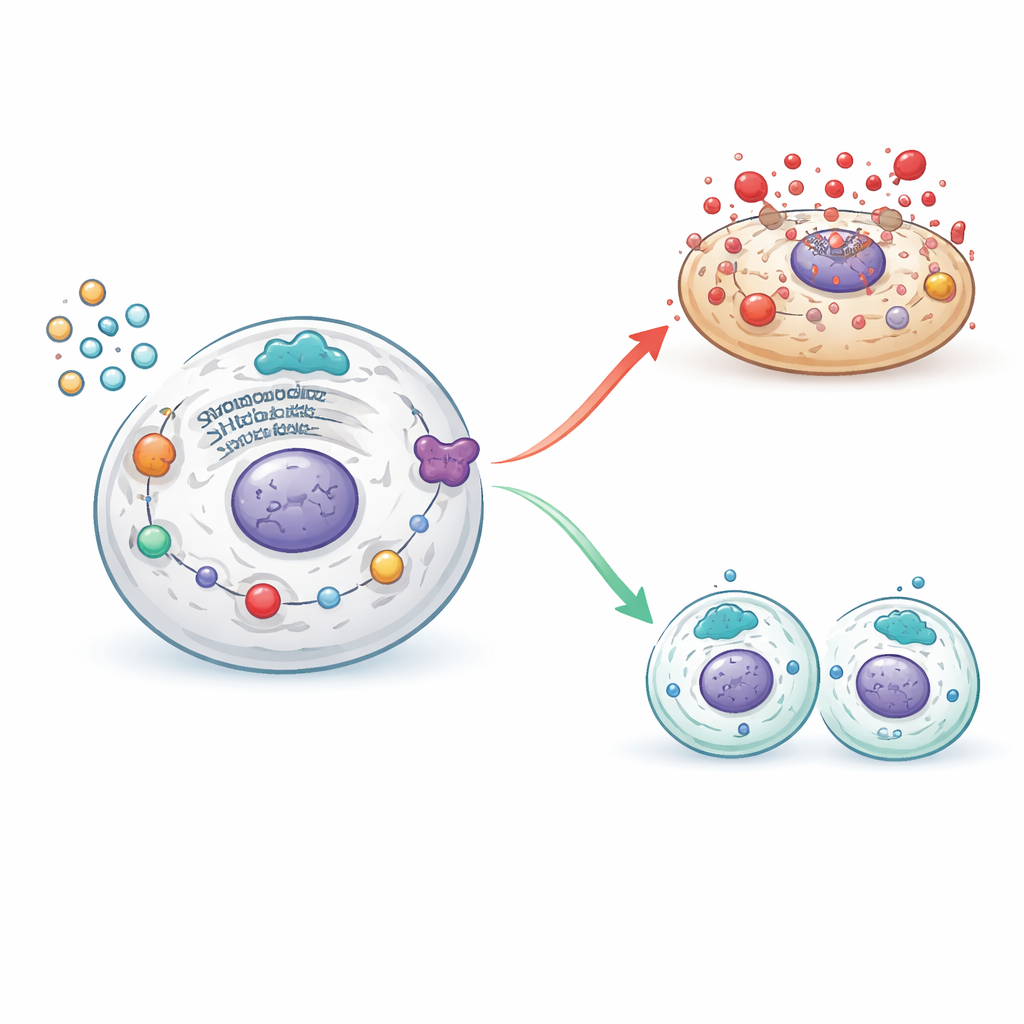
موازنة الموت والتجديد في خلايا المبيض
عندما دُعم نشاط SHP2، خفتت هذه الشلالات الضارة: تناقصت إشارات ضغط الخلية وآليات البيروپتوز، بينما تعافت الجزيئات التي تدعم الانقسام الخلوي المنظم. وكان لعرقلة SHP2 الأثر المعاكس، فأعاد تنشيط مسارات الضغط والالتهاب ودفع الخلايا الحبيبية نحو الموت التدميري بعيدًا عن التكاثر الصحي. من خلال دمج أدوات جينية ومثبطات كيميائية، رسم الباحثون خريطة لكيفية تموضع SHP2 عند مفترق طرق بين الالتهاب الضار وتجديد النسيج، مانعًا أو مسهماً في تحديد ما إذا كانت الخلايا الحبيبية ستموت بانفجار أم تبقى لتدعم الجريبات النامية.
ماذا قد يعني هذا للعلاجات المستقبلية
للجمهور العام، الرسالة الأساسية هي أن PCOS ليس مجرد مشكلة هرمونية، بل أيضاً مرض للخلايا المبيضية المتوترة والملتهبة. تحدد هذه الدراسة SHP2 كمفتاح مركزي يساعد في تقرير ما إذا كانت الخلايا الحبيبية ستدمر نفسها بطريقة تضر المبيض أو ستستمر في الأداء والانقسام بشكل طبيعي. في نموذج الفئران، أدى توجيه مسارات مرتبطة بـ SHP2 إلى تحسن بنية المبيض وتوازن الهرمونات. وعلى الرغم من أن هذا العمل لا يزال في مرحلة قبل السريرية المبكرة، فإنه يشير إلى أن أدوية موجهة بعناية تعدل SHP2 والمسارات المرتبطة به قد تساعد في يوم ما على استعادة مبايض أكثر صحة والخصوبة لدى الأشخاص المصابين بـ PCOS.
الاستشهاد: Wang, D., Wang, J., Yang, B. et al. SHP2 improves ovarian morphology and steroidogenic function in a rat PCOS model by modulating IRE1α/XBP1/NLRP3-mediated granulosa cell pyroptosis. Sci Rep 16, 14376 (2026). https://doi.org/10.1038/s41598-026-43536-2
الكلمات المفتاحية: متلازمة المبيض المتعدد الكيسات, الخلايا الحبيبية, التهاب المبيض, موت الخلايا, اختلال التوازن الهرموني