Clear Sky Science · ru
SHP2 улучшает морфологию яичников и стероидогенную функцию в модели СПКЯ у крыс путем модуляции IRE1α/XBP1/NLRP3-опосредованной пироптозы гранулезных клеток
Почему это важно для женского здоровья
Синдром поликистозных яичников (СПКЯ) затрагивает миллионы женщин во всем мире, часто приводя к нерегулярным менструациям, проблемам с зачатием и долгосрочным рискам, таким как диабет и заболевания сердца. При этом внутренние механизмы этого состояния, особенно то, что идет не так в клетках яичника, остаются частично неясными. В этом исследовании на крысах и человеческих клетках яичника изучают ключевой клеточный переключатель SHP2 и показывают, как его модуляция может защищать яичник от повреждений, вызванных избытком андрогенов.
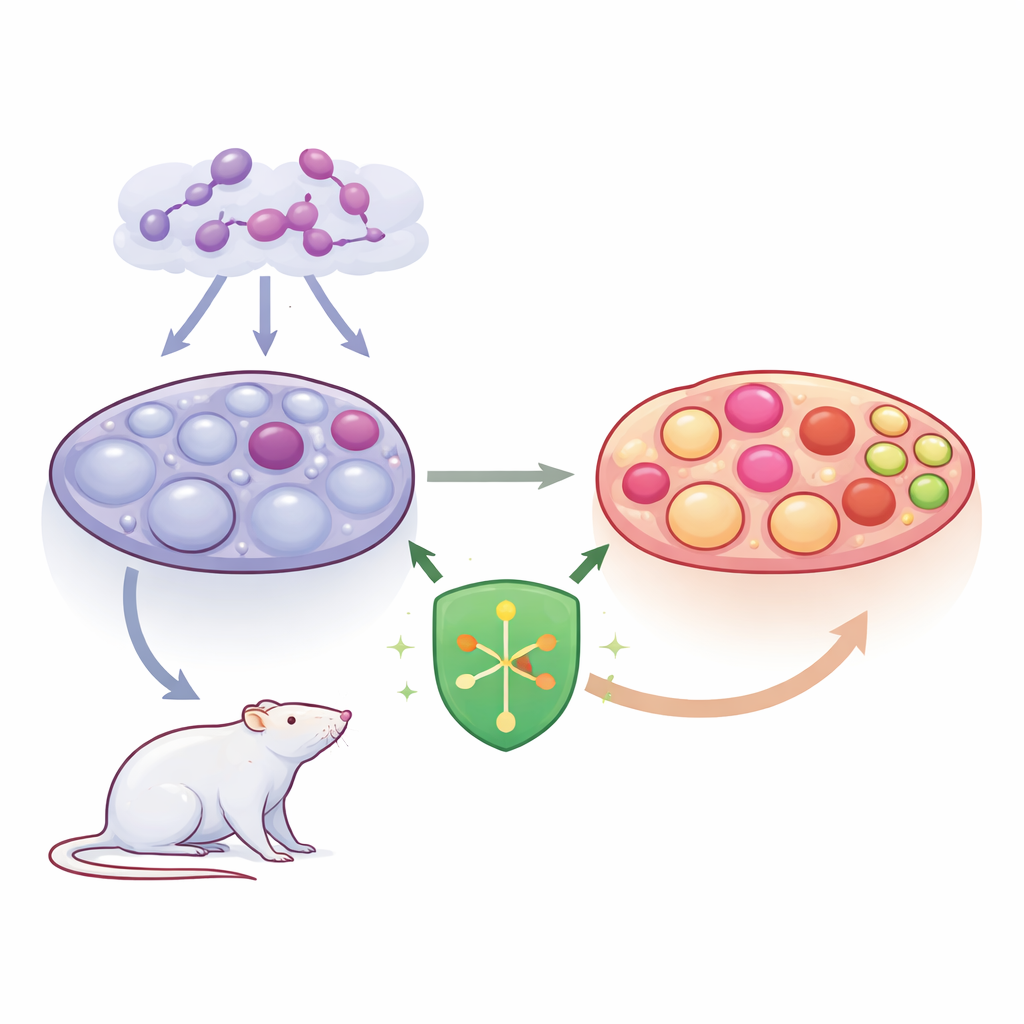
Более пристальный взгляд на СПКЯ в яичнике
СПКЯ характеризуется гормональным дисбалансом и появлением множества заполненных жидкостью пузырьков — кист в яичнике. Эти кисты отражают фолликулы, развитие которых остановилось вместо созревания и овуляции. Исследователи сосредоточились на гранулезных клетках, которые окружают и питают развивающиеся яйцеклетки и участвуют в синтезе половых гормонов. Когда эти клетки испытывают стресс или погибают патологическим образом, фолликулы разрушаются, а гормональный фон еще больше искажается. Особый интерес представляла пироптоз — «воспламеняющаяся» форма гибели клеток, при которой клетки разрываются и усиливают воспаление в яичнике.
Защитная роль клеточного переключателя
Ученые изучали SHP2 — молекулу, действующую как регулятор множества клеточных сигналов, включая те, что связаны с ростом, выживанием и воспалением. В модели СПКЯ у крыс, вызванной летрозолом, они использовали вирус для повышения уровня SHP2 до развития синдрома. По сравнению с не подвергавшимися лечению крысами с СПКЯ, у животных с повышенным SHP2 были более легкие по массе яичники, меньше крупных кистозных фолликулов и больше здоровых постовуляторных структур — желтых тел. Их гормональный профиль сместился в благоприятную сторону: уровни эстрадиола, тестостерона и лютеинизирующего гормона снизились, в то время как фолликулостимулирующий гормон вырос, что указывает на более нормальную овуляцию и гормонопродукцию.
Как стресс клетки становится токсичным
Чтобы понять происходящее в гранулезных клетках, команда обратилась к человеческим гранулезоподобным клеткам, подвергнутым воздействию тестостерона. Высокий уровень тестостерона вызвал стресс в эндоплазматическом ретикулуме — центре обработки белков клетки — и активировал каскад сигналов, сосредоточенный вокруг IRE1α и XBP1. Это, в свою очередь, запустило комплекс белков NLRP3, который приводит к пироптозу. Клетки демонстрировали повышенные уровни молекулярных маркеров, связанных с формированием пор в мембране и воспалительной гибелью. Одновременно другой путь с участием регулятора ZEB1 ослаблял структурный белок PKP3 и нарушал клеточный цикл, который обычно обеспечивает контролируемый рост и деление гранулезных клеток.
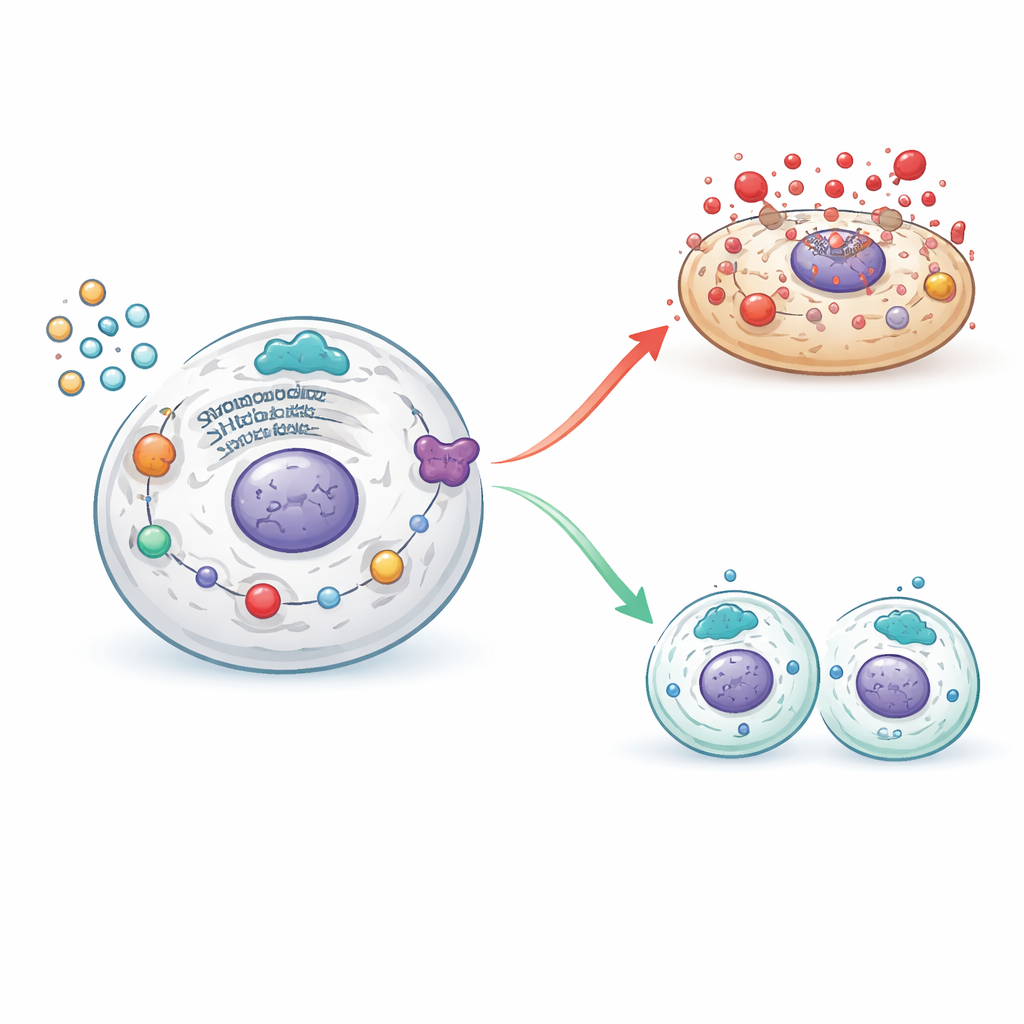
Баланс между гибелью и обновлением в клетках яичника
При поддержке активности SHP2 эти вредоносные каскады ослабевали: сигналы клеточного стресса и механизмы пироптоза снижались, в то время как молекулы, поддерживающие упорядоченное деление клеток, восстанавливались. Блокирование SHP2 имело противоположный эффект — повторно активировало стрессовые и воспалительные пути и снова направляло гранулезные клетки к разрушительной гибели вместо здоровой пролиферации. Сочетая генетические подходы и химические ингибиторы, исследователи проследили, как SHP2 находится на пересечении между вредоносным воспалением и восстановлением ткани, определяя, погибнут ли гранулезные клетки взрывным образом или выживут, чтобы поддержать созревающие фолликулы.
Что это может значить для будущих методов лечения
Для неспециалистов ключевой вывод таков: СПКЯ — это не только гормональная проблема, но и заболевание, связанное со стрессом и воспалением клеток яичника. В этом исследовании SHP2 выделяется как центральный переключатель, который помогает решать, будут ли гранулезные клетки самоуничтожаться способом, вредящим яичнику, или продолжат нормально функционировать и делиться. В модели у крыс модуляция путей, связанных с SHP2, улучшала структуру яичника и гормональный баланс. Хотя работа находится на ранней доклинической стадии, она предполагает, что прицельно направленные препараты, корректирующие SHP2 и связанные с ним стрессовые пути, могут в будущем помочь восстановить здоровье яичников и фертильность у людей с СПКЯ.
Цитирование: Wang, D., Wang, J., Yang, B. et al. SHP2 improves ovarian morphology and steroidogenic function in a rat PCOS model by modulating IRE1α/XBP1/NLRP3-mediated granulosa cell pyroptosis. Sci Rep 16, 14376 (2026). https://doi.org/10.1038/s41598-026-43536-2
Ключевые слова: синдром поликистозных яичников, гранулезные клетки, воспаление яичников, гибель клеток, гормональный дисбаланс