Clear Sky Science · es
SHP2 mejora la morfología ovárica y la función esteroidogénica en un modelo de SOP en ratas al modular la piroptosis de las células de la granulosa mediada por IRE1α/XBP1/NLRP3
Por qué importa para la salud de las mujeres
El síndrome de ovario poliquístico (SOP) afecta a millones de mujeres en todo el mundo, provocando con frecuencia periodos irregulares, dificultad para concebir y riesgos a largo plazo como diabetes y enfermedades cardiovasculares. Sin embargo, los mecanismos internos de esta afección, especialmente lo que falla dentro de las células del ovario, siguen siendo solo parcialmente conocidos. Este estudio utiliza ratas y células ováricas humanas para explorar un interruptor celular clave llamado SHP2 y muestra cómo modular ese interruptor puede proteger al ovario del daño provocado por el exceso de hormonas masculinas.
Una mirada más cercana al SOP en el ovario
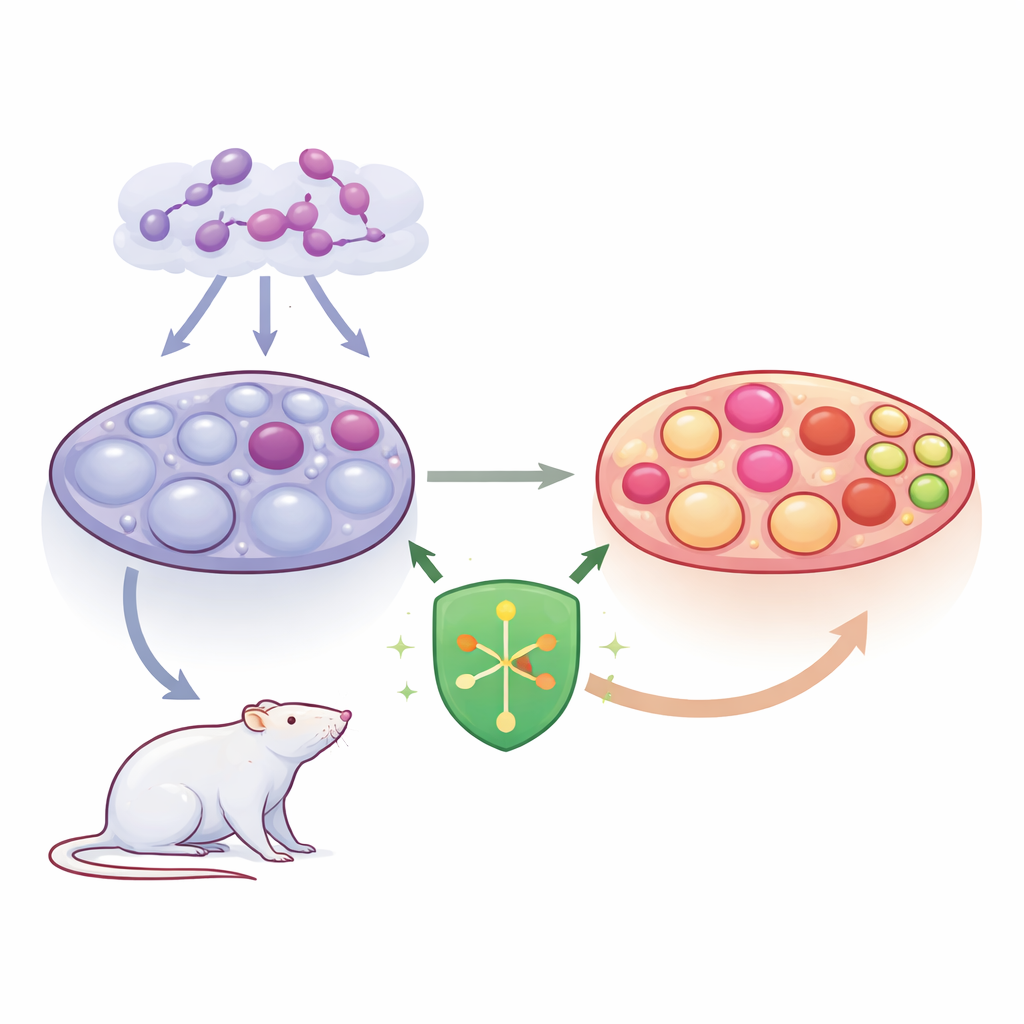
El SOP se caracteriza por un desequilibrio hormonal y la aparición de numerosos sacos llenos de líquido, o quistes, en el ovario. Estos quistes reflejan folículos que se han estancado en lugar de madurar y liberar un óvulo. El equipo se centró en las células de la granulosa, que rodean y nutren los óvulos en desarrollo y contribuyen a la producción de hormonas sexuales. Cuando estas células están estresadas o mueren de forma inadecuada, los folículos fracasan y los niveles hormonales se distorsionan aún más. Los investigadores se interesaron particularmente en una forma inflamatoria de muerte celular llamada piroptosis, que hace que las células estallen y alimenta la inflamación en el ovario.
El papel protector de un interruptor celular
Los científicos investigaron SHP2, una molécula que actúa como un control para muchas señales celulares, incluidas las relacionadas con el crecimiento, la supervivencia y la inflamación. En un modelo de SOP en ratas inducido con el fármaco letrozol, usaron un virus para aumentar los niveles de SHP2 antes de que se desarrollara el síndrome. En comparación con las ratas con SOP no tratadas, las que tenían SHP2 adicional presentaron ovarios más ligeros, menos folículos quísticos grandes y más estructuras sanas posovulatorias llamadas cuerpos lúteos. Su perfil hormonal cambió en una dirección favorable: descendieron el estradiol, la testosterona y la hormona luteinizante, mientras que aumentó la hormona foliculoestimulante, lo que sugiere una ovulación y una producción hormonal más normales.
Cómo el estrés celular se vuelve tóxico
Para entender lo que ocurría dentro de las células de la granulosa, el equipo recurrió a células humanas similares a las de la granulosa expuestas a testosterona. La testosterona elevada desencadenó una respuesta de estrés en el retículo endoplásmico, el centro de procesamiento de proteínas de la célula, y activó una cadena de señales centrada en IRE1α y XBP1. Esto, a su vez, activó un complejo proteico llamado NLRP3, que impulsa la piroptosis. Las células mostraron niveles más altos de marcadores moleculares asociados a la formación de poros en la membrana celular y a la muerte inflamatoria. Al mismo tiempo, otra vía que implicaba al regulador ZEB1 debilitó una proteína estructural, PKP3, y perturbó la maquinaria del ciclo celular que normalmente permite que las células de la granulosa crezcan y se dividan de forma controlada.
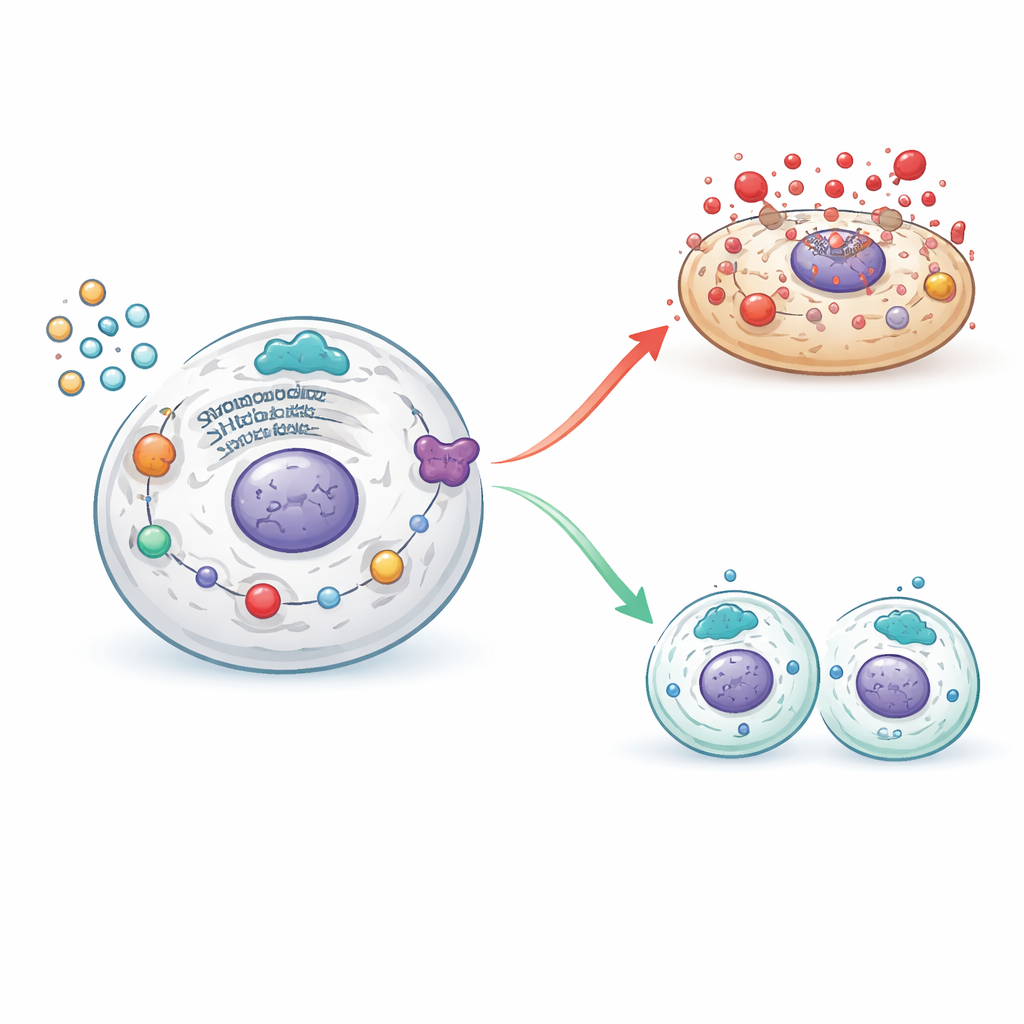
Equilibrando muerte y renovación en las células ováricas
Cuando se apoyó la actividad de SHP2, estas cascadas dañinas se atenuaron: se redujeron las señales de estrés celular y la maquinaria de la piroptosis, mientras que las moléculas que favorecen la división celular ordenada se recuperaron. Bloquear SHP2 tuvo el efecto opuesto, reactivando vías de estrés e inflamación y empujando de nuevo a las células de la granulosa hacia una muerte destructiva en lugar de hacia una proliferación saludable. Mediante herramientas genéticas e inhibidores químicos, los investigadores cartografiaron cómo SHP2 se sitúa en una encrucijada entre la inflamación dañina y la renovación tisular, determinando si las células de la granulosa mueren de forma explosiva o sobreviven para apoyar la maduración de los folículos.
Qué podría significar para futuros tratamientos
Para quienes no son especialistas, el mensaje clave es que el SOP no es solo un problema hormonal, sino también una enfermedad de células ováricas estresadas e inflamadas. Este estudio identifica a SHP2 como un interruptor central que ayuda a decidir si las células de la granulosa se autodestruyen de una manera que daña el ovario o continúan funcionando y dividiéndose con normalidad. En el modelo de rata, orientar las vías relacionadas con SHP2 mejoró la estructura ovárica y el equilibrio hormonal. Aunque este trabajo aún está en una fase preclínica temprana, sugiere que fármacos cuidadosamente dirigidos que ajusten SHP2 y sus vías de estrés conectadas podrían algún día ayudar a restaurar ovarios y la fertilidad más saludables en personas con SOP.
Cita: Wang, D., Wang, J., Yang, B. et al. SHP2 improves ovarian morphology and steroidogenic function in a rat PCOS model by modulating IRE1α/XBP1/NLRP3-mediated granulosa cell pyroptosis. Sci Rep 16, 14376 (2026). https://doi.org/10.1038/s41598-026-43536-2
Palabras clave: síndrome de ovario poliquístico, células de la granulosa, inflamación ovárica, muerte celular, desequilibrio hormonal