Clear Sky Science · zh
小胶质细胞与星形胶质细胞之间的神经炎症对话在iPSC来源的中枢神经系统HIV感染模型中促进病毒复制
为何HIV相关的脑部炎症依然重要
在现代HIV治疗下,许多人可以长寿并维持血液中病毒处于不可检测的水平。然而,一个顽固的问题仍然存在:大量感染者即便在有效治疗下,仍然出现记忆问题、思维迟缓或注意力难以集中。该研究提出了一个对患者和临床医师都很关键的问题:如果血液中的病毒大多被控制,为什么脑部炎症——以及随之出现的精神模糊——仍然常常持续存在?
把聚光灯照在大脑的支持细胞上
研究者没有把注意力放在传递信号的神经元上,而是转向大脑中的两类“支持”细胞:小胶质细胞和星形胶质细胞。小胶质细胞相当于大脑内驻留的免疫细胞,星形胶质细胞则负责维持神经元的健康环境。团队使用人类干细胞技术,从供体皮肤细胞培养出实验室版的这些细胞——称为诱导小胶质细胞和诱导星形胶质细胞。这一方法使他们能够在不使用患者脑组织的情况下,尽可能贴近人类脑生物学进行研究。
首先,他们确认了实验室培养的小胶质细胞具有真实小胶质细胞的特征:形态合适,表达典型基因,并携带HIV进入细胞所需的受体。这些小胶质细胞可以被HIV感染并允许病毒复制,尽管复制效率不如来源于血液的免疫细胞(称为巨噬细胞)。与巨噬细胞不同,小胶质细胞对感染的炎症反应较弱,仅产生少量通常伴随强抗病毒反应的警报分子。
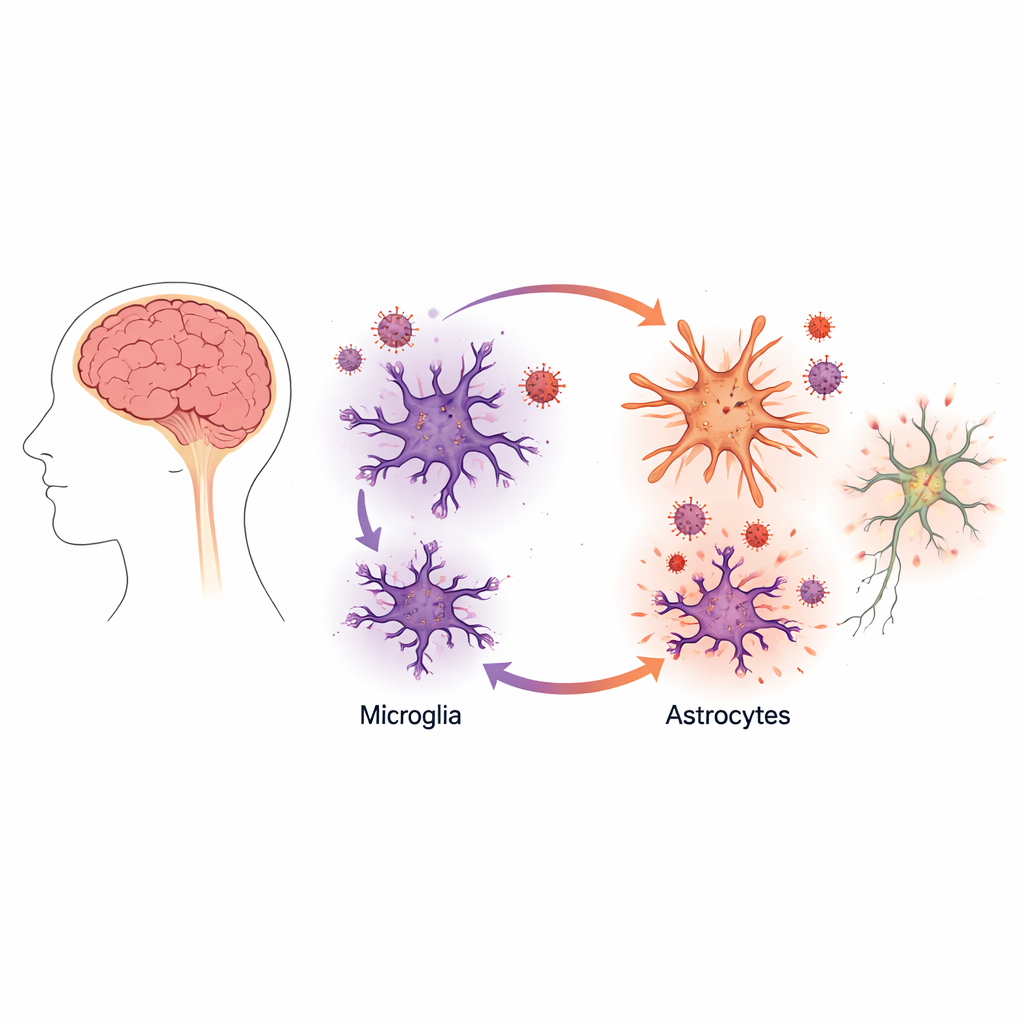
病毒增长的一个令人意外的增强
当科学家将小胶质细胞与星形胶质细胞共同培养时,情况发生了显著变化。在这些混合培养中,小胶质细胞产生的病毒量大约提高了十倍,尽管星形胶质细胞本身并未成为高产的感染宿主。仔细的成像和病毒蛋白测量显示,HIV仍然主要在小胶质细胞中复制。然而,星形胶质细胞的存在使这些被感染的小胶质细胞成为更活跃的病毒“工厂”。
为了解原因,团队检查了培养液中释放的化学信号。当星形胶质细胞暴露于来自被感染小胶质细胞的物质时,它们转向一种反应性、炎症性状态,这种变化类似于许多脑部疾病中观察到的改变。这些星形胶质细胞开始释放更多的炎症信使,包括一种称为肿瘤坏死因子α(TNFα)的分子,长期以来该分子与HIV激活有关。
炎症信号如何放大病毒“声量”
研究者接着探问TNFα是否真的在帮助HIV在小胶质细胞中复制。当他们将纯化的TNFα加入单独培养的被感染小胶质细胞时,病毒产量显著上升。在混合小胶质细胞—星形胶质细胞培养中,用一种抗体药物阻断TNFα可以降低病毒水平,但未完全恢复到基线,表明其他炎性因子也发挥作用。进一步实验指向小胶质细胞内的一个主控开关——NF-κB,这是一个进入细胞核并开启许多免疫与应激相关基因的蛋白复合体,其中包括驱动HIV转录的基因。
使用一种抑制NF-κB激活的小分子,团队能够将混合培养中被放大的病毒复制抑制回单独小胶质细胞的水平。这种处理也减少了TNFα的释放。成像显示,在感染期间,周围有星形胶质细胞的小胶质细胞相比单独培养时,NF-κB更明显地转移到细胞核内,这一转移在加入NF-κB抑制剂后被逆转。综上,这些发现勾勒出一个反馈回路:被感染的小胶质细胞扰动其周围环境,星形胶质细胞通过释放像TNFα这样的炎症信号做出反应,而这些信号反过来通过NF-κB促使小胶质细胞增加HIV产生。
溶酶体、细胞垃圾与有毒的邻里环境
该研究还探讨了被感染的小胶质细胞如何最初激怒星形胶质细胞。作者关注的是溶酶体——细胞的垃圾处理和回收中心。在被感染的小胶质细胞中,溶酶体向细胞表面移动,且其内容物的标志物(例如一种称为胱天蛋白酶B的酶)出现在周围的培养液中。这提示HIV感染促使小胶质细胞向环境排放部分消化的物质。即使是经热灭活的病毒——无法复制但仍携带病毒蛋白——也足以扰乱这种溶酶体运输。此类泄漏可能为邻近细胞创造一个长期刺激性的环境,促使星形胶质细胞进入有害的反应性状态,从而反馈并加剧炎症循环。
这对感染HIV的人意味着什么
对非专业读者而言,核心信息是:许多HIV感染者出现的大脑问题,可能不仅仅反映体内病毒总量,而更多与大脑支持细胞之间的相互交流有关。在这项工作中,被感染的小胶质细胞与反应性的星形胶质细胞形成了一个恶性循环:隐匿的病毒活动扰乱了小胶质细胞的废物处理,这激怒了星形胶质细胞,星形胶质细胞释放像TNFα这样的炎症信号,而这些信号又驱动小胶质细胞产生更多病毒。即便标准药物治疗将整体病毒水平维持在较低水平,这一局部环路也可能帮助维持炎症并导致持续缓慢的大脑损伤。研究结果指出了新的治疗方向——例如靶向TNFα、NF-κB信号通路或异常的溶酶体释放——这些策略未来或许能帮助保护那些病毒总体受控者的思维与记忆功能。
引用: Gesualdi, J., Prah, J., Solomon, S. et al. Neuroinflammatory crosstalk between microglia and astrocytes increases viral replication in an iPSC-derived model of CNS HIV infection. Sci Rep 16, 13047 (2026). https://doi.org/10.1038/s41598-026-43248-7
关键词: HIV神经认知损害, 小胶质细胞, 星形胶质细胞, 脑炎症, 肿瘤坏死因子α