Clear Sky Science · fr
Une communication neuro-inflammatoire entre microglies et astrocytes augmente la réplication virale dans un modèle dérivé de cellules souches iPSC de l’infection cérébrale par le VIH
Pourquoi l’inflammation cérébrale liée au VIH reste importante
Avec les traitements modernes du VIH, de nombreuses personnes vivent désormais longtemps et en bonne santé, et peuvent maintenir le virus à des niveaux indétectables dans le sang. Pourtant, un problème tenace demeure : une grande proportion des personnes vivant avec le VIH souffrent encore de troubles de la mémoire, d’un ralentissement de la pensée ou de difficultés de concentration, même sous traitement efficace. Cette étude pose une question centrale pour les patients et les cliniciens : si le virus est globalement contrôlé, pourquoi l’inflammation cérébrale — et le brouillard mental qui peut l’accompagner — persiste-t-elle si souvent ?
Les cellules de soutien du cerveau sous les projecteurs
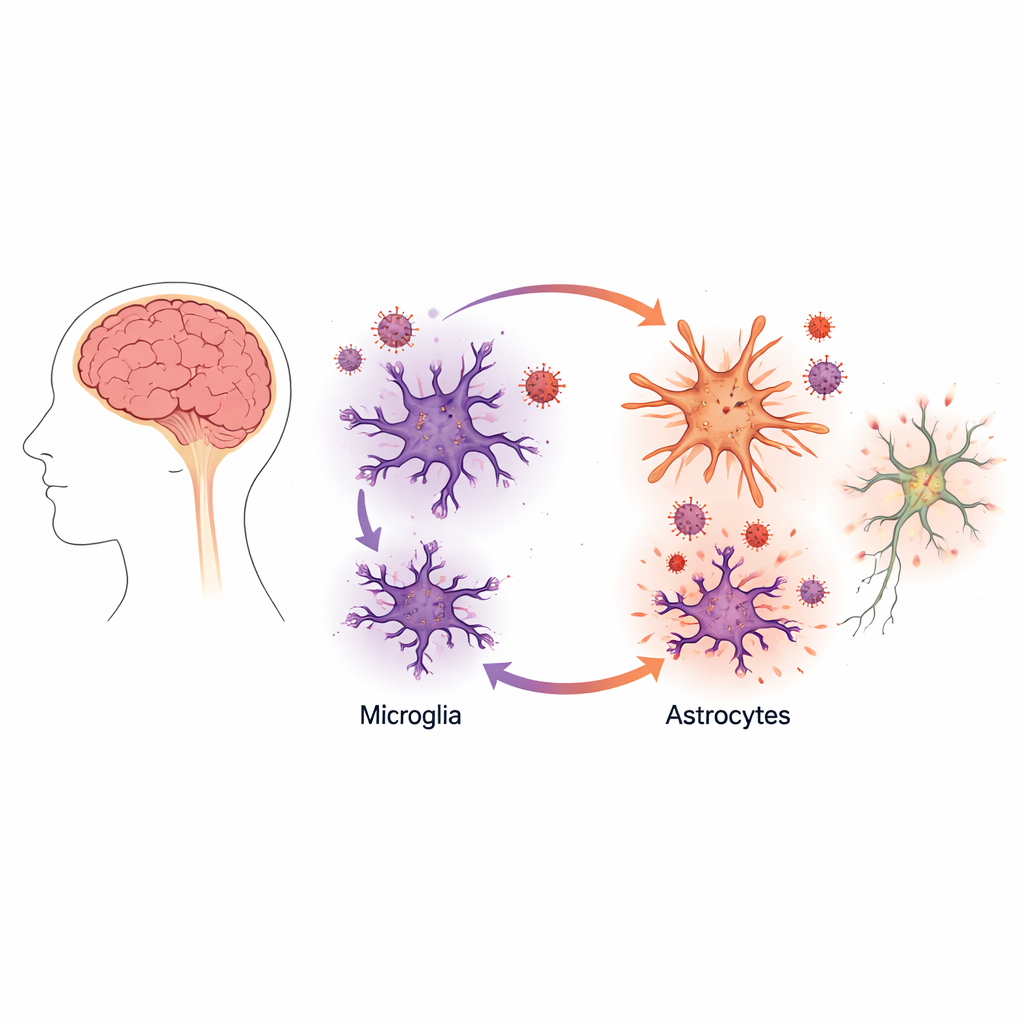
Plutôt que de se concentrer sur les neurones, les cellules nerveuses qui véhiculent les signaux, les chercheurs ont tourné leur attention vers deux types de cellules « de soutien » du cerveau : les microglies et les astrocytes. Les microglies jouent le rôle de cellules immunitaires résidentes du cerveau, tandis que les astrocytes contribuent à maintenir un environnement favorable aux neurones. L’équipe a utilisé la technologie des cellules souches humaines pour générer des versions in vitro de ces cellules — appelées microglies induites et astrocytes induits — à partir de cellules cutanées de donneurs. Cette approche leur a permis de reproduire fidèlement la biologie cérébrale humaine sans nécessiter de tissu cérébral de patients.
Ils ont d’abord vérifié que leurs microglies cultivées se comportaient comme de véritables microglies : elles présentaient la morphologie appropriée, exprimaient des gènes caractéristiques et portaient les récepteurs que le VIH utilise pour pénétrer dans les cellules. Ces microglies pouvaient être infectées par le VIH et laissaient le virus se répliquer, bien moins efficacement toutefois que dans des cellules immunitaires d’origine sanguine appelées macrophages. Contrairement aux macrophages, les microglies n’ont déclenché qu’une faible réponse inflammatoire à l’infection, produisant peu des molécules d’alerte classiques qui accompagnent généralement une forte réaction antivirale.
Une augmentation surprenante de la croissance virale
Le tableau a changé de façon spectaculaire lorsque les scientifiques ont combiné microglies et astrocytes dans la même culture. Dans ces cultures mixtes, la production virale par les microglies a augmenté d’environ dix fois, même si les astrocytes eux-mêmes n’étaient pas productivement infectés. Des imageries et des mesures précises des protéines virales ont montré que le VIH se répliquait principalement dans les microglies. La présence des astrocytes rendait toutefois ces microglies infectées bien plus efficaces comme « usines » virales.
Pour comprendre pourquoi, l’équipe a examiné les signaux chimiques libérés dans le milieu de culture. Lorsque les astrocytes étaient exposés au matériel provenant de microglies infectées, ils basculaient vers un état réactif et inflammatoire qui ressemble aux changements observés dans de nombreuses maladies cérébrales. Ces astrocytes ont commencé à libérer des niveaux plus élevés de messagers inflammatoires, dont une molécule appelée facteur de nécrose tumorale alpha (TNFα), qui est depuis longtemps associée à l’activation du VIH.
Comment les signaux inflammatoires augmentent l’activité virale
Les chercheurs ont ensuite vérifié si le TNFα favorisait réellement la réplication du VIH dans les microglies. Lorsqu’ils ont ajouté du TNFα purifié à des microglies infectées en monoculture, la production virale a augmenté de manière significative. Bloquer le TNFα dans les cultures mixtes microglies–astrocytes avec un anticorps réduit les niveaux viraux, sans toutefois les ramener entièrement au niveau de base, ce qui suggère que d’autres facteurs inflammatoires contribuent aussi. Des expériences supplémentaires ont pointé un interrupteur majeur à l’intérieur des microglies appelé NF-kB, un complexe protéique qui migre vers le noyau cellulaire et active de nombreux gènes liés à l’immunité et au stress, y compris ceux qui stimulent la transcription du VIH.
En utilisant une petite molécule bloquant l’activation de NF-kB, l’équipe a pu ramener la réplication virale amplifiée dans les cultures mixtes au niveau observé dans les microglies seules. Ce même traitement a également réduit la libération de TNFα. L’imagerie a montré que, pendant l’infection, NF-kB pénétrait davantage dans le noyau des microglies entourées d’astrocytes que dans les microglies isolées, et cette translocation était réversible en présence du bloqueur de NF-kB. Ensemble, ces résultats décrivent une boucle de rétroaction : les microglies infectées perturbent leur environnement, les astrocytes répondent en libérant des signaux inflammatoires comme le TNFα, et ces signaux poussent à leur tour les microglies à augmenter la production virale via NF-kB.
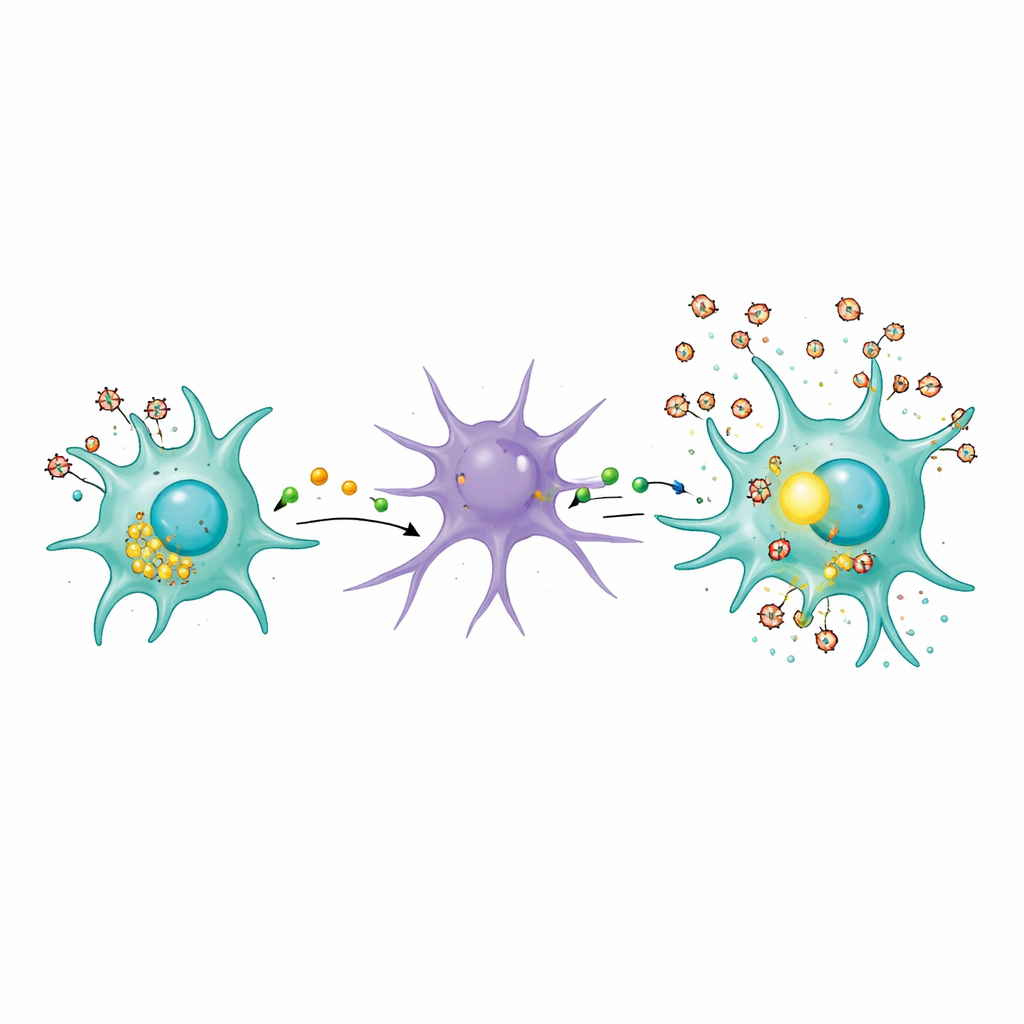
Lysosomes, déchets cellulaires et voisinage toxique
L’étude a également exploré comment les microglies infectées pouvaient initialement irriter les astrocytes. Les auteurs se sont intéressés aux lysosomes, les centres d’élimination et de recyclage des cellules. Dans les microglies infectées, les lysosomes se sont déplacés vers la surface cellulaire, et des marqueurs de leur contenu, comme une enzyme appelée cathépsine B, sont apparus dans le fluide environnant. Cela suggère que l’infection par le VIH pousse les microglies à déverser du matériel partiellement digéré dans leur environnement. Même un virus inactivé par la chaleur — incapable de se répliquer mais conservant des protéines virales — suffisait à perturber ce trafic lysosomal. Ce type de fuite peut contribuer à créer un voisinage chroniquement irritant pour les cellules voisines, poussant les astrocytes vers un état réactif délétère qui alimente à son tour le cycle inflammatoire.
Que signifient ces résultats pour les personnes vivant avec le VIH
Pour un non-spécialiste, le message principal est que les troubles cérébraux observés chez de nombreuses personnes vivant avec le VIH ne reflètent pas simplement la quantité de virus présente, mais aussi la manière dont les cellules de soutien du cerveau communiquent entre elles. Dans ce travail, microglies infectées et astrocytes réactifs forment un cercle vicieux : une activité virale discrète perturbe la gestion des déchets par les microglies, cela agite les astrocytes, les astrocytes libèrent des signaux inflammatoires comme le TNFα, et ces signaux poussent les microglies à produire davantage de virus. Même lorsque la thérapie antirétrovirale standard maintient des niveaux viraux globaux bas, cette boucle locale pourrait entretenir l’inflammation et une lésion cérébrale lente et continue. Les résultats mettent en lumière de nouvelles pistes thérapeutiques — telles que cibler le TNFα, la signalisation NF-kB ou la libération lysosomale anormale — qui pourraient un jour aider à protéger les fonctions cognitives et la mémoire chez des personnes dont le VIH est par ailleurs bien contrôlé.
Citation: Gesualdi, J., Prah, J., Solomon, S. et al. Neuroinflammatory crosstalk between microglia and astrocytes increases viral replication in an iPSC-derived model of CNS HIV infection. Sci Rep 16, 13047 (2026). https://doi.org/10.1038/s41598-026-43248-7
Mots-clés: déficit neurocognitif lié au VIH, microglies, astrocytes, inflammation cérébrale, TNF alpha