Clear Sky Science · pl
Neurozapalna komunikacja między mikroglejem a astrocytami zwiększa replikację wirusa w modelu zakażenia OUN HIV pochodzącym z iPSC
Dlaczego zapalenie mózgu w HIV wciąż ma znaczenie
Dzięki nowoczesnemu leczeniu osoby żyjące z HIV często prowadzą długie, zdrowe życie i utrzymują wirusa na poziomie niewykrywalnym we krwi. Mimo to uporczywy problem pozostaje: duża część osób z HIV wciąż doświadcza kłopotów z pamięcią, spowolnienia myślenia lub trudności ze skoncentrowaniem się, nawet przy skutecznej terapii. W tym badaniu postawiono kluczowe pytanie dla pacjentów i klinicystów: jeśli wirus jest w większości kontrolowany, dlaczego zapalenie mózgu — i wynikająca z niego mgła umysłowa — tak często utrzymują się?
Światło na komórki wspierające mózg
Zamiast skupiać się na neuronach, komórkach nerwowych przewodzących sygnały, badacze zwrócili uwagę na dwa typy komórek „wspierających” w mózgu: mikroglej i astrocyty. Mikroglej pełni rolę miejscowych komórek odpornościowych mózgu, podczas gdy astrocyty pomagają utrzymać środowisko sprzyjające neuronom. Zespół wykorzystał technologię komórek macierzystych człowieka, aby wyhodować w laboratorium wersje tych komórek — tzw. indukowany mikroglej i indukowane astrocyty — z komórek skóry dawców. Podejście to pozwoliło na wierne odtworzenie ludzkiej biologii mózgu bez konieczności pozyskiwania tkanki mózgowej od pacjentów.
Pierwsze potwierdzenia wykazały, że hodowane w laboratorium mikrogleje zachowywały się jak prawdziwe mikrogleje: miały odpowiedni kształt, wyrażały charakterystyczne geny i posiadały receptory, których HIV używa do wejścia do komórek. Te mikrogleje mogły ulegać zakażeniu HIV i pozwalały wirusowi na replikację, choć nie tak efektywnie jak komórki odpornościowe pochodzące z krwi znane jako makrofagi. W przeciwieństwie do makrofagów, mikroglej wywoływał jedynie słabą odpowiedź zapalną na zakażenie, produkując niewiele klasycznych molekuł alarmowych towarzyszących silnej reakcji przeciwwirusowej.
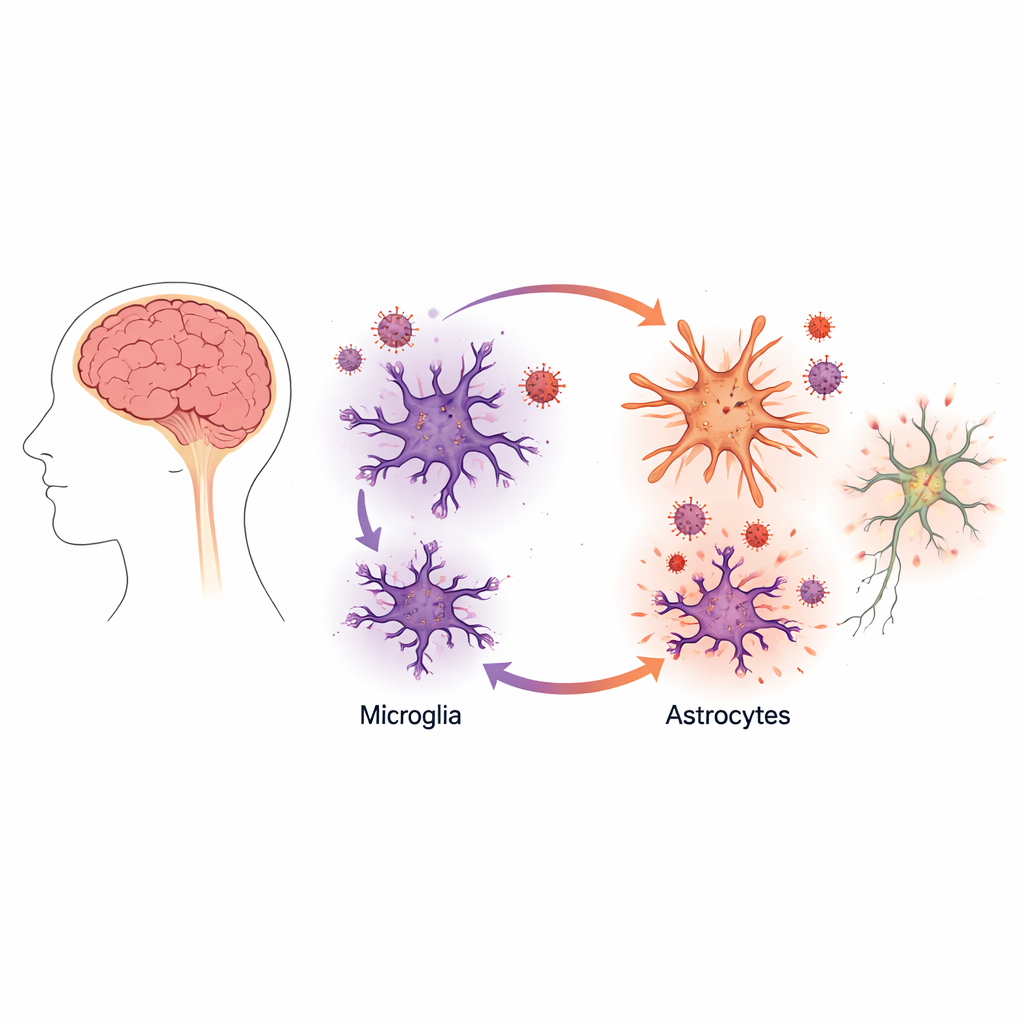
Zaskakujące wzmocnienie wzrostu wirusa
Obraz zmienił się dramatycznie, gdy naukowcy połączyli mikroglej z astrocytami w tej samej hodowli. W kulturach mieszanych produkcja wirusa przez mikroglej wzrosła około dziesięciokrotnie, mimo że same astrocyty nie ulegały produktywnemu zakażeniu. Dokładne obrazowanie i pomiary białek wirusowych wykazały, że HIV nadal replikował się głównie w mikrogleju. Obecność astrocytów sprawiała jednak, że zakażone mikrogleje stały się znacznie bardziej aktywnymi „fabrykami” wirusa.
Aby zrozumieć przyczynę, zespół zbadał sygnały chemiczne uwalniane do płynu hodowlanego. Gdy astrocyty były wystawione na materiał pochodzący z zakażonych mikroglejów, przeszły w reaktywny, zapalny stan przypominający zmiany obserwowane w wielu chorobach mózgu. Astrocyty zaczęły uwalniać wyższe poziomy komunikatorów zapalnych, w tym cząsteczkę zwaną czynnikiem martwicy guza alfa (TNFα), która od dawna kojarzona jest z aktywacją HIV.
Jak sygnały zapalne podkręcają wirusa
Następnie badacze zapytali, czy TNFα rzeczywiście pomaga HIV replikować się w mikrogleju. Gdy dodano oczyszczony TNFα do zakażonych mikroglejów hodowanych osobno, produkcja wirusa wzrosła znacząco. Zablokowanie TNFα w mieszanych kulturach mikrogleju i astrocytów za pomocą przeciwciała obniżyło poziomy wirusa, choć nie całkowicie do wartości wyjściowej, co sugeruje, że inne czynniki zapalne również się przyczyniają. Dalsze eksperymenty wskazały na główny przełącznik wewnątrz mikrogleju zwany NF-kB, kompleks białkowy, który przemieszcza się do jądra komórkowego i włącza wiele genów związanych z odpornością i stresem, w tym tych napędzających transkrypcję HIV.
Używając małej cząsteczki blokującej aktywację NF-kB, zespół był w stanie obniżyć nasiloną replikację wirusa w kulturach mieszanych do poziomu obserwowanego w mikrogleju hodowanym osobno. To samo leczenie także zmniejszyło uwalnianie TNFα. Obrazowanie wykazało, że podczas zakażenia NF-kB przemieszczał się do jądra silniej w mikrogleju otoczonym przez astrocyty niż w mikrogleju samodzielnym, a ten przesunienie odwracało się po podaniu inhibitora NF-kB. Razem te odkrycia opisują pętlę sprzężenia zwrotnego: zakażone mikrogleje zaburzają swoje otoczenie, astrocyty odpowiadają uwalnianiem sygnałów zapalnych takich jak TNFα, a te sygnały z kolei pobudzają mikroglej do zwiększonej produkcji wirusa za pośrednictwem NF-kB.
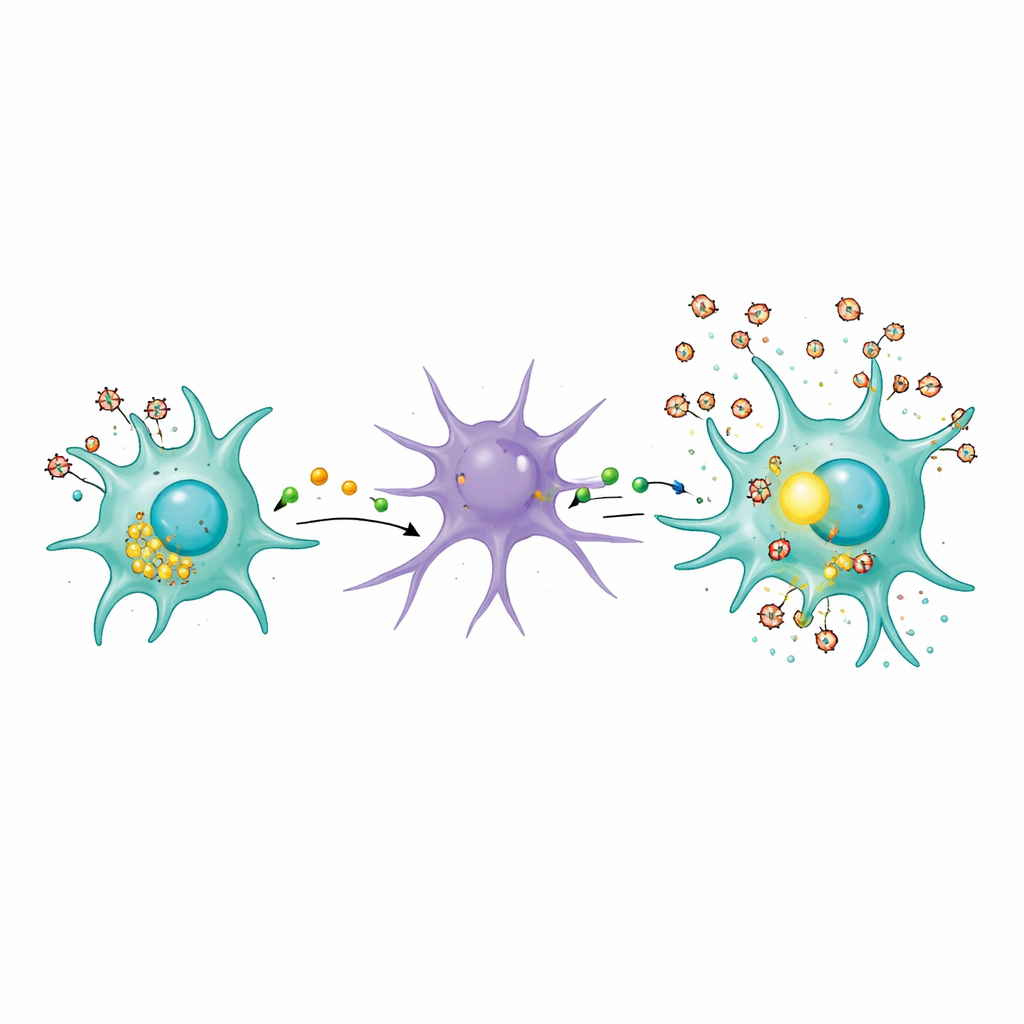
Lizosomy, komórkowe odpady i toksyczne sąsiedztwo
Badanie zbadało też, jak zakażone mikrogleje mogą początkowo drażnić astrocyty. Autorzy skupili się na lizosomach, centrach utylizacji i recyklingu komórkowego. W zakażonych mikroglejach lizosomy przemieszczały się w kierunku powierzchni komórki, a markery ich zawartości, takie jak enzym katego-psyna B, pojawiały się w otaczającym płynie. Sugeruje to, że zakażenie HIV skłania mikroglej do wyrzucania częściowo strawionego materiału do środowiska. Nawet wirus nieaktywny termicznie — niezdolny do replikacji, ale wciąż niosący białka wirusowe — wystarczał, by zaburzyć ten ruch lizosomalny. Taki wyciek może tworzyć przewlekle drażniące otoczenie dla pobliskich komórek, popychając astrocyty w szkodliwy, reaktywny stan, który dalej wzmacnia cykl zapalny.
Co to oznacza dla osób żyjących z HIV
Dla osoby niebędącej specjalistą główne przesłanie jest takie, że problemy mózgowe obserwowane u wielu osób z HIV mogą nie odzwierciedlać wyłącznie ilości wirusa, lecz sposób, w jaki komórki wspierające mózg komunikują się między sobą. W tej pracy zakażone mikrogleje i reaktywne astrocyty tworzą błędne koło: subtelna aktywność wirusowa zaburza gospodarkę odpadami mikrogleju, to z kolei pobudza astrocyty, astrocyty uwalniają sygnały zapalne jak TNFα, a te sygnały skłaniają mikroglej do wytwarzania większej ilości wirusa. Nawet gdy standardowa terapia lekowa utrzymuje ogólne poziomy wirusa nisko, ta lokalna pętla może podtrzymywać zapalenie i powodować powolne, trwające uszkodzenie mózgu. Wyniki wskazują nowe kierunki terapeutyczne — takie jak celowanie w TNFα, sygnalizację NF-kB lub nieprawidłowe uwalnianie lizosomów — które mogłyby w przyszłości pomóc chronić myślenie i pamięć u osób, których HIV jest inaczej dobrze kontrolowany.
Cytowanie: Gesualdi, J., Prah, J., Solomon, S. et al. Neuroinflammatory crosstalk between microglia and astrocytes increases viral replication in an iPSC-derived model of CNS HIV infection. Sci Rep 16, 13047 (2026). https://doi.org/10.1038/s41598-026-43248-7
Słowa kluczowe: HIV i upośledzenie funkcji poznawczych, mikroglej, astrocyty, zapalenie mózgu, TNF alfa