Clear Sky Science · de
Neuroinflammatorische Kommunikation zwischen Mikroglia und Astrozyten erhöht die Virusreplikation in einem iPSC-abgeleiteten Modell der HIV-Infektion des ZNS
Warum Gehirnentzündungen bei HIV weiterhin relevant sind
Dank moderner HIV-Therapien führen viele Menschen heute ein langes, gesundes Leben und können das Virus im Blut auf nachweisbar niedrigen Werten halten. Ein hartnäckiges Problem bleibt jedoch: ein großer Teil der Menschen mit HIV leidet trotz wirksamer Behandlung weiter unter Gedächtnisproblemen, verlangsamtem Denken oder Konzentrationsstörungen. Diese Studie stellt eine zentrale Frage für Patientinnen, Patienten und behandelnde Ärztinnen und Ärzte: Wenn das Virus größtenteils unter Kontrolle ist, warum bestehen Gehirnentzündungen — und die damit verbundene „Gehirnnebel“-Symptomatik — so häufig fort?
Die Stützzellen des Gehirns im Fokus
Anstatt die Neuronen, also die Nervenzellen, die Signale übertragen, in den Mittelpunkt zu stellen, richteten die Forschenden ihre Aufmerksamkeit auf zwei „Stützzell“-Typen im Gehirn: Mikroglia und Astrozyten. Mikroglia fungieren als die residenten Immunzellen des Gehirns, während Astrozyten ein gesundes Umfeld für Neuronen aufrechterhalten. Das Team verwendete menschliche Stammzelltechnologie, um im Labor gezüchtete Versionen dieser Zellen — sogenannte induzierte Mikroglia und induzierte Astrozyten — aus Spender-Hautzellen zu erzeugen. Dieser Ansatz erlaubte es, die menschliche Gehirnbiologie genau nachzubilden, ohne auf Hirngewebe von Patientinnen oder Patienten zurückgreifen zu müssen.
Zunächst bestätigten sie, dass ihre im Labor gezüchteten Mikroglia sich wie echte Mikroglia verhielten: sie wiesen die typische Gestalt auf, exprimierten charakteristische Gene und trugen die Rezeptoren, die HIV zur Zellinvasion nutzt. Diese Mikroglia konnten von HIV infiziert werden und erlaubten derart die Virusreplikation, wenn auch nicht so effizient wie blutabgeleitete Immunzellen, die als Makrophagen bekannt sind. Im Gegensatz zu Makrophagen zeigten die Mikroglia nur eine schwache Entzündungsreaktion auf die Infektion und produzierten nur wenige der klassischen Alarmmoleküle, die normalerweise mit einer starken antiviralen Reaktion einhergehen.
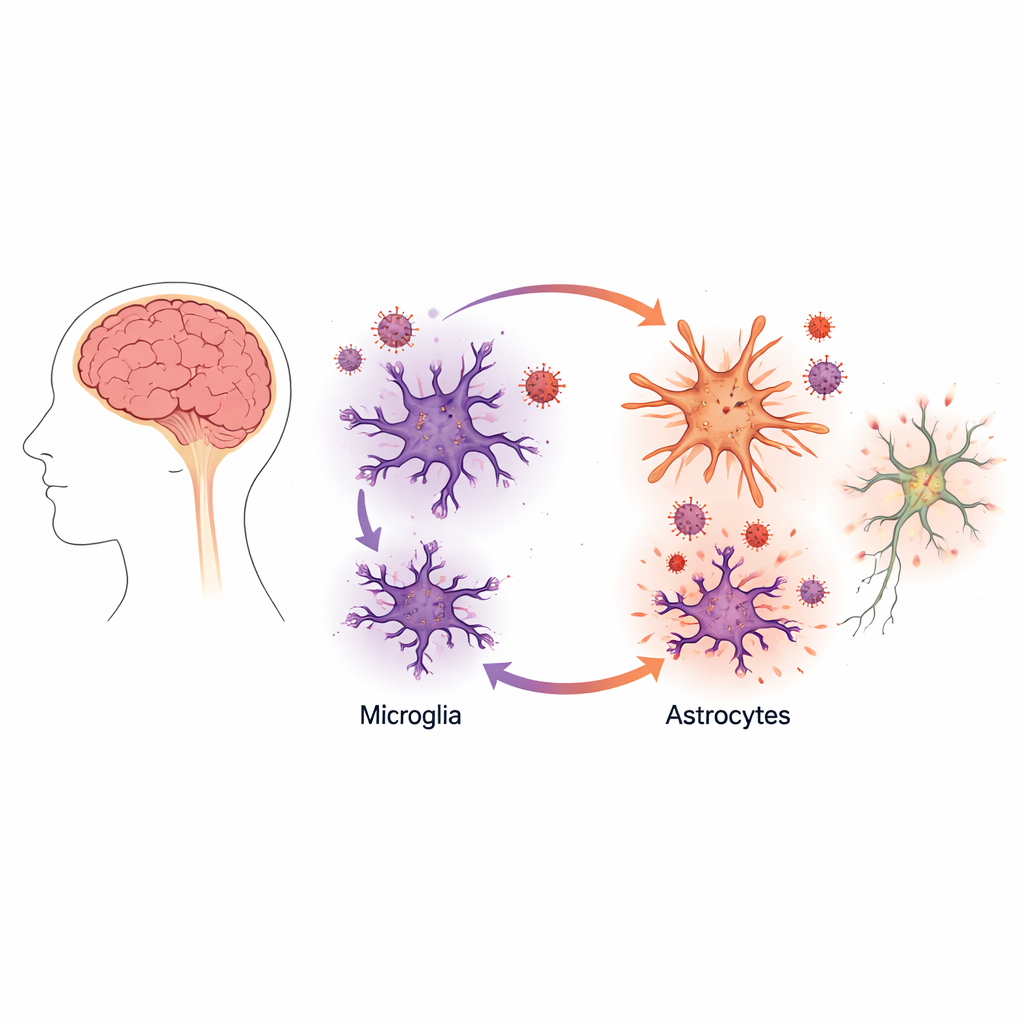
Ein überraschender Anstieg der Virusvermehrung
Das Bild änderte sich dramatisch, als die Wissenschaftler Mikroglia und Astrozyten gemeinsam in derselben Kultur zusammenbrachten. In diesen Mischkulturen stieg die Virusproduktion durch Mikroglia um etwa das Zehnfache an, obwohl die Astrozyten selbst nicht produktiv infiziert wurden. Sorgfältige Bildgebung und Messungen viraler Proteine zeigten, dass HIV weiterhin hauptsächlich in den Mikroglia replizierte. Die Anwesenheit von Astrozyten verwandelte die infizierten Mikroglia jedoch in deutlich aktivere Virusfabriken.
Um zu verstehen, warum das so war, untersuchte das Team die chemischen Signale, die in das Kulturmedium freigesetzt wurden. Wurden Astrozyten Material aus infizierten Mikroglia ausgesetzt, schalteten sie in einen reaktiven, entzündlichen Zustand um, der Veränderungen ähnelt, wie man sie bei vielen Gehirnerkrankungen beobachtet. Diese Astrozyten begannen, höhere Mengen entzündlicher Botenstoffe freizusetzen, darunter ein Molekül namens Tumornekrosefaktor alpha (TNFα), das seit langem mit HIV-Aktivierung in Verbindung gebracht wird.
Wie Entzündungssignale die Virusmenge erhöhen
Die Forschenden fragten dann, ob TNFα tatsächlich die HIV-Replikation in Mikroglia fördert. Als sie gereinigtes TNFα zu allein kultivierten, infizierten Mikroglia gaben, stieg die Virusproduktion deutlich an. Das Blockieren von TNFα in gemischten Mikroglia–Astrozyten-Kulturen mit einem Antikörperpräparat reduzierte die Virusmengen, wenn auch nicht vollständig auf Ausgangsniveau, was darauf hindeutet, dass auch andere entzündliche Faktoren beitragen. Weitere Experimente deuteten auf einen zentralen Schalter innerhalb der Mikroglia hin: den NF-kB-Komplex, ein Proteinkomplex, der in den Zellkern wandert und viele immun- und stressbezogene Gene aktiviert, einschließlich jener, die die HIV-Transkription antreiben.
Mithilfe eines kleinen Moleküls, das die NF-kB-Aktivierung blockiert, gelang es dem Team, die gesteigerte Virusreplikation in den Mischkulturen auf das Niveau zu reduzieren, das in Mikroglia allein beobachtet wurde. Diese Behandlung verringerte zudem die TNFα-Freisetzung. Bildgebende Verfahren zeigten, dass während der Infektion NF-kB stärker in den Zellkern wanderte, wenn Mikroglia von Astrozyten umgeben waren, als bei allein kultivierten Mikroglia, und dass dieser Kerntranslokation durch den NF-kB-Blocker entgegengewirkt wurde. Zusammen skizzieren diese Befunde einen Rückkopplungsmechanismus: infizierte Mikroglia stören ihre Umgebung, Astrozyten reagieren mit der Freisetzung entzündlicher Signale wie TNFα, und diese Signale treiben Mikroglia über NF-kB dazu, mehr HIV zu produzieren.
Lysosomen, zellulärer Abfall und eine toxische Nachbarschaft
Die Studie untersuchte außerdem, wie infizierte Mikroglia die Astrozyten anfänglich aufwühlen könnten. Die Autorinnen und Autoren konzentrierten sich auf Lysosomen, die Abfallentsorgungs- und Recyclingzentren der Zelle. In infizierten Mikroglia verschoben sich Lysosomen in Richtung Zelloberfläche, und Marker ihres Inhalts, etwa ein Enzym namens Cathepsin B, tauchten in der umgebenden Flüssigkeit auf. Dies deutet darauf hin, dass HIV-Infektion Mikroglia dazu veranlasst, teilweise verdautes Material in ihre Umgebung zu entlassen. Selbst hitzeinaktiviertes Virus — nicht replizierfähig, aber noch mit viralen Proteinen beladen — reichte aus, um diesen lysosomalen Verkehr zu stören. Ein solcher Austritt kann ein chronisch reizendes Umfeld für benachbarte Zellen schaffen und Astrozyten in einen schädlichen reaktiven Zustand drängen, der die entzündliche Schleife weiter nährt.
Was das für Menschen mit HIV bedeutet
Für Nichtfachleute ist die Kernbotschaft, dass die Gehirnprobleme, die viele Menschen mit HIV betreffen, nicht allein vom Gesamtviruslastniveau abhängen müssen, sondern davon, wie sich die Stützzellen im Gehirn gegenseitig beeinflussen. In dieser Arbeit bilden infizierte Mikroglia und reaktive Astrozyten einen Teufelskreis: subtile virale Aktivität stört das Abfallmanagement der Mikroglia, dies reizt Astrozyten, Astrozyten setzen entzündliche Signale wie TNFα frei, und diese Signale treiben Mikroglia dazu, mehr Virus zu produzieren. Selbst wenn eine Standardtherapie die gesamte Viruslast niedrig hält, kann dieser lokale Kreislauf Entzündungen aufrechterhalten und zu langsamem, fortschreitendem Hirnschaden beitragen. Die Ergebnisse heben neue therapeutische Ansatzpunkte hervor — etwa die gezielte Hemmung von TNFα, der NF-kB-Signalkaskade oder abnormer Lysosomenfreisetzung —, die eines Tages helfen könnten, Denken und Gedächtnis bei Menschen mit ansonsten gut kontrolliertem HIV zu schützen.
Zitation: Gesualdi, J., Prah, J., Solomon, S. et al. Neuroinflammatory crosstalk between microglia and astrocytes increases viral replication in an iPSC-derived model of CNS HIV infection. Sci Rep 16, 13047 (2026). https://doi.org/10.1038/s41598-026-43248-7
Schlüsselwörter: HIV-bedingte neurokognitive Beeinträchtigung, Mikroglia, Astrozyten, Gehirnentzündung, TNF alpha