Clear Sky Science · ar
الحوار النّوْعيُّ الالتهابي بين الخلايا الدَّقيقة والدبقية يزيد تكاثُر الفيروس في نموذج مشتق من الخلايا الجذعية متعددة القدرات لعدوى HIV في الجهاز العصبي المركزي
لماذا يظل التهاب الدماغ في حالة عدوى HIV مهماً
بفضل علاجات HIV الحديثة، يعيش كثير من الأشخاص الآن حياة طويلة وصحية ويمكنهم إبقاء الفيروس عند مستويات غير قابلة للكشف في الدم. ومع ذلك، هناك مشكلة مستمرة: لا يزال جزء كبير من المصابين بـ HIV يعانون من مشكلات في الذاكرة، تباطؤ التفكير، أو صعوبة في التركيز، حتى أثناء تلقي العلاج الفعّال. تسأل هذه الدراسة سؤالاً حاسماً للمرضى والأطباء على حد سواء: إذا كان الفيروس محكومًا إلى حد كبير، فلماذا يستمر التهاب الدماغ — والضباب الذهني المصاحب له — بهذه الشيوع؟
تسليط الضوء على خلايا الدعم الدماغية
بدلاً من التركيز على الخلايا العصبية، أي الخلايا التي تنقل الإشارات، وجه الباحثون اهتمامهم إلى نوعين من "خلايا الدعم" في الدماغ: الخلايا الدُّقَيْقة (الميكروغليا) والخلايا النجمية (الأستروسايت). تعمل الميكروغليا كالخلايا المناعية المقيمة في الدماغ، بينما تساعد الخلايا النجمية في الحفاظ على بيئة صحية للخلايا العصبية. استخدم الفريق تقنية الخلايا الجذعية البشرية لزراعة نسخ مخبرية من هذه الخلايا — سمّوها ميكروغليا مُستحثّة وخلايا نجمية مُستحثّة — من خلايا جلدية للمتبرعين. أتاح هذا النهج تقليد بيولوجيا الدماغ البشري عن قرب دون الحاجة إلى نسيج دماغي من المرضى.
أولاً، تأكدوا من أن الميكروغليا المزروعة في المختبر تصرفت كالميكروغليا الحقيقية: اتخذت الشكل المناسب، عبّرت عن الجينات المميزة، وحملت المستقبلات التي يستخدمها HIV لدخول الخلايا. كان بالإمكان إصابة هذه الميكروغليا بـ HIV وسمحت بتكاثر الفيروس، وإن لم يكن بكفاءة مشابهة لخلايا المناعة المشتقة من الدم المعروفة بالبلعميات (ماكروفاجات). وعلى عكس البلعمات، أظهرت الميكروغليا استجابة التهابية ضعيفة نسبياً للعدوى، حيث أنتجت القليل من جزيئات الإنذار الكلاسيكية المصاحبة عادةً لاستجابة مضادة للفيروسات قوية.
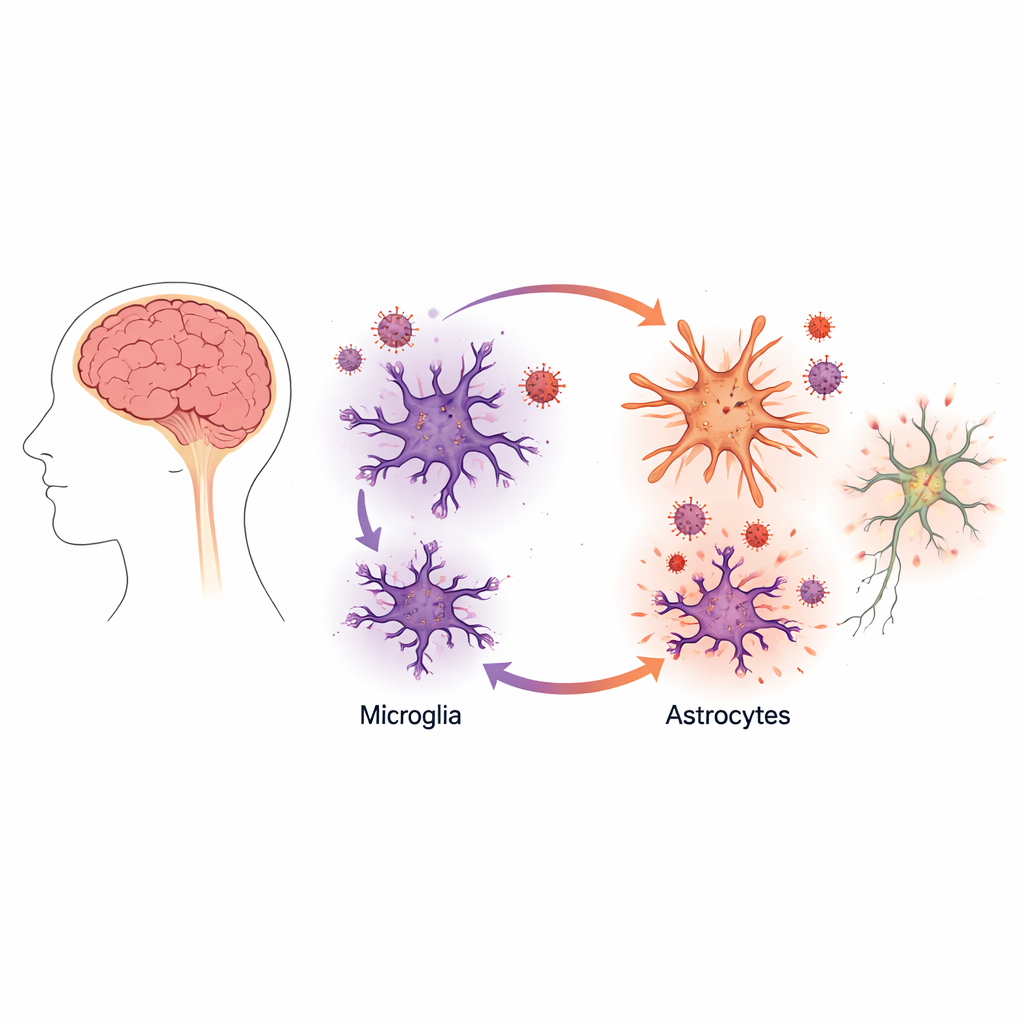
زيادة مفاجئة في نمو الفيروس
تغير المشهد بدرجة كبيرة عندما جمع العلماء الميكروغليا مع الخلايا النجمية في نفس الطبق. في هذه المُزارعات المختلطة، ارتفع إنتاج الفيروس من الميكروغليا بحوالي عشرة أضعاف، رغم أن الخلايا النجمية نفسها لم تُصب إصابة منتجة. أظهرت التصويرات والقياسات الدقيقة لبروتينات الفيروس أن HIV ظل يتكاثر أساسًا في الميكروغليا. ومع ذلك، شكلت وجود الخلايا النجمية مفاعلاً جعل الميكروغليا المصابة مصانع فيروسية أكثر نشاطاً بكثير.
لفهم السبب، فحص الفريق الإشارات الكيميائية المطروحة في سائل الزراعة. عندما تعرضت الخلايا النجمية لمواد من ميكروغليا مصابة، انتقلت إلى حالة تفاعلية التهابية تشبه التغيرات المرصودة في العديد من أمراض الدماغ. بدأت هذه الخلايا النجمية بإفراز مستويات أعلى من المرسلّات الالتهابية، بما في ذلك جزيء يُدعى عامل نخر الورم ألفا (TNFα)، الذي ارتبط طويلاً بتنشيط HIV.
كيف ترفع الإشارات الالتهابية مستوى الفيروس
ثم تساءل الباحثون عمّا إذا كان TNFα يساعد فعلاً HIV على التكاثر داخل الميكروغليا. عندما أضافوا TNFα المنقى إلى ميكروغليا مصابة مزروعة بمفردها، ارتفع إنتاج الفيروس بشكل ملحوظ. أدى حجب TNFα في المزارعات المختلطة للميكروغليا والخلايا النجمية باستخدام دواء مضاد للأجسام المضادة إلى خفض مستويات الفيروس، وإن لم يعدها بالكامل إلى خط الأساس، مما يشير إلى أن عوامل التهابية أخرى تساهم أيضاً. أشارت تجارب إضافية إلى مفتاح تحكّم داخل الميكروغليا يُدعى NF-kB، وهو مركب بروتيني يدخل نواة الخلية ويفعّل العديد من الجينات المناعية والمتعلقة بالإجهاد، بما في ذلك تلك التي تقود النسخ الفيروسي لـ HIV.
باستخدام جزيء صغير يعيق تفعيل NF-kB، تمكن الفريق من خفض تكاثر الفيروس المرتفع في المزارعات المختلطة إلى المستوى المرصود في الميكروغليا وحدها. خفّض هذا العلاج نفسه أيضاً إفراز TNFα. أظهرت الصور أنه أثناء العدوى، تحوّل NF-kB إلى النواة بقوة أكبر في الميكروغليا المحاطة بالخلايا النجمية مقارنة بالميكروغليا المنفردة، وعكس هذا الانتقال عند وجود مثبط NF-kB. تضع هذه النتائج معاً حلقة ارتجاعية: تزعج الميكروغليا المصابة محيطها، تستجيب الخلايا النجمية بإطلاق إشارات التهابية مثل TNFα، وتدفع تلك الإشارات بدورها الميكروغليا إلى زيادة إنتاج الفيروس عبر NF-kB.
الليسوسومات، نفايات الخلايا، والحي المحيط السام
تعمقت الدراسة أيضاً في كيفية إثارة الميكروغليا المصابة للخلايا النجمية مبدئياً. ركز المؤلفون على الليسوسومات، مراكز التخلص من النفايات وإعادة التدوير داخل الخلية. في الميكروغليا المصابة، تحركت الليسوسومات باتجاه سطح الخلية، وظهرت مؤشرات محتوياتها، مثل إنزيم يُدعى كاتيبسين ب (cathepsin B)، في السائل المحيط. يشير هذا إلى أن عدوى HIV تدفع الميكروغليا إلى طرح مواد مهضومة جزئياً إلى بيئتها. حتى الفيروس المعطل بالحرارة — غير القادر على التكاثر ولكنه يحمل بروتينات فيروسية — كان كافياً لتعكير هذه الحركة الليسوسومية. يمكن لمثل هذا التسرب أن يخلق محيطاً مزعجاً بشكل مزمن للخلايا القريبة، دافعاً الخلايا النجمية إلى حالة تفاعلية ضارة تُغذي بدورها الدورة الالتهابية.
ماذا يعني هذا للأشخاص الذين يعيشون مع HIV
بالنسبة لغير المتخصص، الرسالة الرئيسة هي أن المشكلات الدماغية التي يُرى أنها تصيب العديد من الأشخاص المصابين بـ HIV قد لا تعكس ببساطة مقدار الفيروس الموجود، بل كيف تتواصل خلايا الدعم الدماغية مع بعضها البعض. في هذا العمل، تشكل الميكروغليا المصابة والخلايا النجمية التفاعلية دائرة شرّيرة: النشاط الفيروسي الطفيف يخلّ بتعامل الميكروغليا مع النفايات، يهيّج هذا الخلايا النجمية، تطلق الخلايا النجمية إشارات التهابية مثل TNFα، وتدفع تلك الإشارات الميكروغليا لإنتاج المزيد من الفيروس. حتى عندما تحافظ العلاجات الدوائية القياسية على مستويات فيروسية منخفضة بشكل عام، يمكن أن يساعد هذا الحلقة المحلية في استمرار الالتهاب وإحداث إصابة دماغية بطيئة ومستمرة. تبرز النتائج زوايا علاجية جديدة — مثل استهداف TNFα أو إشارة NF-kB أو الإفراز الليسوسومي غير الطبيعي — التي قد تساعد يوماً ما في حماية التفكير والذاكرة لدى الأشخاص الذين يكون فيروس HIV لديهم مضبوطاً بخلاف ذلك.
الاستشهاد: Gesualdi, J., Prah, J., Solomon, S. et al. Neuroinflammatory crosstalk between microglia and astrocytes increases viral replication in an iPSC-derived model of CNS HIV infection. Sci Rep 16, 13047 (2026). https://doi.org/10.1038/s41598-026-43248-7
الكلمات المفتاحية: ضعف الإدراك المرتبط بفيروس HIV, الخلايا الدقيقة (ميكروغليا), الخلايا النجمية (أستروسايت), التهاب الدماغ, عامل نخر الورم ألفا (TNF alpha)