Clear Sky Science · ja
iPSC由来中枢神経系HIV感染モデルにおけるミクログリアとアストロサイト間の神経炎症クロストークがウイルス複製を増加させる
なぜHIVにおける脳の炎症は依然重要なのか
現代のHIV治療により、多くの人が長く健康な生活を送れるようになり、血中ウイルス量を検出限界以下に抑えられるようになりました。それでも根強い問題が残ります。多くのHIV感染者が、治療を受けていても記憶障害、思考の遅れ、集中困難などを経験し続けているのです。本研究は、患者と臨床家の双方にとって重要な問いを投げかけます。ウイルスが大部分で制御されているときになぜ脳の炎症――そしてそれに伴う精神的な霞のような症状――がこれほどしばしば持続するのか?
注目を浴びる脳の支持細胞
研究者たちは信号を伝える神経細胞(ニューロン)に焦点を当てるのではなく、脳の二つの「支持」細胞型、ミクログリアとアストロサイトに注目しました。ミクログリアは脳の常在免疫細胞のように働き、アストロサイトはニューロンのための健全な環境維持を助けます。研究チームはヒトの幹細胞技術を用いて、ドナーの皮膚細胞から誘導ミクログリアと誘導アストロサイトと呼ばれる試験管内で作製した細胞を育てました。この手法により、患者の脳組織を用いることなくヒトの脳生物学を忠実に模倣できます。
まず彼らは、培養したミクログリアが本物のミクログリアのように振る舞うことを確認しました:形態が適切で、特徴的な遺伝子を発現し、HIVが細胞に侵入するために使う受容体を持っていました。これらのミクログリアはHIVに感染し、ウイルスを増殖させることができましたが、血液由来の免疫細胞であるマクロファージほど効率的ではありませんでした。マクロファージとは異なり、ミクログリアは感染に対して弱い炎症反応しか示さず、通常の強い抗ウイルス反応に伴う典型的なアラーム分子をほとんど産生しませんでした。
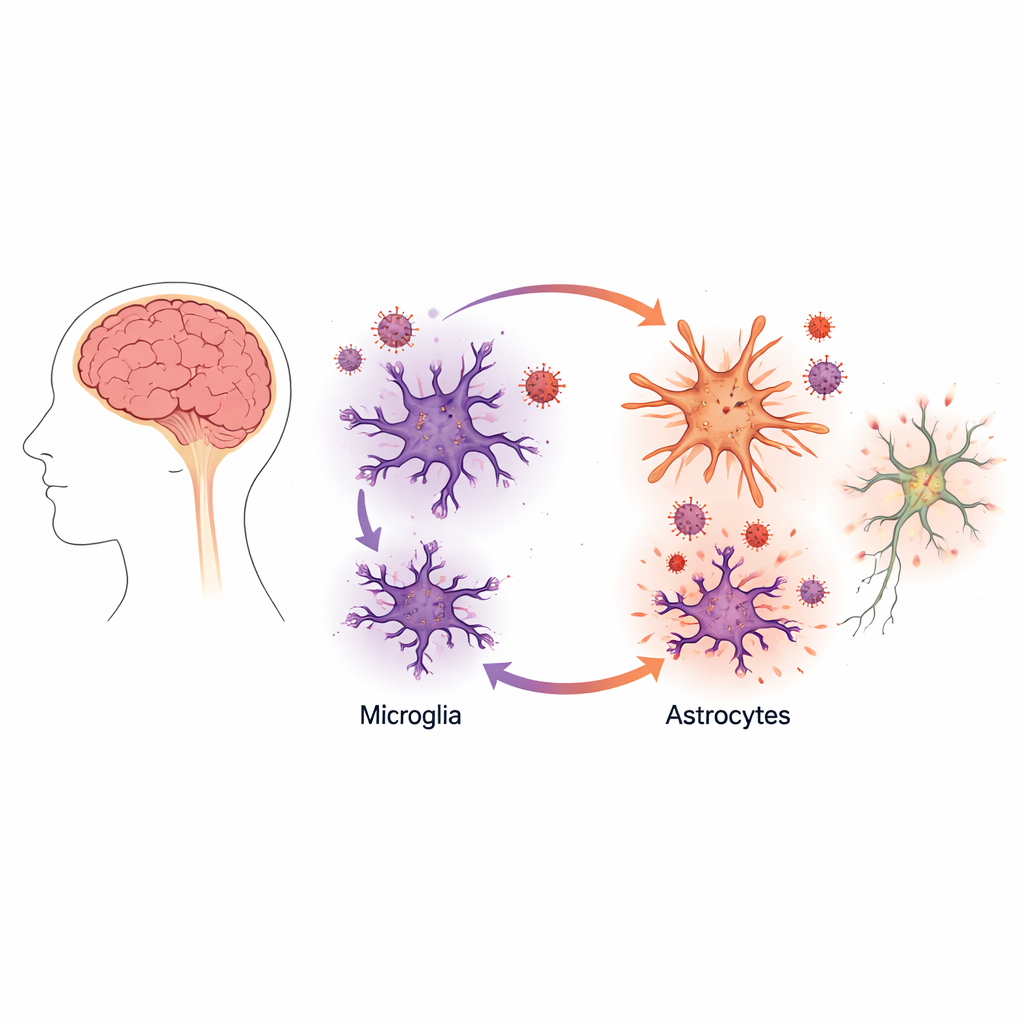
驚くべきウイルス増殖の促進
状況が劇的に変わったのは、ミクログリアとアストロサイトを同じ皿で共培養したときです。こうした混合培養では、ミクログリアによるウイルス産生が約10倍に急増しましたが、アストロサイト自体は生産的に感染しているわけではありませんでした。詳細なイメージングとウイルスタンパク質の測定により、HIVは主にミクログリアで増殖していることが示されました。しかしアストロサイトの存在が、感染したミクログリアをはるかに活発なウイルス製造工場に変えていました。
その理由を理解するために、チームは培養液に放出された化学的シグナルを調べました。感染したミクログリア由来の物質に曝されたアストロサイトは、多くの脳疾患で見られるような反応性の炎症状態に変化しました。これらのアストロサイトは、長くHIV活性化と結びついてきた分子である腫瘍壊死因子アルファ(TNFα)を含む、炎症性シグナルの放出を増加させ始めました。
炎症シグナルがウイルス活動を増幅する仕組み
研究者らは次に、TNFαが実際にミクログリアにおけるHIV複製を助けているかどうかを問いました。精製TNFαを単独培養の感染ミクログリアに添加すると、ウイルスの産出は有意に増加しました。混合ミクログリア–アストロサイト培養で抗体薬によりTNFαを阻害するとウイルスレベルは低下しましたが、基準値まで完全には戻らず、他の炎症因子も寄与していることを示唆しました。さらなる実験は、ミクログリア内部のマスタースイッチであるNF-κBに注目しました。NF-κBは細胞核に移行して多くの免疫およびストレス関連遺伝子をオンにし、HIVの転写を駆動する因子も含みます。
NF-κBの活性化を阻害する小分子を用いると、混合培養で増大していたウイルス複製をミクログリア単独のレベルまで低下させることができました。同じ処置はTNFαの放出も低下させました。イメージングでは、感染時にNF-κBはアストロサイトに囲まれたミクログリアで単独ミクログリアより強く核へ移行し、この移行はNF-κB阻害剤の存在下で逆転しました。これらの結果はフィードバックループの存在を描き出します:感染ミクログリアが周囲を攪乱し、アストロサイトがTNFαのような炎症シグナルを放出して応答し、それらのシグナルがNF-κBを介してミクログリアにHIV産生を促進させるのです。
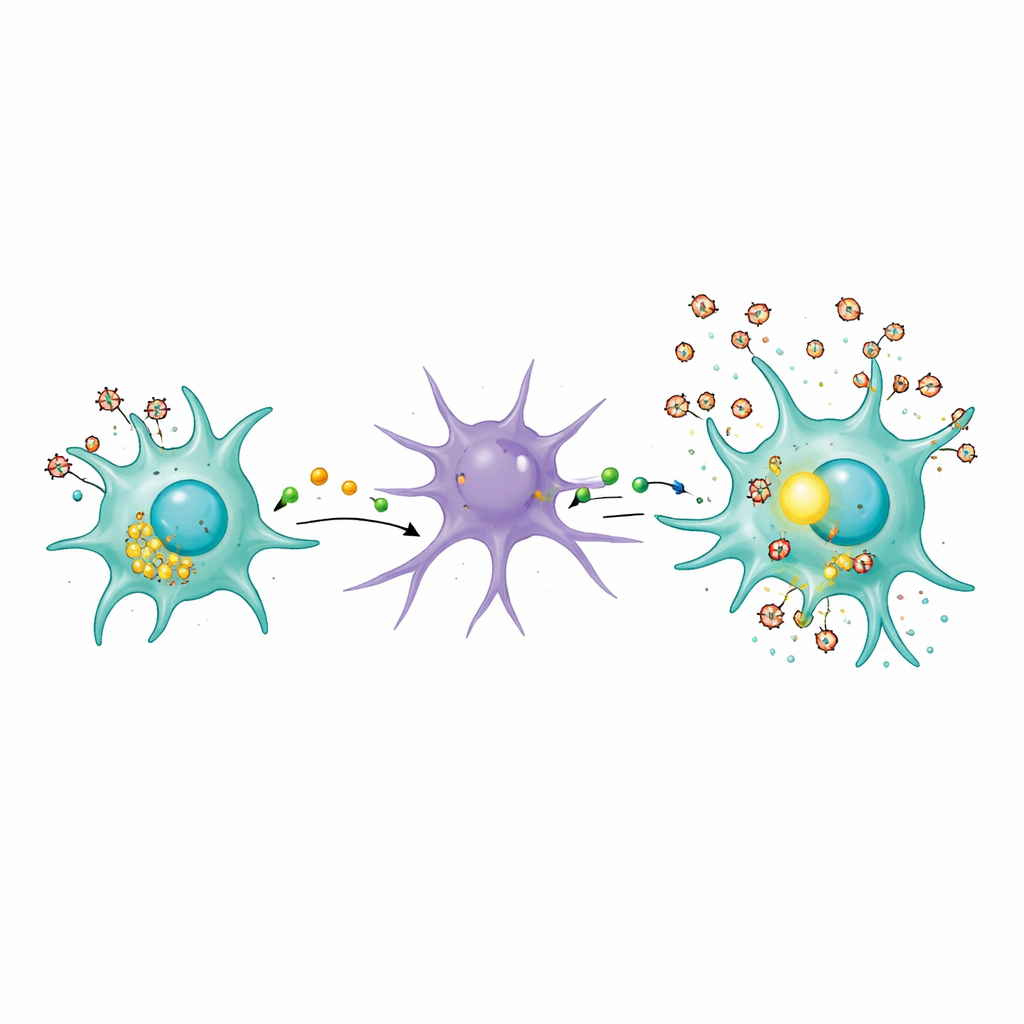
リソソーム、細胞のゴミ処理、そして有害な近隣環境
研究はまた、感染ミクログリアがどのようにして最初にアストロサイトを刺激するのかを探りました。著者らはリソソーム、すなわち細胞の廃棄・リサイクルセンターに注目しました。感染したミクログリアではリソソームが細胞表面側へ移動し、その内容物のマーカー(カテプシンBなどの酵素)が周囲の培養液に現れていました。これはHIV感染がミクログリアに部分的に消化された物質を周囲に排出させることを示唆します。複製できないがウイルスタンパク質を保持する熱不活化ウイルスでさえ、このリソソーム輸送を乱すのに十分でした。そのような漏出は近隣細胞に慢性的な刺激的環境を作り出し、アストロサイトを有害な反応状態へと促し、炎症サイクルに逆戻りさせる可能性があります。
HIV陽性者にとっての意味
非専門家向けの主なメッセージは、多くのHIV陽性者に見られる脳機能の問題は、単に体内のウイルス量だけを反映するのではなく、脳の支持細胞同士の相互作用のあり方によって左右される可能性があるということです。本研究では、感染ミクログリアと反応性アストロサイトが悪循環を形成しています。微妙なウイルス活動がミクログリアの廃棄処理を乱し、それがアストロサイトを刺激し、アストロサイトはTNFαのような炎症シグナルを放出し、それらのシグナルがミクログリアにさらにウイルス産生を促させます。標準的な薬物療法で全体的なウイルス量が低く抑えられていても、この局所的なループは炎症と進行性の脳障害を持続させることがあり得ます。これらの知見は、TNFαやNF-κBシグナル伝達、異常なリソソーム放出などを標的とする新たな治療戦略が、HIVが十分に制御されている人々の認知機能と記憶を守る助けになる可能性を示しています。
引用: Gesualdi, J., Prah, J., Solomon, S. et al. Neuroinflammatory crosstalk between microglia and astrocytes increases viral replication in an iPSC-derived model of CNS HIV infection. Sci Rep 16, 13047 (2026). https://doi.org/10.1038/s41598-026-43248-7
キーワード: HIVによる神経認知機能障害, ミクログリア, アストロサイト, 脳の炎症, TNFα