Clear Sky Science · it
Crosstalk neuroinfiammatorio tra microglia e astrociti aumenta la replicazione virale in un modello iPSC-derived di infezione HIV nel SNC
Perché l’infiammazione cerebrale nell’HIV è ancora rilevante
Con i trattamenti moderni per l’HIV, molte persone oggi vivono vite lunghe e in buona salute e riescono a mantenere il virus a livelli non rilevabili nel sangue. Tuttavia permane un problema ostinato: una larga parte delle persone con HIV continua a sperimentare difficoltà di memoria, rallentamento del pensiero o problemi di concentrazione, anche durante terapie efficaci. Questo studio pone una domanda cruciale per pazienti e clinici: se il virus è per lo più controllato, perché l’infiammazione cerebrale — e la confusione mentale che ne può derivare — persiste così spesso?
Le cellule di supporto del cervello sotto i riflettori
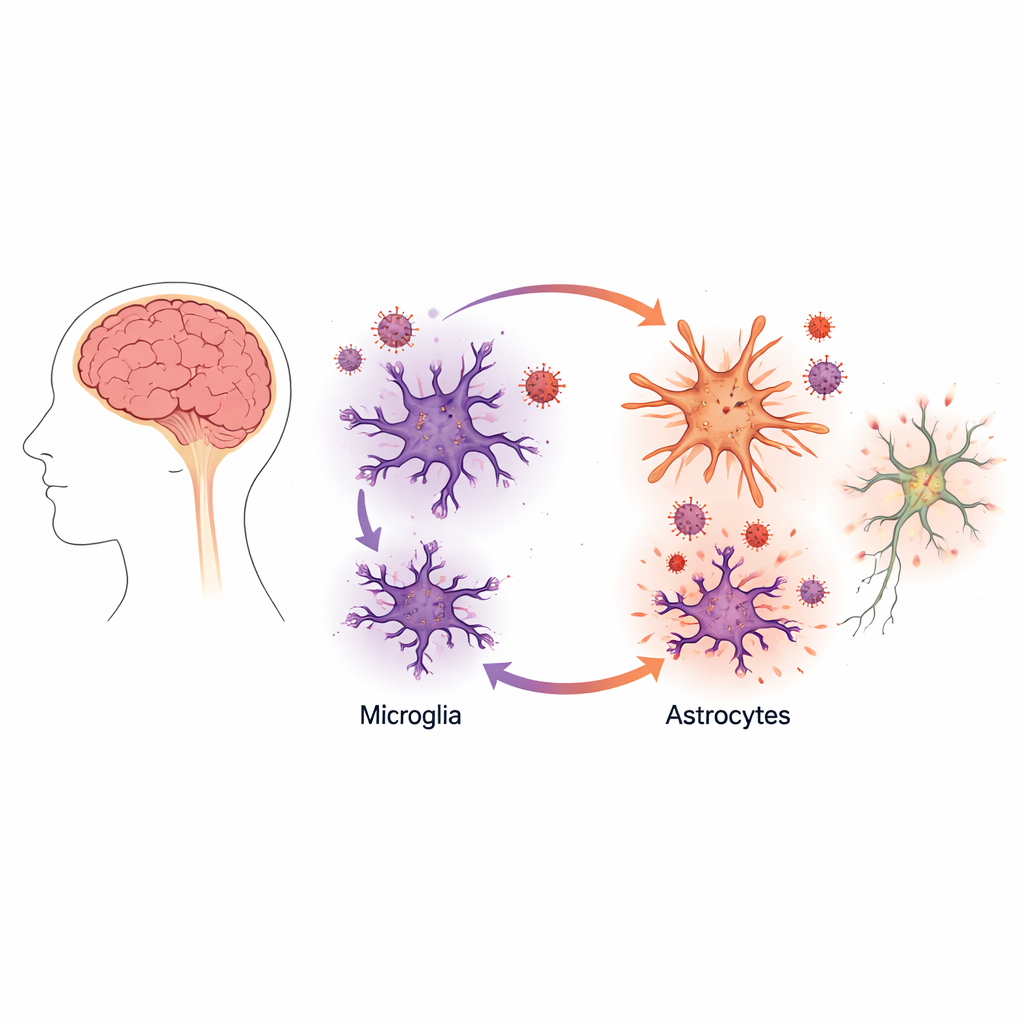
Invece di concentrarsi sui neuroni, le cellule nervose che trasmettono segnali, i ricercatori hanno rivolto l’attenzione a due tipi di cellule “di supporto” nel cervello: microglia e astrociti. Le microglia agiscono come cellule immunitarie residenti del cervello, mentre gli astrociti contribuiscono a mantenere un ambiente sano per i neuroni. Il team ha usato la tecnologia delle cellule staminali umane per crescere versioni in laboratorio di queste cellule — chiamate microglia indotte e astrociti indotti — a partire da cellule cutanee di donatori. Questo approccio ha permesso di riprodurre fedelmente la biologia cerebrale umana senza necessitare di tessuto cerebrale umano.
Per prima cosa, hanno confermato che le microglia coltivate in laboratorio si comportavano come microglia autentiche: avevano la morfologia corretta, esprimevano geni caratteristici e possedevano i recettori che l’HIV usa per entrare nelle cellule. Queste microglia potevano essere infettate dall’HIV e permettere la replicazione virale, sebbene non in modo efficiente come nelle cellule immunitarie derivate dal sangue note come macrofagi. A differenza dei macrofagi, le microglia hanno montato solo una debole risposta infiammatoria all’infezione, producendo poche delle molecole di allarme classiche associate a una forte reazione antivirale.
Un sorprendente aumento della crescita virale
Il quadro è cambiato drasticamente quando gli scienziati hanno combinato microglia e astrociti nella stessa coltura. In queste colture miste, la produzione di virus da parte delle microglia è aumentata di circa dieci volte, anche se gli astrociti stessi non risultavano produttivamente infettati. Imaging accurato e misurazioni delle proteine virali hanno mostrato che l’HIV replicava ancora principalmente nelle microglia. La presenza degli astrociti, tuttavia, trasformava quelle microglia infette in fabbriche virali molto più attive.
Per capire il perché, il team ha esaminato i segnali chimici rilasciati nel liquido di coltura. Quando gli astrociti sono stati esposti a materiale proveniente da microglia infette, sono passati a uno stato reattivo e infiammatorio che ricorda i cambiamenti osservati in molte malattie cerebrali. Questi astrociti hanno cominciato a rilasciare livelli più alti di messaggeri infiammatori, incluso una molecola chiamata fattore di necrosi tumorale alfa (TNFα), collegata da tempo all’attivazione dell’HIV.
Come i segnali infiammatori aumentano il volume virale
I ricercatori si sono poi chiesti se il TNFα aiutasse effettivamente l’HIV a replicare nelle microglia. Quando hanno aggiunto TNFα purificato a microglia infette coltivate da sole, la produzione virale è aumentata in modo significativo. Bloccare il TNFα nelle colture miste microglia–astrociti con un anticorpo riduceva i livelli di virus, sebbene non riportandoli completamente ai valori di base, suggerendo che anche altri fattori infiammatori contribuiscono. Ulteriori esperimenti hanno indicato un interruttore maestro all’interno delle microglia chiamato NF-kB, un complesso proteico che si sposta nel nucleo cellulare e attiva molti geni legati all’immunità e allo stress, inclusi quelli che promuovono la trascrizione dell’HIV.
Usando una piccola molecola che blocca l’attivazione di NF-kB, il team è riuscito a ridurre la replicazione virale aumentata nelle colture miste fino ai livelli osservati nelle microglia coltivate da sole. Questo stesso trattamento ha inoltre ridotto il rilascio di TNFα. L’imaging ha mostrato che, durante l’infezione, NF-kB si spostava verso il nucleo in modo più marcato nelle microglia circondate da astrociti rispetto alle microglia isolate, e questo spostamento veniva invertito quando era presente l’inibitore di NF-kB. Nel complesso, questi risultati delineano un circuito di retroazione: le microglia infette disturbano il loro ambiente, gli astrociti rispondono rilasciando segnali infiammatori come il TNFα, e questi segnali a loro volta spingono le microglia a incrementare la produzione virale tramite NF-kB.
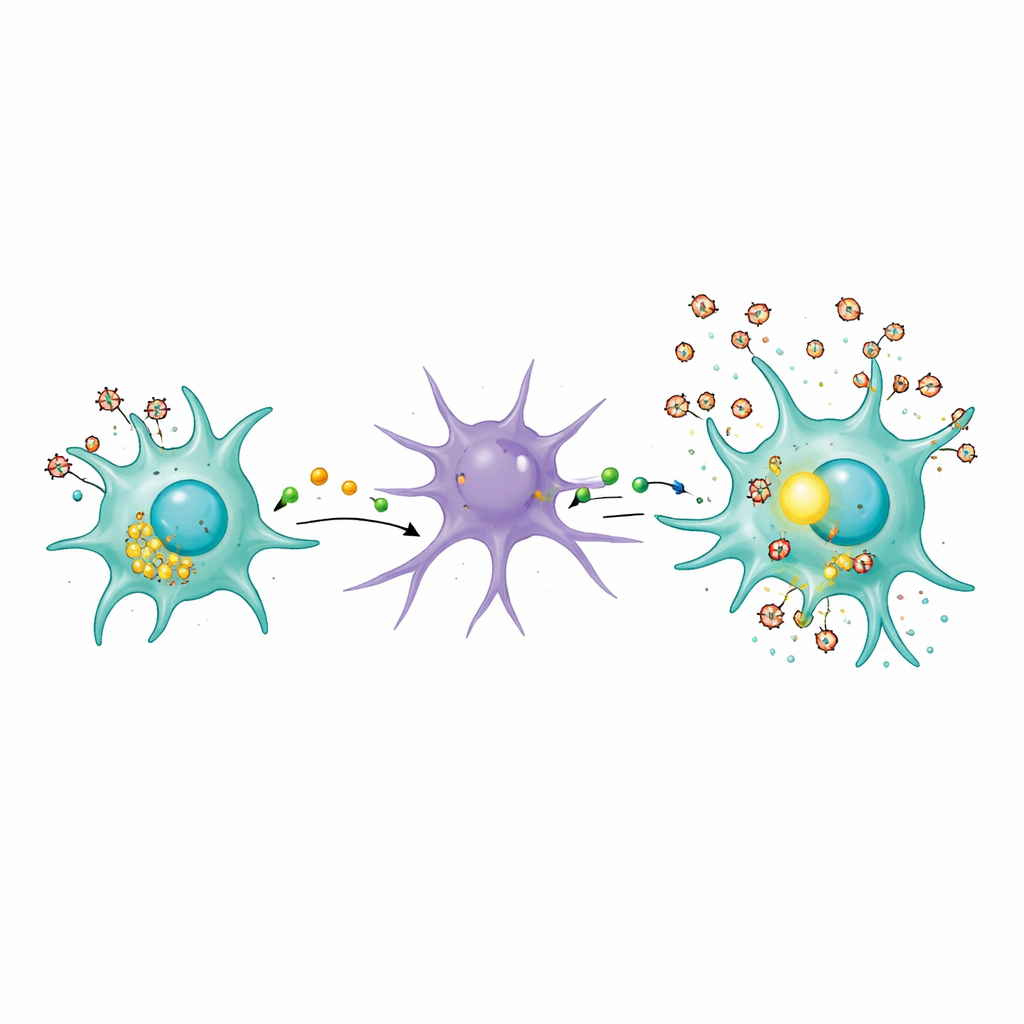
Lisosomi, rifiuti cellulari e un vicinato tossico
Lo studio ha anche indagato come le microglia infette possano inizialmente irritare gli astrociti. Gli autori si sono concentrati sui lisosomi, i centri di smaltimento e riciclo della cellula. Nelle microglia infette, i lisosomi si sono spostati verso la superficie cellulare e marcatori del loro contenuto, come un enzima chiamato catepsina B, sono comparsi nel fluido circostante. Ciò suggerisce che l’infezione da HIV induca le microglia a scaricare materiale parzialmente digerito nell’ambiente. Anche virus inattivati dal calore — incapaci di replicare ma ancora portatori di proteine virali — erano sufficienti a perturbare questo traffico lisosomiale. Tale fuoriuscita può contribuire a creare un ambiente cronicamente irritante per le cellule vicine, spingendo gli astrociti in uno stato reattivo dannoso che alimenta ulteriormente il ciclo infiammatorio.
Cosa significa questo per le persone che vivono con l’HIV
Per un non specialista, il messaggio principale è che i problemi cerebrali riscontrati in molte persone con HIV potrebbero non riflettere semplicemente la quantità complessiva di virus presente, ma il modo in cui le cellule di supporto cerebrali comunicano tra loro. In questo lavoro, microglia infette e astrociti reattivi formano un circolo vizioso: un’attività virale sottile altera la gestione dei rifiuti delle microglia, ciò irrita gli astrociti, gli astrociti rilasciano segnali infiammatori come il TNFα, e questi segnali inducono le microglia a produrre più virus. Anche quando la terapia standard mantiene bassi i livelli virali sistemici, questo circuito locale potrebbe contribuire a sostenere l’infiammazione e un lento danno cerebrale progressivo. I risultati mettono in luce nuovi approcci terapeutici — come il targeting del TNFα, della segnalazione NF-kB o del rilascio anomalo dei lisosomi — che un giorno potrebbero aiutare a proteggere funzione cognitiva e memoria in persone il cui HIV è altrimenti ben controllato.
Citazione: Gesualdi, J., Prah, J., Solomon, S. et al. Neuroinflammatory crosstalk between microglia and astrocytes increases viral replication in an iPSC-derived model of CNS HIV infection. Sci Rep 16, 13047 (2026). https://doi.org/10.1038/s41598-026-43248-7
Parole chiave: Compromissione neurocognitiva da HIV, microglia, astrociti, infiammazione cerebrale, TNF alfa